Tijdens het symposium 'When to optimize heart failure treatment' hebben Michel Komajda (Frankrijk), Michael Böhm (Duitsland) en Martin Cowie (Engeland) de huidige behandeling van patiënten met hartfalen geanalyseerd en nagegaan hoe die behandeling geoptimaliseerd kan worden. De sessie werd voorgezeten door Stefan Anker (Duitsland).
Professor Stefan Anker gaf eerst een korte inleiding. Hij wees op de hoge prevalentie van hartfalen wereldwijd en op het feit dat de prognose slecht blijft hoewel de laatste jaren veel vooruitgang geboekt werd.
Michel Komajda heeft vervolgens geanalyseerd in welke mate de richtlijnen voor de behandeling van hartfalen nageleefd worden.
Hij zei dat er heel wat vooruitgang geboekt werd in de behandeling van hartfalen, waardoor er de laatste decennia minder sterfgevallen waren,1 maar hij betreurde het hoge aantal hernieuwde ziekenhuisopnames,2 meestal wegens hartdecompensatie.3 Daarom moet bijzondere aandacht besteed worden aan de behandelingen (geneesmiddelen of medische hulpmiddelen) die de prognose verbeteren en de ziekte stabiliseren.
De laatste jaren worden dit soort geneesmiddelen vaker voorgeschreven,4 maar nog te vaak in een te lage dosering.3 Uit de QUALIFY-studie, een observationele studie die uitgevoerd werd bij meer dan 7 000 patiënten in 547 centra in 36 landen (tussen september 2013 en december 2014), bleek dat slechts 14,8 % van de patiënten de streefdosering van de bètablokker kreeg.5 Verschillende studies hebben nochtans de gunstige effecten van bètablokkers in de maximale streefdosering aangetoond. De ATLAS-studie (1999) toonde aan dat het gecombineerde criterium (sterfte/ziekenhuisopname) 12 % lager was bij gebruik van lisinopril in de maximale dosering in vergelijking met een lagere dosering van lisinopril.6 Ook de MOCHA-studie (1996), die verschillende doseringen van carvedilol en een placebo vergeleken heeft, toonde aan dat het aantal sterfgevallen duidelijk lager lag in de groep die behandeld werd met carvedilol 25 mg 2x/d.7 Uit de HEAAL-studie (2009) bleek ook dat het gecombineerde criterium (sterfte/ziekenhuisopname) wegens hartfalen lager was in de groep die behandeld werd met losartan 150 mg, in vergelijking met de groep die behandeld werd met losartan 50 mg.8 Er zijn tal van redenen waarom suboptimale doseringen voorgeschreven worden. Zo is een leeftijd van 75 jaar of ouder een onafhankelijke indicator voor het voorschrijven van een suboptimale dosering.9 Ook kan de organisatie van de behandeling van patiënten met hartfalen na een ziekenhuisverblijf te wensen overlaten. Volgens een analyse van de universitaire ziekenhuizen in Parijs meldt ongeveer 20 % van de patiënten zich niet aan op de controleconsultatie (omdat er iets gebeurd is of zonder reden); 72 % van de patiënten komt wel op controle, maar niet snel genoeg (45 pas na ± 28 dagen).10
Michel Komajda zei tot slot dat het naleven van de richtlijnen bij het voorschrijven van de aanbevolen geneesmiddelen het aantal sterftegevallen en hernieuwde ziekenhuisopnames op middellange termijn verlaagt.11
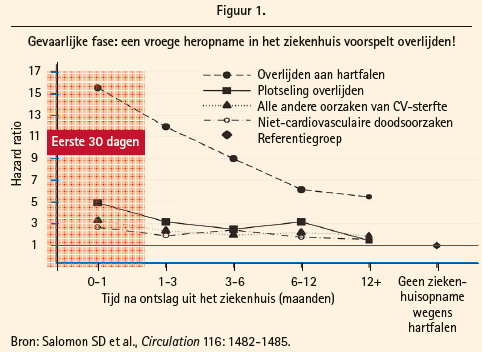
Michael Böhm pleit voor een snelle optimalisering van de behandeling voor hartfalen gezien het hoge risico op hernieuwde ziekenhuisopname en de duidelijke stijging van de sterftegevallen na een ziekenhuisopname wegens hartdecompensatie.12 De gevaarlijkste fase is de eerste maand na het ziekenhuisverblijf. Daarom is het zo belangrijk om de evidentiegebaseerde behandeling voor hartfalen snel te optimaliseren (figuur 1).13
De hartfrequentie heeft een voorspellende waarde: het risico stijgt met 15,6 % telkens wanneer de hartfrequentie met 5 slagen per minuut toeneemt.14 In de SHIFT-studie werd bovendien een daling van het gecombineerde criterium (cardiovasculaire sterfte en ziekenhuisopname wegens hartfalen) met 18 % waargenomen in de ivabradinegroep, waarin een lagere hartfrequentie werd verkregen.15 Een post-hocanalyse van die studie toonde aan dat langdurige toediening van ivabradine het risico op hernieuwde ziekenhuisopname tijdens de gevaarlijke periode (1-3 maanden na ontslag uit het ziekenhuis) verlaagt.16 27 patiënten moeten gedurende een jaar behandeld worden met ivabradine (NNT, number needed tot treat) om een eerste ziekenhuisopname wegens hartfalen te vermijden en per jaar moeten 14 patiënten opgevolgd worden om een hernieuwde ziekenhuisopname te voorkomen.17
Comorbiditeit gaat gepaard met een hoger aantal cardiovasculaire accidenten (cardiovasculaire sterfte en ziekenhuisopname).18 Die comorbiditeit kan optreden via endotheeldisfunctie, oxidatieve stress en ontsteking (wat kan leiden tot een ruptuur van de atheroomplaat met een infarct), toename van de remodellering, orgaanlijden en tot slot multiorgaanfalen.
Martin Cowie besprak de behandeling vóór ontslag uit het ziekenhuis en de aanpak op lange termijn.
De richtlijnen raden momenteel aan om voor ontslag een schema op te stellen met de voorziene consultaties (binnen een week bij de huisarts en binnen twee weken bij de cardioloog) en een programma om de dosering van evidentiegebaseerde geneesmiddelen te verhogen en om na te gaan of de patiënt in aanmerking komt voor een pacemaker of defibrillator. De patiënten moeten ook opgenomen worden in een programma voor hartfalen.19 Ondanks die aanbevelingen betreurt Martin Cowie dat nog geen 10 % van de Britse patiënten die het ziekenhuis verlaten na een episode van hartdecompensatie binnen twee weken terugkeert naar de hartfalenkliniek. Hij merkt ook op dat het erg moeilijk blijkt te zijn de richtlijnen in de praktijk toe te passen. Daarnaast wees hij ook op de tolerantieproblemen die zich kunnen voordoen bij het verhogen van de dosering. In zijn praktijk heeft meer dan 53 % van de patiënten nog een HF > 70/min. ondanks pogingen om de dosering van de bètablokker te verhogen.
Hij gaf enkele tips om de behandeling te optimaliseren. Zo zou een ambulante patiënt die op spreekuur komt in de hartfalenkliniek snel geholpen moeten kunnen worden met wat hij nodig heeft (bloedafname, radiografie, apotheek).
Het programma 'Optimize Heart Failure Care' werd opgesteld om de behandeling van hartfalen na een ziekenhuisopname te verbeteren. Dat programma wordt toegepast in 45 landen. Het bestaat uit initiatieven betreffende het voorschrijven van een geschikte behandeling (klinische protocollen aangepast aan de lokale middelen, checklist voor en na ontslag uit het ziekenhuis), educatie van de patiënt (app voor smartphone, 'my HF passport' om ervoor te zorgen dat de patiënt de ziekte beter begrijpt, de behandeling beter naleeft en actief meewerkt bij de follow-up) en de planning na ontslag.

De ervaring met dat programma leert dat de steun van lokale specialisten in hartfalen, regelmatige educatieve vergaderingen en een multidisciplinaire samenwerking vereist zijn om het programma te doen slagen. Volgens preliminaire resultaten verbetert het programma de farmacologische behandeling en zijn daar weinig nieuwe investeringen voor nodig.
Referenties
- Laribi, S., Trends in death attributed to heart failure over the past two decades in Europe. Eur J Heart Fail, 2012, 1, 234-239.
- Heidenreich, P.A. et al. Divergent trends in survival and readmission following a hospitalization for heart failure in the Veterans Affairs health care system 2002 to 2006. J Am Coll Cardiol, 2010, 56 (5), 362- 368.
- Maggioni, A.P., Dahlström, U., Filippatos, G., Chioncel, O., Crespo Leiro, M., Drozdz., J, et al.; Heart Failure Association of the European Society of Cardiology (HFA). EURObservational Research Programme: regional differences and 1-year follow-up results of the Heart Failure Pilot Survey (ESC-HF Pilot). Eur J Heart Fail, 2013, 15, 808-817.
- Crespo Leiro, M.G., Anker, S.D., Maggioni, A.P., Coats, A.J., Filippatos, G., Ruschitzka, F. et al. European Society of Cardiology Heart Failure Long-Term Registry (ESC-HF-LT): 1-year follow-up outcomes and differences across regions. Eur J Heart Fail, 2016, 18, 613-625.
- Komajda, M., Anker, S.D., Cowie, M.R., Filippatos, G.S., Mengelle, B., Ponikowski, P. et al. Physicians' adherence to guidelinerecommended medications in heart failure with reduced ejection fraction: data from the QUALIFY global survey. Eur J Heart Fail, 2016, 18, 514- 522.
- Packer, M. et al. Comparative effects of low and high doses of the angiotensin-converting enzyme inhibitor, lisinopril, on morbidity and mortality in chronic heart failure. ATLAS Study Group. Circulation, 1999, 100, 2312-2318.
- Bristow, M.R., Gilbert, E.M., Abraham, W.T., Adams, K.F., Fowler, M.B., Hershberger, R.E. et al. Carvedilol produces dose-related improvements in left ventricular function and survival in subjects with chronic heart failure. MOCHA Investigators et al. Circulation, 1996, 94, 2807-2816.
- Konstam, M.A., Neaton, J.D., Dickstein, K. et al. Effects of high-dose versus low-dose losartan on clinical outcomes in patients with heart failure (HEAAL study): a randomised, double-blind trial. Lancet, 2009, 374, 1840-1848.
- De Groote, P., Isnard, R., Clerson, P., et al. Improvement in the management of chronic heart failure since the publication of the updated guidelines of the European Society of Cardiology. The Impact-Reco Programme. Eur J Heart Fail, 2009, 11, 85-91.
- F. Laveau et al, Archives of Cardiovascular Diseases, Volume 110, Issue 1, 2017, 42-50.
- Komajda, M., Cowie, M.R., Tavazzi, L., Ponikowski, P., Anker, S.D., Filippatos, G.S.; QUALIFY Investigators. Physicians' guideline adherence is associated with better prognosis in outpatients with heart failure with reduced ejection fraction: the QUALIFY international registry. Eur J Heart Fail, 2017, doi: 10.1002/ejhf.887 [Epub ahead of print].
- Abrahamsson, P. Swedberg, K., Borer, J.S., Böhm, M., Kober, L., Komajda, M. et al. Risk following hospitalization in stable chronic systolic heart failure. Eur J Heart Fail, 2013, 15 (8), 885-891.
- Solomon, S.D. Influence of nonfatal hospitalization for heart failure on subsequent mortality in patients with chronic heart failure. Circulation, 2007, 116, 1482-1487.
- Böhm, M., Swedberg, K., Komajda, M., Borer, J.S., Ford, I., Dubost-Brama, A. et al.; SHIFT Investigators. Heart rate as a risk factor in chronic heart failure (SHIFT): the association between heart rate and outcomes in a randomised placebo-controlled trial. Lancet, 2010, 376, 886-894.
- Swedberg, K., Komajda, M., Böhm, M., Borer, J.S., Ford, I., Dubost-Brama, A., Lerebours, G., Tavazzi, L.; SHIFT Investigators. Ivabradine and outcomes in chronic heart failure (SHIFT): a randomised placebo-controlled study. Lancet, 2010, 376, 875-885.
- Komajda, M., Tavazzi, L., Swedberg, K., et al. Chronic exposure to ivabradine reduces readmissions in the vulnerable phase after hospitalization for worsening systolic heart failure: a post-hoc analysis of SHIFT. Eur J Heart Fail, 2016, 18 (9), 1182-1189.
- Rogers, J.K., Kielhorn, A., Borer, J.S., et al. Effect of ivabradine on numbers needed to treat for the prevention of recurrent hospitalizations in heart failure patients. Curr Med Res Opin, 2015, 31 (10), 1903- 1909.
- Böhm, M., Robertson, M., Ford, I., Borer, J.S., Komajda, M., Kindermann, I., et al. Influence of cardiovascular and noncardiovascular co-morbidities on outcomes and treatement effect of heart rate reduction with ivabradine in stable heart failure (from SHIFT Trial). Am J Cardiol, 2015, 116 (12), 1890-1897.
- 2013 ACCF/AHA guideline for the management of heart failure: a report of the American College of Cardiology Foundation/American Heart Association Task Force on practice guidelines. Circulation, 2013, 128 (16), e240-327.
- Cowie, M.R., The Optimize Heart Failure Care Program: Initial lessons from global implementation. Int J Cardiol, 2017, 236, 340-344.
Aucun élément du site web ne peut être reproduit, modifié, diffusé, vendu, publié ou utilisé à des fins commerciales sans autorisation écrite préalable de l’éditeur. Il est également interdit de sauvegarder cette information par voie électronique ou de l’utiliser à des fins illégales.