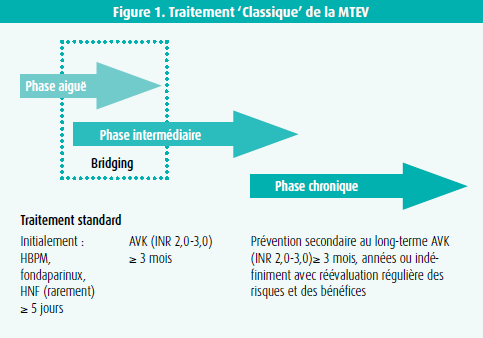
Le but du traitement de la thrombose veineuse profonde (TVP) est d'éviter l'extension du caillot, réduire le risque d'embolie pulmonaire, réduire les symptômes, prévenir le syndrome post-thrombotique et la récidive de la TVP. L'anticoagulation est la pierre angulaire du traitement de la TVP. Pour les patients avec une forte probabilité clinique de TVP, et sans risque hémorragique élevé, le traitement anticoagulant doit être démarré en attendant les investigations complémentaires. Les dernières recommandations d'experts favorisent les anticoagulants oraux directs (AODs) par rapport aux antivitaminiques K (AVK) pour les patients présentant une TVP/EP1. Classiquement, le traitement anticoagulant est poursuivi pendant 3 mois, mais parfois de façon prolongée en cas de risque de récidive élevé (figure 1).
Après une brève revue des anticoagulants disponibles et de leurs propriétés, cet article revoit de façon pratique les principes de prise en charge de la maladie thrombo-embolique veineuse en 2017 en mettant l'accent sur les arguments en faveur d'une anticoagulation prolongée et ses modalités.
Quels sont les anticoagulants disponibles pour traiter la maladie thrombo-embolique veineuse?
Les anticoagulants oraux directs (OADs)
Actuellement, le rivaroxaban2,3, l'apixaban4, 5, l'edoxaban6 et le dabigatran7, 8 sont tous remboursés en Belgique.
Les avantages des AODS sont multiples dans ce contexte9. Ils n'ont pas besoin de monitoring biologique, ne sont pas modifiés par le régime alimentaire et certains d'entre eux (apixaban, rivaroxaban) ne nécessitent pas l'introduction préalable d'héparine en cas de TVP/EP. Du moins, pour ces deux OADs, les études ont démontré qu'ils peuvent être utilisés d'emblée, dès le diagnostic, sans recours préalable à un traitement de quelques jours par HBPM. Ils ont également moins d'interactions que les AVKs, à l'exception d'interactions avec les traitements anti-HIV, antifongiques, immunosuppresseurs. Un des désavantages potentiels est l'absence d'antidote spécifique en cas de complication hémorragique ou de nécessité de réversibilité rapide, sauf pour le dabigatran pour lequel un agent neutralisant existe (idarucizumab) et est disponible11, 12. Le coût des AODS est (actuellement) très supérieur à celui des AVK, mais il est compensé par l'absence de nécessité de monitoring biologique régulier.
Le rivaroxaban et l'apixaban ne nécessitent pas de traitement initial par d'HBPM (figure 2). Pour l'edoxaban et le dabigatran une couverture par HBPM est nécessaire pendant au moins 5 jours avant que le traitement par AOD ne soit instauré en relais de l'HBPM (sans chevauchement toutefois, comme c'est le cas avec les AVKs).

Dans certaines circonstances (doute diagnostic, TVP étendue en phase précoce du traitement, TVP distale très limitée, grossesse, néoplasie, insuffisance rénale …), il semble bienvenu de privilégier un traitement initial par une HBPM avant d'avoir recours (éventuellement) à un AOD.
Les antivitamines K (AVK) principalement utilisés en Belgique sont l'acénocoumarol et la phenprocoumone. Le traitement par AVK nécessite plusieurs jours pour être efficace. Le traitement parentéral par HBPM doit donc être poursuivi au minimum 5 jours, jusqu'à l'obtention d'un INR thérapeutique entre 2 et 3 lors de deux dosages successifs à un intervalle de 24h ou plus. De plus, un traitement concomitant par HBPM est requis au moment d'initier le traitement par AVKs parce que ces derniers induisent au démarrage un état d'hypercoagulabilité (chute rapide de la protéine C).
Le début du traitement, dans la majorité des cas, peut être débuté le jour du diagnostic. Le monitoring de ce traitement nécessite des prises de sang itératives pour contrôler l'INR étant donné qu'un nombre important de facteurs interfèrent avec l'activité des antivitamines K comme l'alimentation et d'autres médicaments.
Fondaparinux et les héparines de bas poids moléculaire (HBPM)
Le fondaparinux et les HBPM (énoxaparine, nadroparine, daltéparine, tinzaparine) constituent les traitements standards de la TVP car ils sont aussi efficaces, plus faciles à utiliser et présentent un risque hémorragique moindre que l'héparine non fractionnée (HNF).
Le fondaparinux est le premier choix, notamment en Suisse et en France. Cette molécule n'est toutefois pas disponible et remboursée en Belgique dans cette indication. Son principal avantage est son origine synthétique, contrairement aux HNF et aux HBPM; il ne nécessite pas de contrôler les plaquettes car il n'induit en principe pas de thrombopénie immuno- allergique. La posologie recommandée est de 7,5 mg/j par voie sous-cutanée (5 mg/j si le poids est < 50 kg et 10 mg/j si le poids est > 100 kg).
Les HBPM constituent le traitement de choix pour les femmes enceintes ou qui allaitent (données insuffisantes pour le fondaparinux).
Lors d'insuffisance rénale avec une clearance à la créatinine <30 ml/min, il s'agit de diminuer les doses et/ou d'augmenter l'intervalle entre les doses, et de suivre l'activité anti-Xa ou alors de passer à une HNF (ce qui en pratique est rarement fait).
Compte tenu des forces et des faiblesses des divers types d'anticoagulants disponibles, un choix doit s'opérer en fonction des circonstances de survenue de la thrombose veineuse, tel que décrit dans le tableau 1.

TVP distales
Le dernier consensus d'experts concernant les TVP distales est de traiter par anticoagulation si présence d'un ou plusieurs facteurs de risque de MTEV ou si le patient présente des symptômes très importants. En l'absence de ces éléments, il est possible de surseoir au traitement tout en répétant un doppler des membres inférieurs dans les 2 semaines. La décision thérapeutique dépendra alors d'une extension proximale du thrombus. En cas d'anticoagulation d'une TVP distale, la durée est habituellement calquée sur celle d'une TVP proximale. Toutefois, pour des TVP distales limitées (veine musculaire, TVP distale monotronculaire), un traitement limité de 40 jours (6 semaines) est probablement suffisant, même si cette approche doit être validée.
Il est important de souligner que les AODs ont été validés parmi des patients présentant une TVP proximale. Dans la pratique, les AODs sont fréquemment prescrits pour des patients avec une TVP distale isolée (expérience personnelle).
Quel anticoagulant privilégier en cas de TVP?
Sur base de ces éléments et des nombreuses études publiées démontrant clairement une non-infériorité antithrombotique et un moindre risque hémorragique des AODs par rapport aux AVKs, il semble légitime de privilégier un traitement par AOD (avec ou sans prétraitement par HBPM) chez tout patient présentant une TVP proximale, en l'absence de contre-indication (grossesse, insuffisance rénale, certains co-traitements, …).
Il semble difficile de privilégier un AOD particulier et/ou de mettre à disposition du corps médical un seul agent, chacun présentant ses propriétés spécifiques (prise 1 à 2 ×/jour, interférences médicamenteuses, effets secondaires, validation spécifique). Les propriétés spécifiques (mode d'action, propriétés pharmacocinétiques, métabolisme, excrétion, effets secondaires, interactions médicamenteuses) de chaque molécule doivent être rigoureusement prises en compte dans la prescription13.
Le tableau 2 résume les modalités pratiques de prise en charge d'une TVP.

Il est important de souligner que les AODs n'ont à ce stade pas été validés pour les patients avec thrombose veineuse cérébrale, thrombose de la veine porte ou thrombose veineuse à d'autres sites inhabituels (même si on peut anticiper une efficacité comparable à celle démontrée dans la MTEV). De même, nous ne disposons pas de données concernant l'efficacité des AODs chez les patients sous AVK avec un INR cible > 2,5.
Durée du traitement anticoagulant
La durée de l'anticoagulation dépend des facteurs de risque sous-jacents et est sujette à controverse. La durée optimale d'anticoagulation dépend avant tout des circonstances de survenue de la TVP/EP (tableau 3) et de la présence de facteurs de risque de récidive qui doivent être identifiés.

à l'exception de certaines TVP distales (ci-dessus), il existe un consensus concernant l'indication formelle et indiscutable de traiter par anticoagulants tout patient présentant une TVP. Décider de la durée optimale d'anticoagulation et identifier les patients chez lesquels une anticoagulation prolongée est indiquée est une tâche complexe et souvent empreinte d'une certaine subjectivité. La décision de maintenir le traitement anticoagulant doit prendre en compte et intégrer de multiples paramètres décrits ci-dessous.
Quel score pour prédire le risque de récidive et identifier les candidats à une anticoagulation prolongée?
Contrairement au score CHA2DS2-VASc largement utilisé pour prédire le risque d'AVC thrombo-embolique (premier épisode ou récidive) chez les patients en FA, il n'existe pas de score unique, largement adopté permettant de prédire rigoureusement le risque de récidive de TVP et d'identifier les patients candidats à une anticoagulation prolongée.
Toutefois plusieurs scores ont été récemment proposés et pour certains validés. Ils devraient permettre d'identifier plus rigoureusement/ aisément les patients candidats à une anticoagulation prolongée (tableau 4).
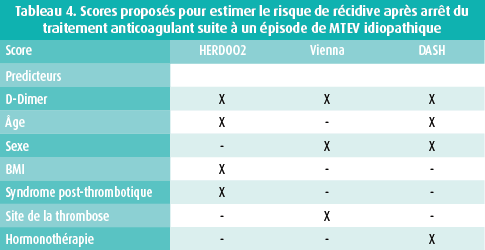
Il s'agit du score de vienne (Dynamic Vienna Prediction Model for Recurrent VTEhttp://www.meduniwien.ac.at/user/ georg.heinze/dvpm/) qui tient compte du sexe, de la localisation du thrombus, de la valeur des D-dimères et du délai écoulé entre la mesure des DD et l'interruption du traitement anticoagulant. Il s'agit par ailleurs du score DASH (D-dimer, Age, Sex, Hormonal therapy) récemment validé14, 15 ainsi que du score HERDOO2 (Hyperpigmentation, Edema, or Redness in either leg; D-dimer level ≥ 250 μg/L; Obesity with body mass index ≥ 30; or Older age, ≥ 65 years) également validé16, 17.
Une revue systématique récente a mis en lumière les limites de ces scores, l'absence de validation suffisante et l'impossibilité de les implémenter actuellement en routine clinique18.
Les paramètres à prendre en compte pour identifier les patients candidats à une anticoagulation prolongée sont détaillés dans le tableau 5.

Difficultés de définir la durée optimale d'anticoagulation chez certains patients
Sur base de la littérature actuelle, certaines conditions justifient formellement une anticoagulation courte ou prolongée. Il existe toutefois plusieurs situations cliniques pour lesquelles la décision d'avoir recours à une anticoagulation prolongée est très débattue.
à titre d'exemple, lors d'une TVP proximale idiopathique, la durée du traitement anticoagulant est à adapter en fonction du risque de saignement et des préférences du patient. Les arguments plaidant pour une anticoagulation au long cours sont: sexe masculin, syndrome post-thrombotique (SPT) modéré à sévère, bon contrôle de l'anticoagulation, D-dimères élevés à la fin du traitement.
Quelle que soit la décision prise, toutes les indications à l'anticoagulation à long terme doivent être revues chaque année pour réévaluer la balance risque-bénéfice de ce traitement (risques hémorragiques versus bénéfices antithrombotiques) et le choix de la molécule19. Il s'agit d'une démarche difficile, nécessitant une réelle expertise clinique et qui n'est pas dénuée d'éventuelles implications médico-légales.
Il est important que les arguments/ éléments justifiant une anticoagulation prolongée (ou la non prolongation) soient clairement explicités dans le dossier, communiqués au médecin traitant et expliqués au patient.
Faut-il démontrer la résolution du thrombus en fin de traitement et poursuivre en cas de persistance?
Il n'est pas clairement démontré que la durée du traitement doive être influencée par la persistance de thrombi résiduels. Toutefois, si après une durée de traitement de 3 mois, il s'avère qu'il persiste un thrombus résiduel significatif surtout si toujours occlusif au niveau des veines des membres inférieurs, il semble légitime de poursuivre le traitement anticoagulant afin d'augmenter les chances de résolution (durée difficile à préciser d'autant plus que chez certains patients une résolution complète ne sera jamais obtenue).
Quel agent anticoagulant pour une anticoagulation prolongée?
Les options de traitement antithrombotique au long cours sont le maintien du traitement par AVK (éventuellement à dose réduite en visant un INR entre 1,5 et 2), le remplacement de l'AVK par une faible dose d'aspirine, la poursuite par un AOD, éventuellement à dose réduite.
Plusieurs études ont évalué une anticoagulation prolongée par AVK en visant un INR réduit entre 1,5-2, soit par rapport au placébo (étude PREVENT)20,soit par rapport au traitement classique (étude ELATE - INR cible 2-3)21. Ces études démontrent qu'une réduction de l'INR cible (1,5-2) n'est pas l'option thérapeutique de choix en cas d'anticoagulation prolongée par AVK.
Même si les données issues de la chirurgie orthopédique lourde et d'études récentes en prévention secondaire démontrent un effet préventif de l'aspirine sur la maladie thrombo-embolique veineuse, les bénéfices antithrombotiques sont largement inférieurs à ceux observés avec les anticoagulants (HBPMs, AVKs, nouveaux anticoagulants oraux)22, 23. Sur base de ces données, l'aspirine ne peut certainement pas se substituer aux anticoagulants. Elle peut toutefois apporter une certaine protection chez les patients à risque de thrombose veineuse et chez lesquels les anticoagulants sont contre-indiqués, tout en étant bien conscient que le degré de protection est bien moindre.
Plusieurs études récentes (extension trials) ont évalué les bénéfices des AODs (généralement comparativement à un placébo et/ou à doses réduites d'ADO) utilisés de façon prolongée après un traitement de 6-12 mois d'un accident thrombotique veineux initial. Les quatre AODs réduisent significativement le risque de récidive d'accident thrombotique sans induire de saignements en excès. Il est évident que ces données ouvrent de nouvelles perspectives et permettent d'envisager de proposer une anticoagulation prolongée à un plus grand nombre de patients.
Se pose la question de la sécurité d'avoir recours à une réduite d'AOD (rivaroxaban à raison de 10 mg/jour et apixaban à raison de 2,5 mg 2 ×/J) au long cours chez tous les patients. Certaines études d'extension ont en effet inclus des patients à faible risque de récidive. On peut s'interroger à propos de la posologie optimale en prévention secondaire prolongée en cas de thrombophilie sévère, multiple, d'antécédents thrombo-emboliques majeurs (EP massive, TVP très étendue) ou accompagnés de séquelles significatives (thrombus résiduel étendu, hypertension artérielle pulmonaire résiduelle ...).
Il est important de tenter de définir individuellement la posologie appropriée pour un traitement d'extension prolongé, en veillant à ne pas surdoser des patients à faible risque de récidive et sous-doser des patients à risque élevé.
Traitement anticoagulant prolongé et compliance
En termes de compliance et d'adhérence, il est important de souligner qu'elle est généralement meilleure parmi les patients anticoagulés compte tenu de leurs antécédents thrombo-emboliques veineux par rapport aux patients en fibrillation auriculaire (FA). De nombreux patients en FA sont anticoagulés préventivement (prévention primaire), alors que les patients anticoagulés compte tenu de leurs antécédents thrombotiques veineux ont tous un jour expérimenté une TVP et/ou une EP, ce qui a un impact sur leur adhérence (expérience personnelle).
Conclusions
Les AODS modifient fondamentalement la prise en charge de la MTEV (initiation, anticoagulation prolongée, réduction des risques hémorragiques, facilité d'utilisation). Certaines précautions doivent toutefois être respectées. De nombreux patients doivent être anticoagulés au long cours. L'identification des patients éligibles pour une anticoagulation prolongée demeure difficile. Il reste une place certaine mais limitée pour les AVKs et HBPMs. Les critères actuels de remboursement des AODs en Belgique doivent être adaptés afin de permettre au plus grand nombre de patients avec antécédents de MTEV d'être traités par les AODs.
Références
- Kearon, C., Akl, E.A., Ornelas, J., Blaivas, A., Jimenez, D., Bounameaux, H. et al. Antithrombotic Therapy for VTE Disease: CHEST Guideline and Expert Panel Report. Chest, 2016, 149 (2), 315-352.
- Bauersachs, R., Berkowitz, S.D., Brenner, B., Buller, H.R., Decousus, H., Gallus, A.S. et al. Oral rivaroxaban for symptomatic venous thromboembolism. N Engl J Med, 2010, 363 (26), 2499-2510.
- Buller, H.R., Prins, M.H., Lensin, A.W., Decousus, H., Jacobson, B.F., Minar, E. et al. Oral rivaroxaban for the treatment of symptomatic pulmonary embolism. N Engl J Med, 2012, 366 (14), 1287-1297.
- Agnelli, G., Buller, H.R., Cohen, A., Curto, M., Gallus, A.S., Johnson, M. et al. Oral apixaban for the treatment of acute venous thromboembolism. N Engl J Med, 2013, 369 (9), 799-808.
- Agnelli, G., Buller, H.R., Cohen, A., Curto, M., Gallus, A.S., Johnson, M. et al. Apixaban for extended treatment of venous thromboembolism. N Engl J Med, 2013, 368 (8), 699-708.
- Buller, H.R., Decousus, H., Grosso, M.A., Mercuri, M., Middeldorp, S., Prins, M.H. et al. Edoxaban versus warfarin for the treatment of symptomatic venous thromboembolism. N Engl J Med, 2013, 369 (15), 1406-1415.
- Schulman, S., Kearon, C., Kakkar, A.K., Mismetti, P., Schellong, S., Eriksson, H. et al. Dabigatran versus warfarin in the treatment of acute venous thromboembolism. N Engl J Med, 2009, 361 (24), 2342-2352.
- Schulman, S., Kearon, C., Kakkar, A.K., Schellong, S., Eriksson, H., Baanstra, D. et al. Extended use of dabigatran, warfarin, or placebo in venous thromboembolism. N Engl J Med, 2013, 368 (8), 709-718.
- Thachil, J. The newer direct oral anticoagulants: a practical guide. Clin Med (Lond), 2014, 14 (2), 165-175.
- van Es, N., Coppens, M., Schulman, S., Middeldorp, S., Buller, H.R. Direct oral anticoagulants compared with vitamin K antagonists for acute venous thromboembolism: evidence from phase 3 trials. Blood, 2014, 124 (12), 1968-1975.
- Pollack, C.V., Jr., Reilly, P.A., Weitz, J.I. Dabigatran Reversal with Idarucizumab. N Engl J Med, 2017, 377 (17), 1691-1692.
- Pollack, C.V., Jr., Reilly, P.A., Eikelboom, J., Glund, S., Verhamme, P., Bernstein, R.A. et al. Idarucizumab for Dabigatran Reversal. N Engl J Med, 2015, 373 (6), 511-520.
- Millar, C.M., Laffan, M.A. Drug therapy in anticoagulation: which drug for which patient? Clin Med (Lond), 2017, 17 (3), 233-244.
- Tosetto, A., Testa, S., Martinelli, I., Poli, D., Cosmi, B., Lodigiani, C. et al. External validation of the DASH prediction rule: a retrospective cohort study. J Thromb Haemost, 2017, 15 (10), 1963-1970.
- Tosetto, A., Iorio, A., Marcucci, M., Baglin, T., Cushman, M., Eichinger, S. et al. Predicting disease recurrence in patients with previous unprovoked venous thromboembolism: a proposed prediction score (DASH). J Thromb Haemost, 2012, 10 (6), 1019-1025.
- Kruger, P., Eikelboom, J. HERDOO2 identified women at low risk for recurrence after 5 to 12 mo of anticoagulation for a first unprovoked VTE. Ann Intern Med, 2017, 167 (6), JC33.
- Rodger, M.A., Le Gal, G., Anderson, D.R., Schmidt, J., Pernod, G., Kahn, S.R. et al. Validating the HERDOO2 rule to guide treatment duration for women with unprovoked venous thrombosis: multinational prospective cohort management study. Brit Med J, 2017, 356, j1065.
- Ensor, J., Riley, R.D., Moore, D., Snell, K.I., Bayliss, S., Fitzmaurice, D. Systematic review of prognostic models for recurrent venous thromboembolism (VTE) post-treatment of first unprovoked VTE. Brit Med J Open, 2016, 6 (5): e011190.
- Kearon, C., Akl, E.A. Duration of anticoagulant therapy for deep vein thrombosis and pulmonary embolism. Blood, 2014, 123 (12), 1794- 1801.
- Ridker, P.M., Goldhaber, S.Z., Glynn, R.J. Low-intensity versus conventional-intensity warfarin for prevention of recurrent venous thromboembolism. N Engl J Med, 2003, 349 (22), 2164-2167.
- Kearon, C., Ginsberg, J.S., Kovacs, M.J., Anderson, D.R., Wells, P., Julian, J.A. et al. Comparison of low-intensity warfarin therapy with conventional-intensity warfarin therapy for long-term prevention of recurrent venous thromboembolism. N Engl J Med, 2003, 349 (7), 631-639.
- Becattini, C., Agnelli, G., Schenone, A., Eichinger, S., Bucherini, E., Silingardi, M. et al. Aspirin for preventing the recurrence of venous thromboembolism. N Engl J Med, 2012, 366 (21), 1959-1967.
- Brighton, T.A., Eikelboom, J.W., Mann, K., Mister, R., Gallus, A., Ockelford, P. et al. Low-dose aspirin for preventing recurrent venous thromboembolism. N Engl J Med, 2012, 367 (21), 1979-1987.
- van Es, J., Douma, R.A., Kamphuisen, P.W., Gerdes, V.E., Verhamme, P., Wells, P.S. et al. Clot resolution after 3 weeks of anticoagulant treatment for pulmonary embolism: comparison of computed tomography and perfusion scintigraphy. J Thromb Haemost, 2013, 11 (4), 679-685.
Aucun élément du site web ne peut être reproduit, modifié, diffusé, vendu, publié ou utilisé à des fins commerciales sans autorisation écrite préalable de l’éditeur. Il est également interdit de sauvegarder cette information par voie électronique ou de l’utiliser à des fins illégales.