Introduction
Cela fait déjà 10 ans que le premier défibrillateur sous-cutané a été implanté, une première révolutionnaire. Depuis, ce modèle de défibrillateur a parcouru beaucoup de chemin et progressé tant sur le plan technologique que clinique; il fait actuellement partie intégrante de l'arsenal thérapeutique disponible dans la prévention de la mort subite.
Pour rappel, depuis plus de 20 ans, le défibrillateur automatique implantable est devenu incontournable dans la prévention de la mort subite, à titre secondaire d'abord, puis primaire. Son format standard comprend un boitier préou sous-pectoral avec une ou plusieurs sondes endo-cavitaires. En dépit de son efficacité dans le traitement d'arythmies malignes, l'implantation de ce type de dispositif (TV-ICD) comporte des risques telles que l'infection souvent systémique nécessitant alors l'extraction du matériel (chirurgie lourde), la fracture de sonde, la thrombose veineuse, la perforation myocardique … tous liés à son caractère trans-veineux. Le taux de complications varie selon les séries mais s'élève parfois à plus de 20 % pour des procédures complexes notamment de repositionnement de matériel1.
C'est à ce titre qu'a été développé le défibrillateur sous-cutané (S-ICD), entièrement extravasculaire : un boitier, placé en position latéro-thoracique gauche, et une sonde, sans lumière donc très solide, placée en sous-cutané, le long du bord gauche du sternum, en général.2 Ce défibrillateur 'extra-thoracique' a donc été créé pour éviter les complications précitées. Son efficacité ainsi que sa sécurité ont été confirmées dans les études IDE et EFFORTLESS.3, 4 Il persiste tout de même quelques limitations, principalement l'absence de fonction pacemaker (ni traitement de bradycardie sauf post-choc, ni traitement ATP), un fonctionnement donc type 'boite à chocs', des mémoires Holter peu développées, un volume majoré, et la nécessité d'un screening pré-implantation puisque certaines morphologies de QRS et de repolarisation ne sont pas compatibles.
Après dix ans d'existence, quelles sont les nouveautés en termes de technique d'implantation et d'anesthésie, quels sont les chiffres en termes de nombres d'implantation, de types d'indications et que disent les recommandations? Ces questions seront adressées dans cette édition. Les progrès technologiques ont été adressés dans une édition antérieure par le Dr L. Timmers.
Chiffres et indications
Jusqu'à présent, en Belgique, un total de plus de 500 patients ont déjà bénéficié de l'implantation d'un défibrillateur sous-cutané dont 164 implantations en 2017 ; le premier avait été implanté en 2010 chez une jeune patiente atteinte d'un syndrome de QT long chez qui l'accès veineux était devenu très limité suite à la présence de plusieurs sondes avec fractures, encombrant son système veineux … Le remboursement belge date de 2014. à l'échelle mondiale, plus de 50 000 patients sont porteurs d'un défibrillateur sous-cutané.
En tant que nouvelle technologie et au vu de ses particularités citées plus haut, le défibrillateur sous-cutané a d'abord été considéré comme un traitement de 'niche' pour des patients très fragiles avec risque infectieux majeur ou sans abord veineux. Progressivement, le profil du patient type s'est élargi vers une population plus jeune, et puis à la prévention primaire de cardiomyopathie ischémique notamment grâce aux données récentes évoquant le bénéfice lié à la prolongation des délais de détection et de thérapie des tachycardies ventriculaires.5
Un registre prospectif américain initié après l'approbation FDA du S-ICD dévoile les données de l'expérience 'real-life' sur 1 687 patients.6 Le défibrillateur sous-cutané était la seule option possible pour 8,8 % des patients. Sinon, le S-ICD a été choisi selon différents critères : choix du patient (52,4 %), jeune âge (43,7 %), profil d'activité du patient (12,5 %), ou infection/dysfonction d'un TV-ICD préalable (9,2 %).
Au vu du l'expérience croissante, les recommandations européennes de l'ESC ont inclus dès 2015 le défibrillateur avec une classe de recommandation IIaC.7 Ces recommandations excluent le patient nécessitant de la stimulation qu'elle soit pour des problèmes de bradycardie, à but resynchronisant ou pour un traitement type ATP. La pathologie sous-jacente, et l'indication de prévention secondaire ou primaire ne sont pas adressées.
Le défibrillateur sous-cutané était déjà repris comme option thérapeutique (classe IIbC) dans les recommandations de 2014 sur la cardiomyopathie hypertrophique. D'ailleurs en 2017, aux Etats-Unis, pour certaines indications (haut risque infectieux ou accès veineux inadéquat), la recommandation est passée en classe I.8
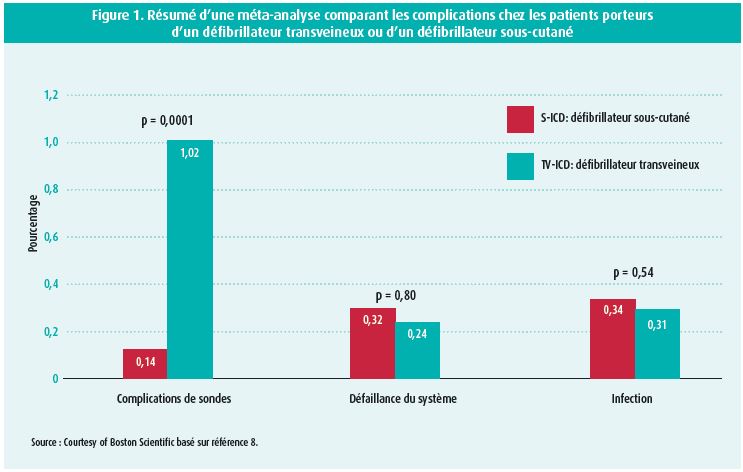
Une méta-analyse récente comparant directement S-ICD et TV-ICD chez plus de 6 400 patients issus de 5 études (4 rétrospective, une prospective) a été publiée avec des résultats en faveur du modèle sous-cutané en termes de complications liées à la sonde.9 Le nombre de complications non-liées à la sonde dont chocs inappropriés et le nombre d'infections étaient comparables (figure 1). Notons qu'après l'infection d'un dispositif trans-veineux, le défibrillateur sous-cutané a toute sa place. Dans une cohorte de 229 patients infectés avec un défibrillateur trans-veineux, le choix se portant sur un défibrillateur sous-cutané lors du remplacement est passé de 9 % en 2011 à 85 % en 2017.10
L'étude PRAETORIAN est une étude multicentrique, randomisée, prospective, qui compare le S-ICD et le TV-ICD chez 700 patients avec une indication classe I ou IIa pour un défibrillateur implantable (sans indication de stimulation).11 L'endpoint primaire composite comprend les chocs inappropriés et des complications liés au défibrillateur. L'endpoint secondaire concerne l'efficacité des chocs et la mortalité. L'inclusion est terminée, mais les résultats sont attendus pour 2020.
Techniques d'implantation
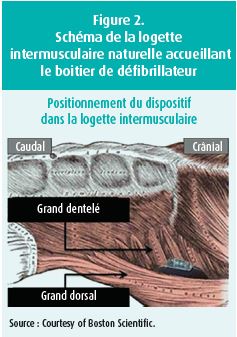
Initialement totalement sous-cutané, le boitier du S-ICD est devenu intermusculaire s'implantant dans l'espace naturel entre le Grand dentelé/Serratus anterior et le Grand dorsal/Latissimus dorsi, pour assurer plus de confort au patient, moins de risque d'érosion mais aussi pour rapprocher le boitier de la cage thoracique et donc augmenter son efficacité de choc (figure 2).
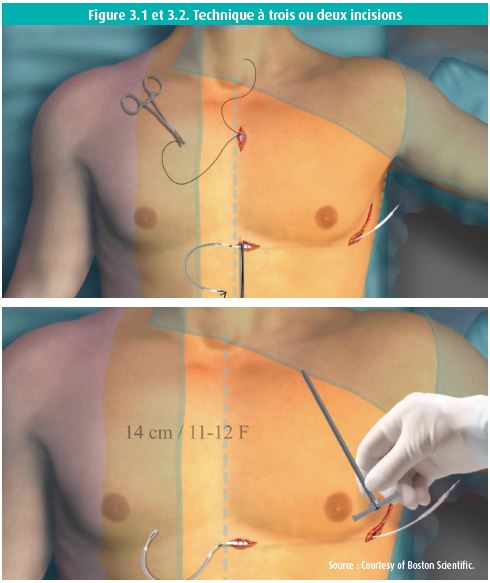
Pour implanter et fixer l'ensemble du dispositif, boitier et sonde, la technique d'implantation initiale nécessitait trois incisions. Pour des raisons cosmétiques, une technique à deux incisions a été développée.12 L'incision en regard de l'extrémité distale de la sonde au niveau de la partie supérieure du sternum en regard de l'extrémité distale de la sonde n'est plus nécessaire. Cette technique diminue aussi le temps d'implantation, le nombre de plaies et donc le nombre de sources potentielles d'infection (figure 3.1 et 3.2). Dans la grande majorité des cas, le défibrillateur sous-cutané est implanté sous anesthésie générale. Cela assure l'antalgie pendant la procédure (le déplacement des muscles étant souvent très douloureux pour le patient), et une importante facilité pour le test de défibrillation, encore recommandé à l'heure actuelle pour ce type de défibrillateur.13 Pour se passer d'anesthésie générale chez certains patients à risque, certains groupes utilisent la technique du 'bloc serratus', déjà décrite et proposée pour des chirurgies mammaires.14, 15 Cette technique nécessite un repérage échographique du plan aponévrotique au niveau de la zone d'implantation (entre les grands dorsal et dentelé) puis infiltration de cette zone intermusculaire d'abord de sérum physiologique pour décoller les deux plans puis d'anesthésiant. Cette anesthésie cible les nerfs de la zone thoracique antérolatérale, essentiellement le nerf thoracique long. La chirurgie d'implantation peut alors avoir lieu moyennant en général une légère sédation supplémentaire. La faisabilité et la sécurité de cette technique étant confirmées, elle séduit plusieurs groupes d'autant plus qu'elle assure une antalgie qui dépasse en durée celle de l'intervention, avantage net pour le confort du patient en post-opératoire.
Le positionnement du boitier a également évolué, il est maintenant placé plus postérieurement. Le seuil de défibrillation est en effet meilleur quand le boitier est postérieur par rapport à la ligne médio-axillaire car le boitier et la sonde 'englobent' de façon plus appropriée la masse myocardique (figure 4).
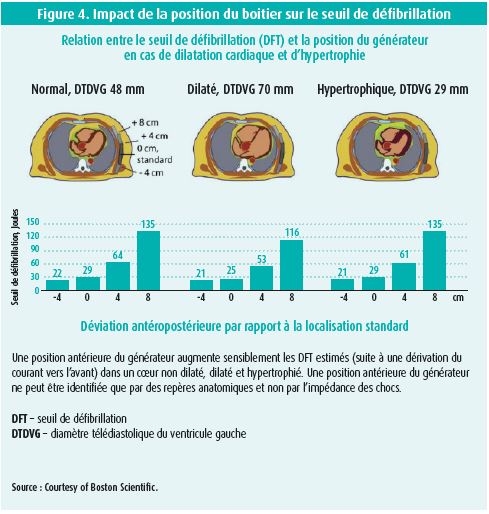
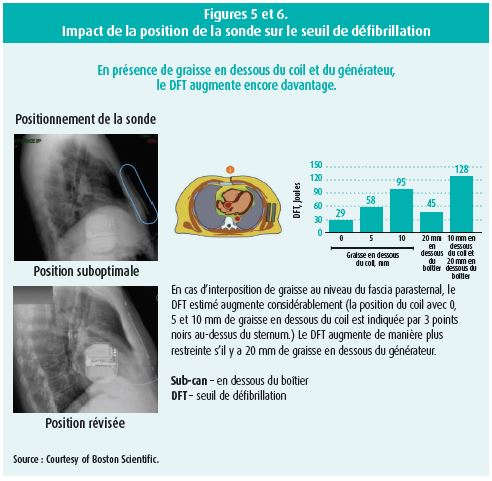
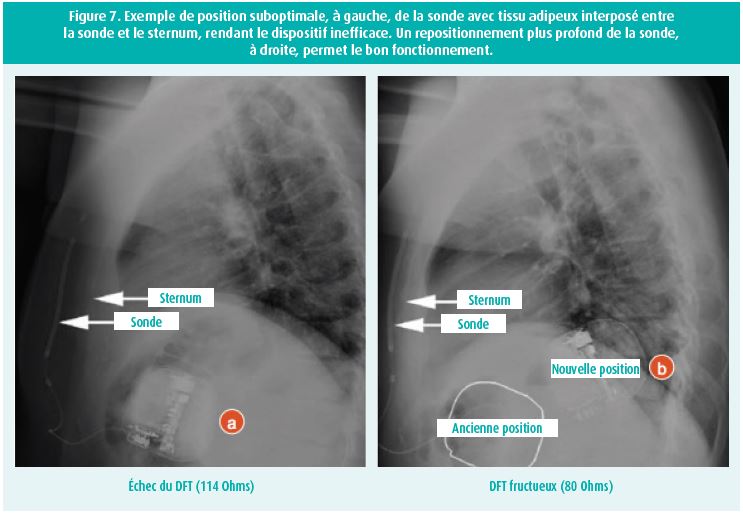
D'ailleurs, toujours pour assurer le meilleur seuil de défibrillation possible, il est conseillé d'atteindre une position de sonde parasternale la plus profonde possible, c'est à dire le plus proche possible du sternum (sans tissu adipeux interposé). Cette astuce est particulièrement intéressant chez les patients à BMI élevés (figure 4, 5 et 6).
Conclusion
En bref, le défibrillateur sous-cutané a mérité sa place dans l'arsenal thérapeutique actuel pour lutter contre la mort subite, comme démontré par différentes études et registres regroupant un grand nombre de patients. Efficace et sûr, il peut être considéré pour tout patient devant bénéficier d'une protection simple chambre que ce soit en prévention primaire ou secondaire de mort subite. Le futur nous réserve encore d'intéressantes perspectives dont l'interaction entre le S-ICD et un pacemaker sans sonde proposant une stimulation pour bradycardie ou même des ATP, à suivre donc … 16
Références
- Kirkfeldt, R.E., Johansen, J.B., Nohr, E.A., Jorgnesen, O.D., Nielsen, J.C. Complications after cardiac implantable electronic device implantations: an analysis of a complete, nationwide cohort in Denmark. Eur Heart J, 2014, 35 (18), 1186-1194.
- Bardy, G., Smith, W., Hood, M., Crozier, I., Melton, I., Jordaens, L., et al. An Entirely Subcutaneous Implantable Cardioverter-Defibrillator. N Engl J Med, 2010, 363, 36-44.
- Weiss, R., Knight, B., Gold, M., Leon, A., Herre, J., Hood, M., Rashtian, M., et al. Safety and Efficacy of a Totally Subcutaneous Implantable-Cardioverter Defibrillator. Circulation, 2013, 128, 944-953.
- Lambiase, P., Barr, C., Theuns, D.A.M.J., Knops, R., Neuzil, P., Johansen, J.B., et al. Worldwide experience with a totally subcutaneous implantable defibrillator: early results from the EFFORTLESS S-ICD Registry . Eur Heart J, 2014, 35 (25), 1657-1665.
- Moss, A.J., Schuger, C., Beck, C.A., Brown, M.W., Cannom, D.S., Daubert, J.P., et al. Reduction in inappropriate therapy and mortality through ICD programming. N Engl J Med, 2012, 367, 2275-2283.
- Gold, M.R., Aasbo, J.D., El-Chami, M.F., Niebauer, M., Herre, J., Prutkin, J.M., et al. The Subcutaneous ICD Post-Market Approval Study: Clinical Characteristic and Perioperative Results. Heart Rhythm, 2017, 14 (10), 1456-1463.
- Priori, S., Blomström-Lundqvist, C., Mazzanti, A., Blom, N., Borggefe, M., Camm, J., et al. 2015 ESC guidelines for management of patients with ventricular arrhythmias and the prevention of sudden cardiac death. Eur Heart J, 2015, 36, 2793-2867.
- Al-Khatib, S., Stevenson, W., Ackerman, M., Bryant, W., Callans, D., Curtis, A., et al. 2017 AHA/ACC/HRS Guideline for Patients With Ventricular Arrhythmias and the Prevention of Sudden Cardiac Death: Executive Summary. Heart Rhythm, 2018, 15 (10), e190-e252.
- Basu-Ray, I., Liu, J., Jia, X., Gold, M., Ellenbogen, M., Ellenbogen, K., et al. Subcutaneous Versus Transvenous Implantable Defibrillator Therapy: A Meta-Analysis of Case-Control Studies. JACC Clin Electrophysiol, 2017, 3 (13), 1475-1483.
- Viani, S., Migliore, F., Tola, G., Pisanò, E.C.L., Russo, A.D., Luzzi, G., et al. Use and outcomes of subcutaneous implantable cardioverter-defibrillator (ICD) after transvenous ICD extraction: An analysis of current clinical practice and a comparison with transvenous ICD reimplantation. Heart Rhythm, 2018, S1547- 5271(18)34053-1 [Epub ahead of print].
- Olde Nordkamp, L.R., Knops, R.E., Bardy, G.H., Blaauw, Y., Boersma, L.V., Bos, J.S., et al. Rationale and design of the PRAETORIAN trial: a Prospective, RAndomizEd comparison of subcuTaneOus and tRansvenous ImplANtable cardioverter-defibrillator therapy. Am Heart J, 2012, 163 (5), 753-760.
- Knops, R.E., Olde Nordkamp, L.R., de Groot, J.R., Wilde, A.A. Two-incision technique for implantation of the subcutaneous implantable cardioverter-defibrillator. Heart Rhythm, 2013, 10 (8), 1240-1243.
- le Polain de Waroux, J.B., Ploux, S., Mondoly, P., Eschalier, R., Strik, M., Houard, L., et al. Defibrillation testing is mandatory in patients with subcutaneous implantable cardioverter- defibrillator to confirm appropriate ventricular fibrillation detection. Heart Rhythm, 2018, 15 (5), 642-650.
- Blanco, R., Parras, T., McDonnell, J.G., Prats-Galino, A. Original Article Serratus plane block: a novel ultrasound-guided thoracic wall nerve block. Anaesthesia, 2013, 68, 1107-1113.
- Droghetti, A., Basso, Ricci, E., Scimia, P., Harizai, F., Marini, M. Ultrasound-guided serratus anterior plane block combined with the two-incision technique for subcutaneous ICD implantation. Pacing Clin Electrophysiol, 2018, 41 (5), 517-523.
- Tjong, F.V.Y., Brouwer, T.F., Koop, B., Soltis, B., Shuros, A., Schmidt, B., et al. Acute and 3-Month Performance of a Communicating Leadless Antitachycardia Pacemaker and Subcutaneous Implantable Defibrillator. JACC Clin Electrophysiol, 2017, 3 (13), 1487-1498.
Aucun élément du site web ne peut être reproduit, modifié, diffusé, vendu, publié ou utilisé à des fins commerciales sans autorisation écrite préalable de l’éditeur. Il est également interdit de sauvegarder cette information par voie électronique ou de l’utiliser à des fins illégales.