Compte rendu du symposium BHRM
Introduction
Divers sujets ont été abordés lors du récent Belgian Heart Rhythm Meeting. Notamment une session dédiée aux avantages et inconvénients de la stimulation du faisceau de His et de la branche gauche. Il a également été examiné si ces méthodes peuvent, à terme, offrir une alternative à la stimulation biventriculaire dans le cadre d'une thérapie de resynchronisation cardiaque. Cet article se destine dès lors à résumer cette présentation. Les intervenants étaient le Dr Elise Bakelants et le Pr Christophe Leclercq.
Pourquoi la stimulation du faisceau de His et la stimulation de la branche gauche peuvent effectivement offrir une alternative à la stimulation biventriculaire
Dr. E. Bakelants
Chez les patients avec insuffisance cardiaque et dyssynchronie, la thérapie de resynchronisation cardiaque (TRC) par stimulation (pacing) biventriculaire entraîne une amélioration des symptômes, de la morbidité et de la mortalité. Cela a été démontré, entre autres, dans l'étude CARE-HF et dans l'étude MADIT-CRT.1, 2 Une analyse de sous-groupes de ces études montre que ce sont principalement les patients avec un bloc de branche gauche (BBG) qui connaissent des résultats favorables, tandis que les patients avec un bloc de branche droit (BBD) ou des troubles de la conduction intraventriculaire ne bénéficient pas de cet avantage.3 Chez les patients avec insuffisance cardiaque caractérisée par une dyssynchronie cardiaque et un complexe QRS étroit, la stimulation biventriculaire (SBV) conduit même à une mortalité accrue.4 Sans oublier que la SBV a également divers inconvénients. Premièrement, la méthode de stimulation cardiaque n'est pas physiologique. En effet, la stimulation se fait de l'épicarde vers l'endocarde et repose sur une lente conduction de cellule à cellule. Deuxièmement, il existe des limites anatomiques qui empêchent l'implantation d'une électrode ventriculaire gauche. Suite à ces deux éléments, il n'est pas possible d'atteindre une resynchronisation chez un grand groupe de patients (les chiffres varient autour des 30-40 %). Ces restrictions ont conduit au développement de formes plus physiologiques de stimulation, dont la stimulation du faisceau de His (SFH).
La SFH offre en outre la possibilité de corriger un bloc de branche préexistant. Cela s'explique par deux principes. D'une part: la théorie de la dissociation longitudinale, selon laquelle les fibres conductrices du faisceau de His sont déjà prédisposées pour le bloc de branche dans lequel elles auront une position plus distale. D'autre part: la théorie de la dépendance du stimulus, où l'on voit que la correction d'un bloc dépend de la puissance du stimulus électrique délivré. Il est ainsi possible de corriger un bloc de deux façons. Premièrement, on peut stimuler le bloc de manière plus distale ; deuxièmement, on peut continuer à stimuler en proximal, mais en délivrant un voltage supérieur (figure 1).
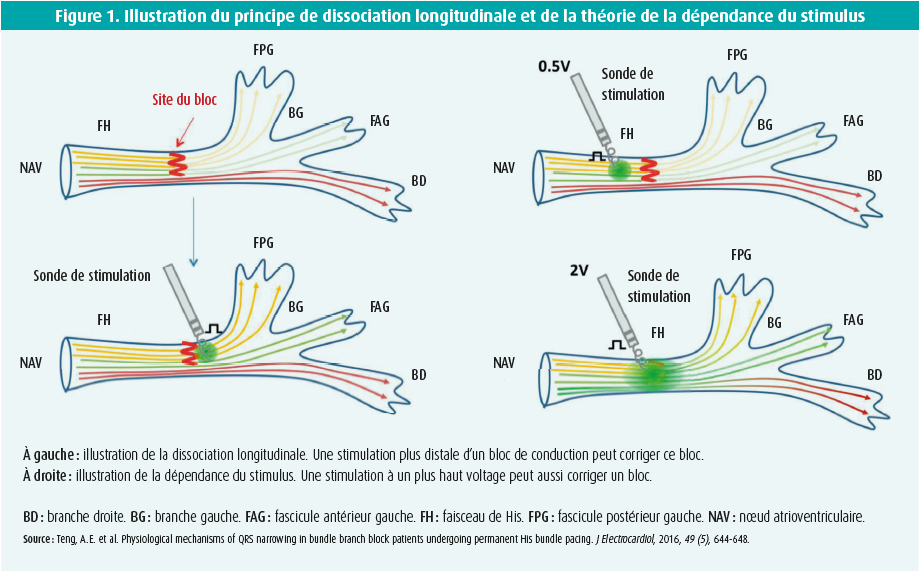
Le potentiel de la SFH a été démontré, entre autres, dans une étude menée par Arnold en 2018.5 Dans cette étude, une SFH temporaire était effectuée pendant la pose d'un système de SBV et les paramètres hémodynamiques et mécaniques étaient comparés entre les deux méthodes. Les investigateurs y ont observé, entre autres, une plus grande réduction de la durée du QRS (-18,6 ms ; IC à 95 %: -31,6 à -5,7 ms ; P = 0,007), une plus grande diminution de l'indice de dyssynchronie (-11,2 ms ; IC à 95 %: -16,8 à -5,6 ms ; P < 0,001) et une plus grande hausse de la pression artérielle systolique (4,6 mmHg ; IC à 95 %: 0,2 à 9,1 mmHg ; P = 0,04).5 Par ailleurs, diverses études de cohorte, publiées ces dernières années, soulignent l'avantage de la SFH.6-11 Initialement, la SFH était utilisée dans ces études en solution de rechange, lorsque la pose d'un système de SBV s'avérait impossible. Mais, par la suite, d'autres études sont parues, utilisant la SFH en thérapie de première intention. Une autre étude importante à cet égard est l'étude menée par Sharma en 2018.10 Dans cette étude, un groupe hétérogène de 106 patients ayant une indication de TRC a été divisé en deux sous-groupes. Dans un sous-groupe, la SFH était utilisée lorsque la pose d'un système de SBV s'avérait impossible. Dans l'autre sous-groupe, la SFH était appliquée en thérapie de premier choix. Un système de SBV a été implanté avec succès chez 95 des 106 patients (taux de réussite de 90 %). Après un suivi médian de 14 mois, les deux sous-groupes présentaient une réduction significative de la durée du QRS (de 157 ± 33 ms à 117 ± 18 ms ; P = 0,0001), une augmentation de la fraction d'éjection ventriculaire gauche (de 30 % ± 10 % à 43 % ± 13 % ; P = 0,0001) et une amélioration de la classe NYHA (de 2,8 ± 0,5 à 1,8 ± 0,6 ; P = 0,0001).10
Étant donné que les patients BBD réagissent moins favorablement à la SBV, une étude a également été publiée en vue d'évaluer l'effet de la SFH dans cette population.12 Dans cette étude, un système de SFH a été implanté avec succès chez 37 des 39 patients (taux de réussite de 95 %). Après un suivi médian de 15 mois, les investigateurs ont également observé une réduction significative de la durée du QRS, de même qu'une augmentation de la fraction d'éjection ventriculaire gauche et une diminution de la classe NYHA.12
La première (et à ce jour unique) étude randomisée s'est toutefois fait attendre jusqu'à la fin de l'année dernière avec la publication de l'étude His-SYNC.13 Dans celle-ci, 41 patients ont été randomisés vers une thérapie de première intention par SBV (n = 20) ou par SFH (n = 21). Le taux élevé de permutation entre les deux groupes est important. Ainsi, 48 % des patients du groupe SFH sont passés dans le groupe SBV, car la durée du complexe QRS n'était pas réduite aux valeurs prédéfinies. À l'inverse, 26 % des patients du groupe SBV ont également dû passer dans le groupe SFH en raison de difficultés lors de la pose de l'électrode ventriculaire gauche. Après un suivi médian de 6 mois, une réduction significative de la durée du QRS était certes observée dans le groupe SFH (de 172 ms ± 16 ms à 144 ms ± 30 ms ; P = 0,002). Mais la différence de durée du QRS entre les deux groupes n'était pas significative (P = 0,42). De même, l'augmentation de la fraction d'éjection ventriculaire gauche n'était pas significativement différente entre les deux groupes, malgré une augmentation plus importante dans le groupe SFH (médiane resp. + 9,1 % (Q1-Q3: 5,0 % -14,4 %) vs + 5,2 % (Q1-Q3: 1,5 % - 11,3 %) ; P = 0,33) (figure 2).13 Au vu du haut taux de permutation entre les deux groupes, cette étude montre essentiellement que les indications doivent être choisies avec soin. En effet, cette étude a inclus des patients atteints de troubles de la conduction intraventriculaire non spécifiques, qui ne peuvent pas être corrigés par SFH.
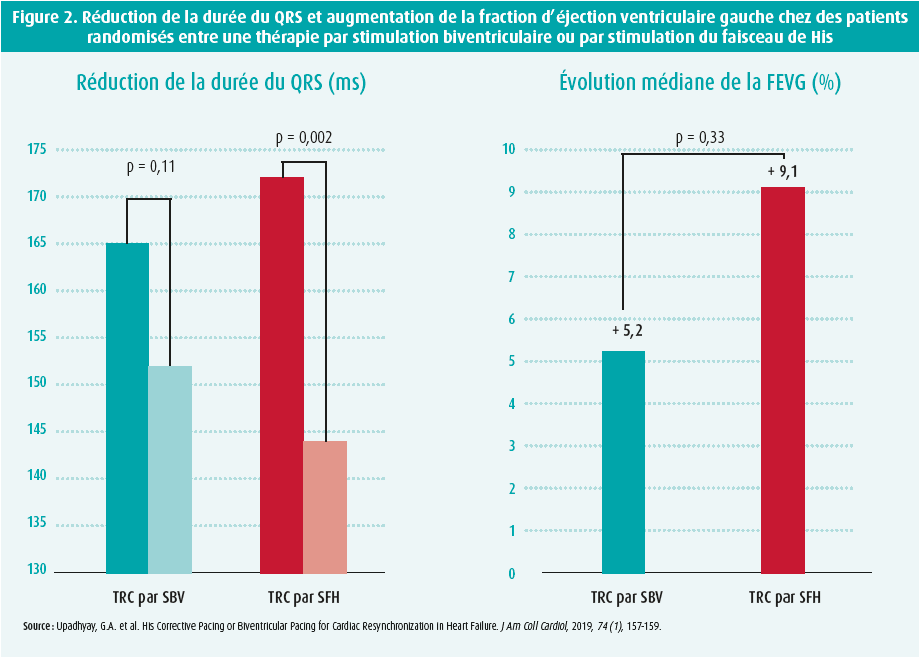
L'utilisation croissante de la SFH a également suscité des inquiétudes en ce qui concerne la stabilité des seuils, l'amplitude de l'onde R et une possible progression en pathologie de conduction plus distale. Dans ce cadre, une deuxième forme de stimulation physiologique a été développée, à savoir la stimulation de la branche gauche (SBG). En substance, la sonde de stimulation y est positionnée 1 à 1,5 cm plus en distal et en apical et vissée jusqu'à stimulation de la branche gauche. Depuis la première description, en 2017, diverses études sont parues démontrant la pertinence et la sécurité de cette méthode, et ce chez des patients avec un complexe QRS tant étroit que large. Une récente publication de Vijayaraman montre ainsi des résultats favorables. Dans cette étude, il a été tenté d'implanter un système de SBG chez 325 patients avec insuffisance cardiaque et indication de TRC. L'intervention a réussi chez 277 des 325 patients (taux de réussite de 85 %). Après un suivi médian de 6 mois, on notait une réduction significative de la durée du QRS (de 152 ms ± 32 ms à 137 ms ± 22 ms ; P < 0,01), une augmentation de la fraction d'éjection ventriculaire gauche (de 33 % ± 10 % à 44 % ± 11 % ; P < 0,01) et une diminution de la classe NYHA (de 2,7 ± 0,7 à 1,8 ± 0,7 ; P < 0,01) (figure 3).14 Les seuils et l'amplitude de l'onde R, qui étaient également étudiés, sont restés stables pendant la période de suivi. En bref, la SBG peut devenir une alternative additionnelle et prometteuse chez les patients non éligibles à la SFH.
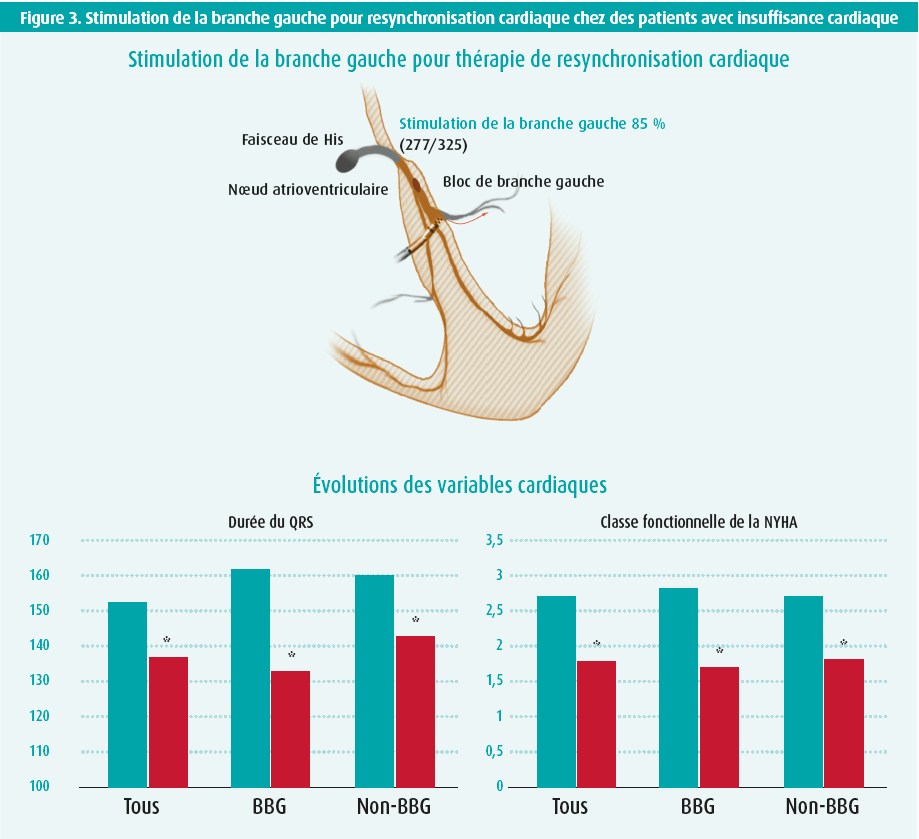
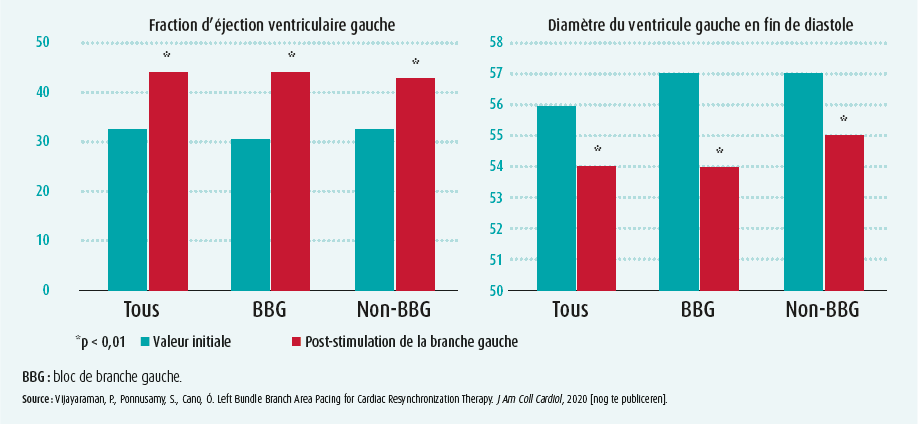
Pourquoi la stimulation du faisceau de His et la stimulation de la branche gauche ne peuvent pas (encore) offrir une alternative à la stimulation biventriculaire
Prof. C. Leclercq
L'utilisation de la SBV en vue d'atteindre une resynchronisation cardiaque a été décrite pour la première fois en 1994 et implémentée pour la première fois dans les recommandations de l'ESC en 2005. Qui plus est, de nombreuses études randomisées en démontrant le bénéfice en termes de morbidité et de mortalité ont déjà été publiées. En outre, plus de 12 000 patients ont déjà été inclus dans ces études. A contrario, la SFH est une méthode plus récente, la première publication remontant à l'année 2000 et la première implémentation dans les recommandations américaines datant de 2018. Contrairement à la SBV, nous ne disposons à ce jour que d'une seule étude randomisée pour la SFH.13 Une étude qui n'a inclus que 41 patients, dans 7 centres, sur une période de 2 ans. Par ailleurs, le suivi médian était court (6 mois) et les critères de jugement évalués étaient tous accessoires (durée du QRS et fraction d'éjection ventriculaire gauche). Lorsque l'on examine en plus les résultats, on remarque d'emblée que la durée de l'intervalle QRS dans le groupe SBV n'est quasi pas réduite (figure 2). Ce, alors que la réduction du QRS par la SBV a pourtant été démontrée à de nombreuses reprises par le passé. Une autre étude importante est celle menée par Huang en 2019. Celle-ci a évalué l'efficacité de la SFH pour corriger un BBG chez 74 patients. Il en est ressorti que la stimulation du faisceau de His était réussie dans seulement 75 % des cas, et ce pour diverses raisons (valeurs seuils élevées, échec de la fixation, etc.). Bien que les résultats de l'étude se soient révélés favorables (augmentation de la fraction d'éjection ventriculaire gauche, réduction du volume en fin de systole et amélioration de la classe NYHA), les effets indésirables ont (trop) peu été soulignés. Un bloc AV complet permanent traumatique a ainsi été causé chez 20 % des patients du groupe SFH, contre aucun dans le groupe SBV.11 Il s'agit là d'une observation importante, à ne pas négliger.
Conclusion
La stimulation du faisceau de His et la stimulation de la branche gauche sont deux formes de stimulation physiologique. Des études sont en cours pour évaluer la sécurité et la pertinence de ces procédures en alternative à la stimulation biventriculaire dans le cadre d'une thérapie de resynchronisation cardiaque chez des patients avec insuffisance cardiaque sévère et dyssynchronie cardiaque. Bien que les études observationnelles montrent des effets favorables, les études randomisées restent rares. De ce fait, ces méthodes ne peuvent pas (encore) être utilisées en traitement de première intention. L'application de ces techniques prometteuses peut cependant déjà être envisagée, en attendant d'autres recherches scientifiques complémentaires, dans les situations où la stimulation biventriculaire n'est pas possible ou ne permet pas d'atteindre une resynchronisation.
Références
- Moss, A.J., Hall, W.J., Cannom, D.S., Klein, H., Brown, M.W., Daubert, J.P. et al. Cardiacresynchronization therapy for the prevention of heart-failure events. N Engl J Med, 2009, 361 (14), 1329-1338.
- Cleland, J.G.F., Daubert, J-C., Erdmann, E., Freemantle, N., Gras, D., Kappenberger, L. et al. The effect of cardiac resynchronization on morbidity and mortality in heart failure. N Engl J Med, 2005, 352 (15), 1539-1549.
- Zareba, W., Klein, H., Cygankiewicz, I., Hall, W.J., McNitt, S., Brown, M. et al. Effectiveness of Cardiac Resynchronization Therapy by QRS Morphology in the Multicenter Automatic Defibrillator Implantation Trial-Cardiac Resynchronization Therapy (MADIT-CRT). Circulation, 2011, 123 (10), 1061-1072.
- Ruschitzka, F., Abraham, W.T., Singh, J.P., Bax, J.J., Borer, J.S., Brugada, J. et al. Cardiacresynchronization therapy in heart failure with a narrow QRS complex. N Engl J Med, 2013, 369 (15), 1395-1405.
- Arnold, A.D., Shun-Shin, M.J., Keene, D., Howard, J.P., Sohaib, S.M.A., Wright, I.J. et al. His Resynchronization Versus Biventricular Pacing in Patients With Heart Failure and Left Bundle Branch Block. J Am Coll Cardiol, 2018, 72 (24), 3112-3122.
- Moriña-Vázquez, P., Moraleda-Salas, M.T., Manovel-Sánchez, A.J., Fernández-Gómez, J.M., Arce-Léon, Á., Venegas-Gamero, J. et al. Early improvement of left ventricular ejection fraction by cardiac resynchronization through His bundle pacing in patients with heart failure. Europace, 2020, 22 (1), 125-132.
- Barba-Pichardo, R., Manovel Sánchez, A., Fernández-Gómez, J.M., Moriña-Vázquez, P., Venegas-Gamero, J., Herrera-Carranza, M. Ventricular resynchronization therapy by direct His-bundle pacing using an internal cardioverter defibrillator. Europace, 2013, 15 (1), 83-88.
- Lustgarten, D.L., Crespo, E.M., Arkhipova- Jenkins, I., Lobel, R., Winget, J., Koehler, J. et al. His-bundle pacing versus biventricular pacing in cardiac resynchronization therapy patients: A crossover design comparison. Heart Rhythm, 2015, 12 (7), 1548-1557.
- Ajijola, O.A., Upadhyay, G.A., Macias, C., Shivkumar, K., Tung, R. Permanent Hisbundle pacing for cardiac resynchronization therapy: Initial feasibility study in lieu of left ventricular lead. Heart Rhythm, 2017, 14 (9), 1353-1361.
- Sharma, P.S., Dandamudi, G., Herweg, B., Wilson, D., Singh, R., Naperkowski, A. et al. Permanent His-bundle pacing as an alternative to biventricular pacing for cardiac resynchronization therapy: A multicenter experience. Heart Rhythm, 2018, 15 (3), 413- 420.
- Huang, W., Su, L., Wu, S., Xu, L., Xiao, F., Zhou, X. et al. Long-term outcomes of His bundle pacing in patients with heart failure with left bundle branch block. Heart, 2019, 105 (2), 137-143.
- Sharma, P.S., Naperkowski, A., Bauch, T.D., Chan, J.Y.S., Arnold, A.D., Whinnett, Z.I. et al. Permanent His Bundle Pacing for Cardiac Resynchronization Therapy in Patients With Heart Failure and Right Bundle Branch Block. Circ Arrhythm Electrophysiol, 2018, 11 (9), e006613.
- Upadhyay, G.A., Vijayaraman, P., Nayak, H.M., Verma, N., Dandamudi, G., Sharma, P.S. et al. His Corrective Pacing or Biventricular Pacing for Cardiac Resynchronization in Heart Failure. J Am Coll Cardiol, 2019, 74 (1), 157- 159.
- Vijayaraman, P., Ponnusamy, S., Cano, Ó. Left Bundle Branch Area Pacing for Cardiac Resynchronization Therapy. J Am Coll Cardiol Clin Electrophysiol, 2020, [publication en attente].
Aucun élément du site web ne peut être reproduit, modifié, diffusé, vendu, publié ou utilisé à des fins commerciales sans autorisation écrite préalable de l’éditeur. Il est également interdit de sauvegarder cette information par voie électronique ou de l’utiliser à des fins illégales.