Le congrès annuel du Belgian Working Group On Non-Invasive Cardiac Imaging (BWGNICI), intitulé Valvular Heart Disease in Heart Failure, s'est tenu le 18 novembre 2022. Toute la journée, d'intéressantes sessions ont été animées par des experts nationaux et internationaux. La session principale de cette année, présentée par Denisa Muraru (Milan, Italie), portait sur l'insuffisance mitrale et tricuspide fonctionnelle auriculaire. Ensuite, des sessions ont été consacrées aux valvulopathies mitrales et tricuspides dans l'insuffisance cardiaque.
Insuffisance mitrale et tricuspide fonctionnelle auriculaire
Denisa Muraru - Milan, Italie
Le traitement d'une valvulopathie fonctionnelle commence par la compréhension du mécanisme physiopathologique grâce au phénotypage de la valvulopathie fonctionnelle. L'insuffisance mitrale fonctionnelle auriculaire (AF-MR) est due à une dilatation de l'anneau couplée à une coaptation insuffisante des feuillets valvulaires, par exemple en raison d'un remodelage auriculaire en cas de fibrillation auriculaire (FA). Contrairement à l'IM fonctionnelle ventriculaire (VF-MR), la dimension et la fonction du ventricule gauche sont plus souvent normales. Cependant, les directives actuelles ne décrivent pas encore l'AF-MR comme une entité distincte, et il n'existe pas encore de recommandations thérapeutiques spécifiques. Les mécanismes physio pathologiques sont, entre autres, une malcoaptation due à une contraction auriculaire présystolique limitée au moment de la FA, un tethering atriogène et une diminution de la transition endothélio- mésenchymateuse (EMT).1-3 Ici, un tethering atriogène est un marqueur de maladie avancée de plus mauvais pronostic et il est associé à une augmentation du nombre d'hospitalisations et de la mortalité (figure 1).4-5
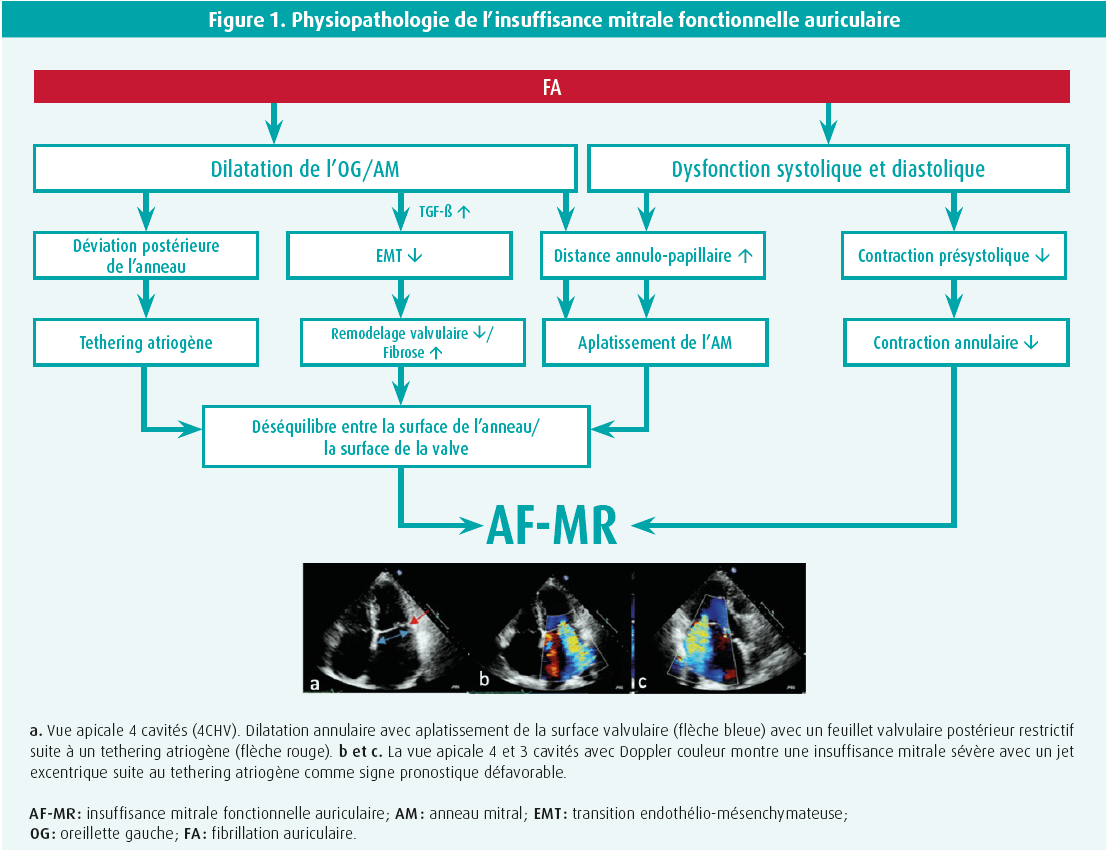
Suite à l'EMT, on observe une augmentation compensatoire de la longueur de la valve en réponse à une expansion de la surface de l'anneau. Une EMT insuffisante entraîne une malcoaptation des feuillets valvulaires. Chez les patients souffrant d'AF-MR traités par inhibiteurs de l'ECA (IECA) ou antagonistes des récepteurs de l'angiotensine (ARB), on a plutôt observé une IM moins sévère et un rapport surface/ fermeture de la valve mitrale plus grand par rapport à ceux qui n'utilisaient pas d'ARB/IECA. Ceci suggère un rôle possible pour les inhibiteurs de l'ECA ou les ARB dans le traitement de l'AF-MR.6 Comparativement à l'IM primaire, l'AF-MR est associée à davantage de comorbidités et d'hospitalisations pour insuffisance cardiaque et à une mortalité plus élevée. En outre, les patients souffrant d'AF-MR sont moins susceptibles de subir des interventions valvulaires.5 Cependant, comme il n'existait auparavant aucune définition claire, le véritable pronostic reste inconnu.7
Par analogie avec l'AF-MR, le remodelage auriculaire peut également entraîner une insuffisance tricuspide fonctionnelle auriculaire (AF-TR). Dans ce cas, le volume de l'oreillette droite est un important élément prédictif de la surface de l'anneau et le rétablissement du rythme sinusal a un effet bénéfique sur le remodelage inverse, avec une restauration fonctionnelle de l'oreillette droite et de l'anneau tricuspide.8-9 La proposition de nouvelle nomenclature de l'IT incluant une distinction entre l'IT fonctionnelle auriculaire et ventriculaire a été adoptée par le Tricuspid Valve Academic Research Consortium (TVARC).
Les défis sur le plan de l'imagerie pour déterminer la sévérité de l'AF-MR/AF-TR comprennent la surestimation du volume du ventricule droit en échocardiographie 2D, l'irrégularité de l'intervalle RR en cas de FA avec une variabilité interbattements et une petite cavité ventriculaire gauche lors de la détermination du volume refluant, où il faut peut-être utiliser d'autres seuils. L'index-beat method est recommandée pour mesurer le signal CW. L'utilisation des volumes 3D est préférable à l'utilisation des diamètres 2D.
La combinaison d'une AF-MR/AF-TR et d'une insuffisance cardiaque ou d'une dysfonction ventriculaire droite est associée à un mauvais pronostic. Une identification et un traitement précoces sont indiqués. La connaissance des défis sur le plan de l'imagerie est nécessaire pour éviter une sous-estimation. Le rétablissement rapide du rythme sinusal pourrait prévenir le remodelage, tant auriculaire que ventriculaire, réduisant ainsi la nécessité d'interventions valvulaires. De plus amples études sur l'effet des inhibiteurs de l'ECA et des ARB sur la sévérité de l'AF-MR/AF-TR sont souhaitables.
Calcification de l'anneau mitral - défis diagnostiques et implications
Philippe Bertrand - ZOL Genk
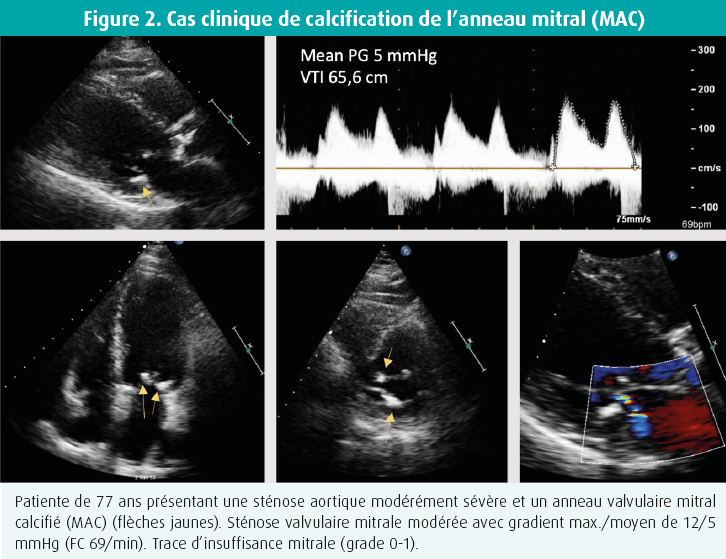
La calcification de l'anneau mitral (MAC) est une observation fréquente, surtout dans la population âgée, et elle est associée à un risque accru de morbi-mortalité cardiovasculaire. En outre, la présence d'une dysfonction valvulaire mitrale liée à la MAC, telle qu'une sténose et/ou une régurgitation, contribuera largement au pronostic défavorable.
L'échocardiographie est la meilleure technique pour évaluer la sténose mitrale (SM) en présence d'une MAC, mais il est important de pointer quelques pièges potentiels dans le calcul de la surface de la valve mitrale. Ainsi, la planimétrie 2D, la référence pour la SM rhumatismale, est souvent peu fiable en présence d'une MAC significative. De plus, la pressure half-time method va typiquement surestimer la surface de la valve mitrale en présence d'une compliance réduite du ventricule ou de l'oreillette gauches, ce qui est fréquent dans cette population âgée. L'équation de continuité constitue vraisemblablement la meilleure méthode, à condition qu'il n'y ait pas de FA, ni de régurgitation aortique ou mitrale significative.10 Le paramètre qui a la plus grande valeur pronostique en cas de dysfonction valvulaire liée à une MAC est le gradient moyen à travers la valve mitrale, en dépit du fait qu'il dépende du rythme cardiaque et du débit cardiaque.11
À ce jour, l'attitude en cas de dysfonction valvulaire mitrale liée à une MAC reste surtout basée sur le traitement médicamenteux, via le contrôle de la fréquence cardiaque, les diurétiques et le traitement d'une éventuelle HFpEF sous-jacente. Les interventions chirurgicales ou percutanées (telles que la valve-in-MAC) sont techniquement très difficiles et ne sont indiquées que dans des cas spécifiques, après mûre discussion au sein d'une équipe cardiaque pluridisciplinaire.
Insuffisance mitrale en cas de TAVI
Frank Timmermans - UZ Gent
L'IM est un phénomène très fréquent chez les patients présentant une sténose sévère de la valve aortique (SA), avec une prévalence comprise entre 2 % et 20 % dans la population TAVI.12 Cependant, la présence d'une IM modérément sévère ou sévère semble plutôt limitée chez ces patients et le mécanisme sous-jacent peut être tant une maladie dégénérative que fonctionnelle de la valve.13 Actuellement, on ne sait toujours pas si on doit utiliser les mêmes valeurs seuils pour une IM sévère dans le contexte d'une SA que dans la population générale, surtout en présence de comorbidités avec une compliance réduite du ventricule ou de l'oreillette gauches.
Après un TAVI, on observe une diminution de l'IM chez environ la moitié des patients, surtout en cas d'IM fonctionnelle. Il serait intéressant de savoir si la présence d'une IM significative (plus que modérée) a un effet sur le pronostic après un TAVI. Bien que les études PARTNER n'aient montré aucune différence de mortalité entre une IM modérément sévère et une IM nulle/légère au départ, d'autres études indiquent qu'une IM significative constitue un facteur pronostique défavorable pour les patients, après un TAVI.12 Ceci s'explique peut-être par le fait qu'une IM fonctionnelle est souvent un marqueur indirect d'une pathologie ventriculaire gauche sous-jacente.
En conclusion, il est nécessaire de mener des études plus approfondies axées sur la quantification et l'hémodynamique de l'IM, afin de mieux phénotyper la population 'IM-TAVI', et de conduire des études randomisées pour analyser l'effet d'une intervention valvulaire mitrale percutanée par rapport au traitement médicamenteux.
Mise à jour de 2022 au sujet de la gradation de l'insuffisance mitrale et tricuspide secondaire
Adriana Postolache - CHU Liège
Étant donné que l'IM secondaire ou fonctionnelle repose sur un mécanisme physiopathologique différent de celui de l'IM primaire, les deux entités posent également leurs propres défis diagnostiques et thérapeutiques. Bien que, ces dernières années, il y ait eu un certain désaccord entre les recommandations européennes et américaines au sujet de la définition de l'IM secondaire sévère, on est parvenu à un consensus international. Les recommandations 2021 de l'ESC et 2020 de l'AHA préconisent toutes deux de définir l'IM secondaire sévère comme un EROA ≥ 40 mm² ou un volume refluant ≥ 60 ml, soit les mêmes valeurs seuils que pour l'IM primaire.14-15
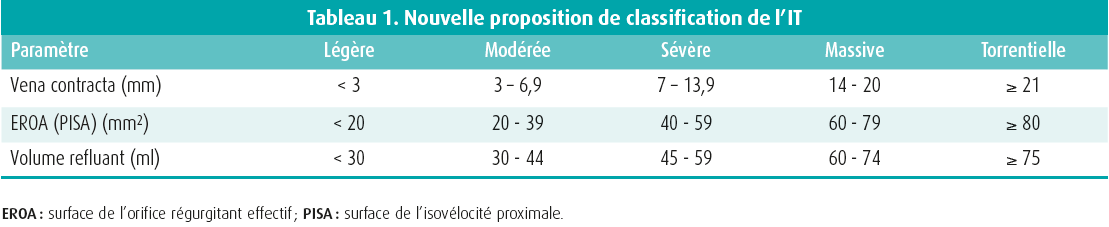
Les dernières recommandations de l'ESC et de l'AHA sont également en phase pour l'évaluation de l'insuffisance tricuspide (IT) secondaire. Une IT sévère (primaire ou secondaire) est définie comme un EROA ≥ 40 mm2 ou un volume refluant ≥ 45 ml et, comme pour l'IM, une prise en charge multi-intégrative est indiquée. Cependant, Rebecca Hahn a récemment introduit deux nouveaux grades pour les valvulopathies tricuspides très sévères : IT 'massive' et IT 'torrentielle' (tableau 1).16 Cette gradation plus précise des IT sera particulièrement importante à une époque où on pratique de plus en plus d'interventions transcathéter sur la valve tricuspide, afin d'identifier les patients entrant en ligne de compte pour un traitement interventionnel et d'en évaluer quantitativement le succès.
Références
- Muraru, D., Guta, A.C., Ochoa-Jimenez, R.C., Bartos, D., Aruta, P., Mihaila, S. et al. Functional Regurgitation of Atrioventricular Valves and Atrial Fibrillation: An Elusive Pathophysiological Link Deserving Further Attention. J Am Soc Echocardiogr, 2020, 33 (1), 42-53.
- Van De Heyning, C., Claeys, M. et al. Annular Dynamics in Patients With Atrial Fibrillation and AFMR. J Am Coll Cardiol Img, 2022, 15 (1), 14-16.
- Mihaila, S., Muraru, D., Miglioranza, M.H., Piasentini, E., Peluso, D., Cucchini, U. et al. Normal mitral annulus dynamics and its relationships with left ventricular and left atrial function. Int J Cardiovasc Imaging, 2015, 31 (2), 279-290.
- Silbiger, J.J. Does left atrial enlargement contribute to mitral leaflet tethering in patients with functional mitral regurgitation? Proposed role of atriogenic leaflet tethering. Echocardiography, 2014, 31 (10), 1310-1311.
- Mesi, O., Gad, M.M., Crane, A.D., Ramchand, J., Puri, R., Layoun, H. Severe Atrial Functional Mitral Regurgitation: Clinical and Echocardiographic Characteristics, Management and Outcomes. JACC Cardiovasc Imaging, 2021, 14 (4), 797-808.
- Kim, D.H., Heo, R., Handschumacher, M.D., Lee, S., Choi, Y.S., Kim, K.R. Mitral Valve Adaptation to Isolated Annular Dilation: Insights Into the Mechanism of Atrial Functional Mitral Regurgitation. JACC Cardiovasc Imaging, 2019, 12 (4), 665-677.
- Alkhouli, M., Hahn, R., Petronio, A. et al. Transcatheter Edge-to-Edge Repair for Atrial Functional Mitral Regurgitation. J Am Coll Cardiol Intv, 2022, 15 (17), 1741-1747.
- Hahn, R.T., Badano, L.P., Bartko, P.E., Muraru, D., Maisano, F., Zamorano, J.L., Donal, E. Tricuspid regurgitation: recent advances in understanding pathophysiology, severity grading and outcome. Eur Heart J Cardiovasc Imaging, 2022, 23 (7), 913-929.
- Soulat-Dufour, L., Lang, S., Addetia, K., Ederhy, S., Adavane-Scheube, S.S., Chauvet- Droit, M. et al. Restoring Sinus Rhythm Reverses Cardiac Remodeling and Reduces Valvular Regurgitation in Patients With Atrial Fibrillation. J Am Coll Cardiol, 2022, 79, 951-961.
- Churchill, T.W., Yucel, E., Deferm, S., Levine, R.A., Hung, J., Bertrand, P.B. Mitral Valve Dysfunction in Patients With Annular Calcification: JACC Review Topic of the Week. J Am Coll Cardiol, 2022, 80 (7), 739-751.
- Bertrand, P.B., Churchill, T.W., Yucel, E., Namasivayam, M., Bernard, S., Nagata, Y., He, W. et al. Prognostic importance of the transmitral pressure gradient in mitral annular calcification with associated mitral valve dysfunction. Eur Heart J, 2020, 41 (45), 4321-4328.
- Nombela-Franco, L., Ribeiro, H.B., Urena, M., Allende, R., Amat-Santos, I., DeLarochellière, R. et al. Significant mitral regurgitation left untreated at the time of aortic valve replacement: a comprehensive review of a frequent entity in the transcatheter aortic valve replacement era. J Am Coll Cardiol, 2014, 63 (24), 2643-2658.
- Barbanti, M., Webb, J.G., Hahn, R.T., Feldman, T., Boone, R.H., Smith, C.R. et al. Placement of Aortic Transcatheter Valve Trial Investigators. Impact of preoperative moderate/severe mitral regurgitation on 2-year outcome after transcatheter and surgical aortic valve replacement: insight from the Placement of Aortic Transcatheter Valve (PARTNER) Trial Cohort A. Circulation, 2013, 128 (25), 2776-2784.
- Vahanian, A., Beyersdorf, F., Praz, F., Milojevic, M., Baldus, S., Bauersachs, J. et al. ESC/EACTS Scientific Document Group. 2021 ESC/EACTS Guidelines for the management of valvular heart disease. Eur Heart J, 2022, 43 (7), 561-632.
- Otto, C.M., Nishimura, R.A., Bonow, R.O., Carabello, B.A., Erwin, J.P.3rd, Gentile, F. et al. 2020 ACC/AHA Guideline for the Management of Patients With Valvular Heart Disease: A Report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. Circulation, 2021, 143 (5), e72-e227.
- Hahn, R.T., Zamorano, J.L. The need for a new tricuspid regurgitation grading scheme. Eur Heart J Cardiovasc Imaging, 2017, 18 (12), 1342-1343.
Aucun élément du site web ne peut être reproduit, modifié, diffusé, vendu, publié ou utilisé à des fins commerciales sans autorisation écrite préalable de l’éditeur. Il est également interdit de sauvegarder cette information par voie électronique ou de l’utiliser à des fins illégales.