La nécessité d'une intervention précoce pour éviter la progression de la fibrillation auriculaire (FA) a été largement abordée lors du symposium de Boston, entièrement consacré à la FA. à l'aide de plusieurs études marquantes, on a décrit une évolution dans la prise en charge de ce trouble du rythme, qui modifiera sans aucun doute les futures recommandations.
Implications cliniques de l'étude EAST-AF
Andreas Rillig - University Heart & Vascular Center, Hambourg, Allemagne
Classiquement, la stratégie de contrôle du rythme était réservée aux patients souffrant de FA symptomatique. C'est également ce que préconisent les recommandations actuelles de l'ESC.1 L'étude EAST-AF est la première étude multicentrique randomisée qui a démontré un bénéfice pronostique de la stratégie de contrôle du rythme comparativement à la stratégie de contrôle de la fréquence dans une population de patients présentant une FA récemment diagnostiquée (diagnostic au cours de l'année écoulée). En effet, on a observé un risque moindre d'un critère d'évaluation cardiovasculaire combiné constitué des décès cardiovasculaires, des AVC, des hospitalisations pour insuffisance cardiaque et des syndromes coronariens (HR 0,79 [0,66-0,94]; P = 0,005).2 L'effet d'une stratégie de contrôle du rythme précoce est surtout médié par la présence d'un rythme sinusal 12 mois après le début du traitement (estimation: 81 % d'effet du traitement). Dès lors, dans cette population de patients, il semble indiqué de tendre au maintien du rythme sinusal et, si nécessaire, de modifier le traitement de contrôle du rythme (antiarythmiques et/ ou ablation par cathéter).3
En outre, plusieurs sous-analyses de l'étude EAST-AF ont montré que l'effet du traitement se maintenait dans différentes sous-populations. Ceci s'applique également aux patients souffrant d'insuffisance cardiaque (HFpEF, HFmrEF et HFrEF).4 Une stratégie de contrôle du rythme précoce a conduit à un meilleur pronostic dans les différents sous-types de FA (premier diagnostic, FA paroxystique et persistante).5 Bien que les recommandations européennes actuelles réservent la stratégie de contrôle du rythme aux patients symptomatiques, une stratégie de contrôle du rythme précoce a un effet pronostique tout aussi favorable chez les patients asymptomatiques. En effet, 30 % de la population de l'étude EAST-AF était asymptomatique.6 Des données récentes montrent également que l'effet du traitement est préservé chez les patients ayant un antécédent d'AVC, une sous-population courant un risque accru de nouvel AVC et de complications cardiovasculaires (HR 0,52 [0,29-0,93]).7 Bien que les recommandations européennes pour la stratégie de contrôle du rythme préconisent plutôt cette stratégie chez les patients ayant peu de comorbidités, une sous-analyse a montré que, précisément chez les patients ayant un score CHA2DS2-VASc ≥ 4, le critère d'évaluation combiné était significativement moins prévalent (HR 0,64 [0,51-0,81]; P < 0,001), ce qui n'était pas le cas chez les patients ayant un score CHA2DS2-VASc < 4 (HR 0,93 [0,73-1,19]; P = 0,56).8
Implications cliniques des études Cryo-FIRST, EARLY-AF et STOP-AF First
Carlos Morillo - Libin Cardiovascular Institute, Calgary, Canada
Il est important de souligner que l'étude EAST-AF n'est pas une étude d'ablation, car seulement 20 % des patients du groupe intervention ont été traités par ablation. En tout cas, il est prouvé que l'ablation par cathéter à cryoballon est meilleure que les antiarythmiques en traitement de première ligne pour éviter une récidive de FA chez les patients souffrant de FA paroxystique. Ceci a également été démontré dans 3 études multicentriques prospectives randomisées avec une durée de suivi d'un an (tableau 1).
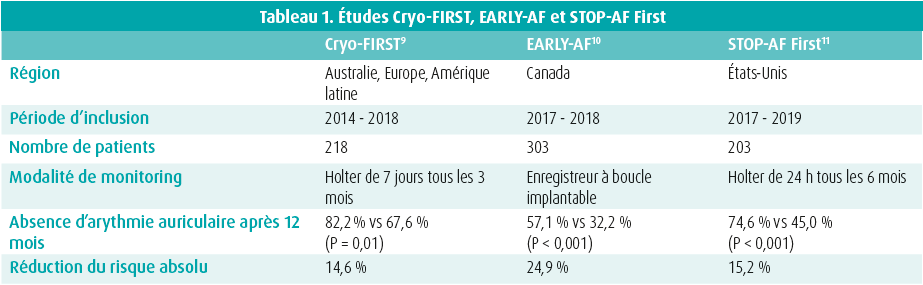
Les études diffèrent en ce qui concerne l'absence d'arythmie auriculaire après 12 mois, en raison d'une différence dans la modalité de monitoring. Cependant, elles montrent toutes une importante réduction du risque absolu. L'étude EARLY-AF s'est distinguée des autres par un monitoring continu à l'aide d'enregistreurs à boucle implantables. Dans cette étude, le NNT (number needed to treat) n'était que de 4.
Une récidive de FA est classiquement définie comme 30 secondes de FA après l'intervention, mais cette limite est évidemment arbitraire. Grâce aux enregistreurs à boucle implantables, l'étude EARLY-AF a fourni des informations non seulement sur un critère d'évaluation binaire (récidive ou non), mais aussi sur le fardeau de la FA. L'étude a montré un fardeau de FA minime dans le groupe intervention, avec une moyenne de 0,6 ± 3,3 % (groupe contrôle 3,9 ± 12,4 %). Le groupe d'Andrade et al. a déjà montré que les patients ayant un fardeau de FA > 0,1 % avaient davantage recours aux soins de santé, ce qui constitue un critère d'évaluation cliniquement pertinent.12
Il est important de noter que les études portant sur l'ablation ont principalement inclus des patients jeunes et en bonne santé, alors que dans l'étude EAST-AF, les patients ayant un score CHA2DS2-VASc ≥ 4 avaient le meilleur pronostic après une stratégie de contrôle du rythme. L'efficacité et la sécurité de l'ablation par cathéter doivent donc être évaluées plus en détail dans le cadre d'études randomisées incluant des patients présentant de multiples comorbidités. Le suivi trop court (5 ans) de cette population en relativement bonne santé (score CHA2DS2-VASc < 4) explique potentiellement pourquoi les patients de l'étude EAST-AF n'ont pas eu un meilleur pronostic.
Implications cliniques des études ATTEST-AF et PROGRESSIVE-AF
Laurent Macle - Montreal Heart Institute, Canada
La FA est une affection progressive avec une évolution annuelle d'une forme paroxystique vers une forme persistante d'environ 7 %. La FA persistante a un pronostic plus défavorable avec un risque plus élevé d'AVC, d'insuffisance cardiaque, de syndrome coronarien et de décès.13,14 Deux études multicentriques prospectives randomisées, toutes deux avec une durée de suivi de 3 ans, ont comparé l'effet de l'ablation par rapport à des antiarythmiques sur l'évolution d'une FA paroxystique vers une FA persistante (tableau 2). Les deux études ont inclus une population de patients différente. Dans l'étude ATTEST-AF, les patients présentaient déjà une récidive de FA paroxystique sous au moins un antiarythmique (préconisé par les recommandations européennes actuelles), tandis que dans l'étude PROGRESSIVE-AF, l'ablation avait été proposée en première ligne. Comme prévu, on notait une grande différence de délai entre le diagnostic et l'ablation entre ces 2 études, avec une moyenne de 4 ans dans l'étude ATTEST-AF et d'un an dans l'étude PROGRESSIVE-AF. Ainsi, la population de l'étude PROGRESSIVE-AF était à un stade plus précoce de la maladie.

La FA est une affection chronique et évolutive. Malgré les différences dans le stade de la FA paroxystique et la modalité de traitement utilisée, les deux études ont montré que l'ablation empêche mieux la progression de la maladie que les antiarythmiques.
Conclusion
Malgré la pandémie de COVID, les 3 dernières années ont été extrêmement passionnantes pour la communauté des électrophysiologistes. En ce qui concerne la FA, il est désormais prouvé qu'une stratégie de contrôle du rythme précoce a un effet pronostique favorable et que l'ablation par cathéter diminue les récidives et la progression de la maladie, comparativement aux antiarythmiques. Il faut encore prouver que l'ablation par cathéter pour une FA à un stade précoce a un meilleur effet pronostique que les antiarythmiques. Quoi qu'il en soit, l'ablation par cathéter jouera un rôle encore plus important dans les recommandations européennes consacrées à la FA, qui devraient être publiées l'an prochain. Compte tenu de la prévalence élevée (et croissante) de la FA, l'organisation de toutes ces procédures constituera un véritable défi.
Références
- Hindricks, G., Potpara, T., Dagres, N., Arbelo, E., Bax, J.J., Blomstrom-Lundqvist, C. et al. 2020 ESC Guidelines for the diagnosis and management of atrial fibrillation developed in collaboration with the European Association for Cardio-Thoracic Surgery (EACTS): The Task Force for the diagnosis and management of atrial fibrillation of the European Society of Cardiology (ESC) Developed with the special contribution of the European Heart Rhythm Association (EHRA) of the ESC. Eur Heart J, 2021, 42 (5), 373-498.
- Kirchhof, P., Camm, A.J., Goette, A., Brandes, A., Eckardt, L., Elvan, A. et al. Early Rhythm-Control Therapy in Patients with Atrial Fibrillation. N Engl J Med, 2020, 383 (14), 1305-1316.
- Eckardt, L., Sehner, S., Suling, A., Borof, K., Breithardt, G., Crijns, H. et al. Attaining sinus rhythm mediates improved outcome with early rhythm control therapy of atrial fibrillation: the EAST-AFNET 4 trial. Eur Heart J, 2022, 43 (40), 4127-4144.
- Rillig, A., Magnussen, C., Ozga, A.K., Suling, A., Brandes, A., Breithardt, G. et al. Early Rhythm Control Therapy in Patients With Atrial Fibrillation and Heart Failure. Circulation, 2021, 144 (11), 845-858.
- Goette, A., Borof, K., Breithardt, G., Camm, A.J., Crijns, H., Kuck, K.H. et al. Presenting Pattern of Atrial Fibrillation and Outcomes of Early Rhythm Control Therapy. J Am Coll Cardiol, 2022, 80 (4), 283-295.
- Willems, S., Borof, K., Brandes, A., Breithardt, G., Camm, A.J., Crijns H. et al. Systematic, early rhythm control strategy for atrial fibrillation in patients with or without symptoms: the EAST-AFNET 4 trial. Eur Heart J, 2022, 43 (12), 1219-1230.
- Calvert, P., Gupta, D., Lip, G.Y.H. Early atrial fibrillation rhythm control after stroke. Lancet Neurol, 2023, 22 (1), 3-4.
- Rillig, A., Borof, K., Breithardt, G., Camm, A.J., Crijns, H., Goette, A. et al. Early Rhythm Control in Patients With Atrial Fibrillation and High Comorbidity Burden. Circulation, 2022, 146 (11), 836-847.
- Kuniss, M., Pavlovic, N., Velagic, V., Hermida, J.S., Healey, S., Arena, G. et al. Cryoballoon ablation vs. antiarrhythmic drugs: first-line therapy for patients with paroxysmal atrial fibrillation. Europace, 2021, 23 (7), 1033-1041.
- Andrade, J.G., Wells, G.A, Deyell, M.W., Bennett, M., Essebag, V., Champagne, J. et al. Cryoablation or Drug Therapy for Initial Treatment of Atrial Fibrillation. N Engl J Med, 2021, 384 (4), 305-315.
- Wazni, O.M., Dandamudi, G., Sood, N., Hoyt, R., Tyler, J., Durrani, S. et al. Cryoballoon Ablation as Initial Therapy for Atrial Fibrillation. N Engl J Med, 2021, 384 (4), 316-324.
- Andrade, J.G., Deyell, M.W., Macle, L., Steinberg, J.S., Glotzer, T.V., Hawkins, N.M. et al. Healthcare utilization and quality of life for atrial fibrillation burden: the CIRCA-DOSE study. Eur Heart J, 2023, 44 (9), 765-776.
- Ganesan, A.N., Chew, D.P., Hartshorne, T., Selvanayagam, J.B., Aylward, P.E., Sanders, P. et al. The impact of atrial fibrillation type on the risk of thromboembolism, mortality, and bleeding: a systematic review and meta-analysis. Eur Heart J, 2016, 37 (20), 1591-1602.
- Chiang, C.E., Naditch-Brule, L., Murin, J., Goethals, M., Inoue, H., O'Neill, J. et al. Distribution and risk profile of paroxysmal, persistent, and permanent atrial fibrillation in routine clinical practice: insight from the real-life global survey evaluating patients with atrial fibrillation international registry. Circ Arrhythm Electrophysiol, 2012, 5 (4), 632-639.
- Kuck, K.H., Lebedev, D.S., Mikhaylov, E.N., Romanov, A., Geller, L., Kalejs, O. et al. Catheter ablation or medical therapy to delay progression of atrial fibrillation: the randomized controlled atrial fibrillation progression trial (ATTEST). Europace, 2021, 23 (3), 362-369.
- Andrade, J.G., Deyell, M.W., Macle, L., Wells, G.A., Bennett, M., Essebag, V. et al. Progression of Atrial Fibrillation after Cryoablation or Drug Therapy. N Engl J Med, 2023, 388 (2), 105-116.
Aucun élément du site web ne peut être reproduit, modifié, diffusé, vendu, publié ou utilisé à des fins commerciales sans autorisation écrite préalable de l’éditeur. Il est également interdit de sauvegarder cette information par voie électronique ou de l’utiliser à des fins illégales.