Het Marokkaanse veldhospitaal in het Jordaanse kamp Zaatari op de grens met Syrië heeft sinds zijn oprichting in 2012 al meer dan 500 000 vluchtelingen opgevangen. De medische prestaties betreffen vooral zuigelingen en kinderen met overwegend infectieziekten die eigen zijn aan kinderen op de vlucht. Toch wordt de aandacht van de 2 kinderartsen daar ook vaak door zeldzame aandoeningen getrokken. Ondanks de schaarse middelen en de hoge toestroom van patiënten proberen de kinderartsen die speciale aandoeningen zo goed mogelijk op te vangen. We rapporteren het geval van een jongetje van 4 jaar dat sinds 1 jaar in het kamp verbleef en dat voordien in Syrië werd gemonitord wegens een bilaterale doofheid waarvan de oorsprong niet bekend was. Sinds ongeveer 2,5 jaar vertoonde het kind syncopes, voorafgegaan door syncopale neigingen. Het gezin had al een dochtertje verloren op de leeftijd van 5 jaar wegens een plotselinge hart- en ademhalingsstilstand. Het ecg dat van de jongen afgenomen werd in het Marokkaanse ziekenhuis toonde een verlengd QT-interval van 600 msec. Het hart zag er normaal uit bij echocardiografie. Het Jervell-Lange-Nielsen-syndroom (SJLN), een autosomaal recessieve aandoening, is een zeldzaam maar mogelijk levensbedreigend syndroom als de diagnose gemist wordt. We kennen al twee genen: KCNQ1 en KCNE1. Die worden vooral tot expressie gebracht in de stria vascularis en zijn verantwoordelijk voor de perceptiedoofheid. De behandeling heeft tot doel syncopes, hartstilstand en plotselinge dood te voorkomen.
Inleiding
Het Jervell-Lange-Nielsen-syndroom (SJLN) wordt gekenmerkt door een aangeboren bilaterale doofheid en een verlengd QT-interval op het elektrocardiogram (> 500 msec.). Die verlenging veroorzaakt ventrikeltachycardie, torsade de pointes en ventrikelfibrillatie met klinische syncopes bij stress (typisch syncope tijdens het wenen of het spelen). Die syncope kan uitmonden in een plotselinge dood.1 Aangezien het een autosomaal recessieve aandoening betreft, zijn er klassiek geen familiale antecedenten, maar gezien de mogelijke ernst van het syndroom is het toch wenselijk een anamnese af te nemen van de familieleden en navraag te doen naar flauwtes en gevallen van plotselinge dood in de familie.
Observatie
We beschrijven hier het geval van een 4-jarige jongen. Zijn ouders zijn tweedegraads bloedverwanten. Er is geen voorgeschiedenis van doofheid of plotselinge dood in de familie van de twee ouders, maar de anamnese leert dat een ouder zusje in Syrië op de leeftijd van 5 jaar overleden is en dat het een plotse dood betrof tijdens een gewoon spel waarbij matige inspanning geleverd werd. Bij de familiale anamnese op dat moment bleek dat het broertje doof was, maar gezien de politieke omstandigheden - een land in oorlog met veel vluchtelingen - kon de diagnose niet bevestigd worden. Een jaar nadat de jongen zijn land verlaten had, is hij op het spreekuur kindergeneeskunde van het Marokkaanse ziekenhuis gekomen wegens herhaalde malaise bij wisselende inspanningen, doofheid en niet spreken. Aangezien het beeld zeer suggestief was voor een JLNS, hebben we meteen een elektrocardiogram afgenomen (figuur 1). Dat toonde een regelmatig sinusritme, smalle QRS-complexen, een normaal PR-interval, een gecorrigeerd QT-interval van 600 msec. en een abnormale repolarisatie met een negatieve T-top. Uit de echocardiografie die de cardioloog ter plaatse uitvoerde bleek dat het hart een normale architectuur en een goede systolische functie had, en geen afwijkingen vertoonde. Het neus-keel-ooronderzoek toonde een bilaterale doofheid zonder afwijkingen bij otoscopie. Het bloedonderzoek toonde een hypochrome anemie en een normaal serumkalium. We zijn een behandeling met bètablokkers gestart in afwachting dat het kind uit het kamp zou worden geëvacueerd voor een eventuele inplanting van een cochlea-implantaat en een genetisch advies.
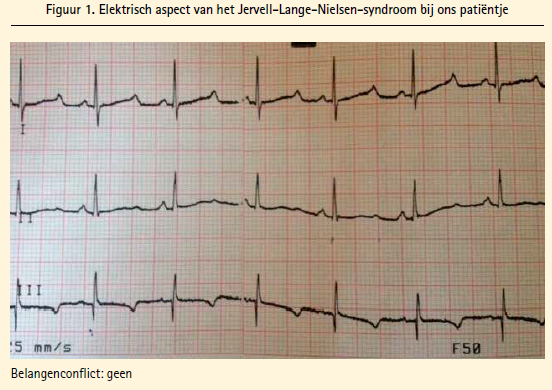
Commentaar
Het JLN-syndroom is een zeldzame aandoening, die levensbedreigend kan zijn. Het syndroom werd voor het eerst beschreven in 1957 in een publicatie door Anton Jervell.1 Helaas wordt de diagnose van het syndroom vaak laat gesteld, zodat de kinderen een risico lopen op plotselinge dood door ritmestoornissen of asystolie. Ongeveer de helft van de kinderen met het syndroom sterft voor de leeftijd van 20 jaar. In de literatuur lezen we dat 15 % van de kinderen symptomen vertoont voor de leeftijd van 23 maanden. Minstens 90 % van de patiënten van 18 jaar of ouder met een JLN-syndroom heeft al een cardiaal accident gehad.2 Je moet altijd een ecg aanvragen bij kinderen met een ernstige tot zeer ernstige doofheid waarvan de oorzaak niet bekend is, vooral als het kind een algemene anesthesie moet ondergaan.3
Het lange-QT-syndroom wordt gekenmerkt door een verlengd QT-interval, recidiverende syncopes en maligne ventriculaire tachyaritmieën. Het syndroom kan familiaal zijn, met of zonder aangeboren of idiopathische doofheid. Waarom het JLNS doofheid veroorzaakt, weten we nog niet goed. Neyround et al.4 hebben aangetoond dat het JLNS-gen en het KVLQT1-gen op chromosoom 11 een primordiale rol spelen bij de ventrikelrepolarisatie en de homeostase van de endolymfe. De kinderen vertonen een aangeboren, geïsoleerde, diepe of ernstige, bilaterale doofheid, vooral voor de hoge frequenties. Er zijn geen vestibulaire afwijkingen.
Het JLNS wordt autosomaal recessief overgedragen. De ouders van het patiëntje dat we in het vluchtelingenkamp hebben gezien, waren verre neef en nicht, wat wel vaker het geval is bij autosomaal recessieve aandoeningen. In Syrië is een huwelijk tussen leden van hetzelfde gezin verboden om religieuze redenen, maar andere consanguïene huwelijken - zoals tussen een oom en een nicht of tussen verre neven en nichten - worden aangemoedigd en horen bij de plaatselijke gebruiken. Een studie in Saoedi-Arabië5 heeft aangetoond dat gearrangeerde huwelijken binnen eenzelfde familie een nefast genetisch effect hebben en dat het aantal kinderen met genetische aandoeningen naar schatting 23 % bedraagt. Een eerste geval van JLNS werd gerapporteerd in 1996.6
De genetische oorzaak van het JLNS is intussen bevestigd; we kennen al zes loci en vijf genen. In recente genetische studies werden in 10-15 % van de gevallen van onverklaarde plotselinge dood waarbij een autopsie uitgevoerd werd, mutaties vastgesteld die een lange-QTsyndroom veroorzaken.7 De diagnose wordt gesteld met een elektrofysiologisch onderzoek, waarvan de resultaten soms moeilijk te interpreteren zijn, en met een uitgebreid genetisch onderzoek. Het preventieve en therapeutische beleid hangt immers af van het genotype.8 Sinds de ontdekking van het eerste gen in 1997 werden 10 genen en meer dan 200 mutaties in verband gebracht met dit syndroom.9
Dankzij een levenslange behandeling met bètablokkers is de mortaliteit in 10 jaar tijd gedaald van 75 % naar 5 %. Nu bedraagt de sterfte ongeveer 0,2 tot 0,5 % per jaar.10
Bètablokkers onderdrukken de adrenerge respons. Ze verminderen de flauwtes, ook al hebben ze nagenoeg geen invloed op de duur van het QT-interval. Bij dit patiëntje zijn we een behandeling met nadolol gestart. De therapietrouw werd wekelijks gecontroleerd. Daardoor is het aantal flauwtes gedaald met ongeveer 50 %, maar het verlengde QT-interval bleef zichtbaar op de latere ecg's.
We schrijven dus bètablokkers voor om activering van het sympathische zenuwstelsel af te remmen. De respons op bètablokkers verschilt echter van de ene patiënt tot de andere. In de studie van met een JLNS nog altijd ernstige ritmestoornissen ondanks een behandeling met bètablokkers en 51 % vertoonde nog altijd symptomen.11 Die slechte resultaten werden waargenomen als bètablokkers gecombineerd werden met een linker cervicothoracale sympathectomie (LCSD) of plaatsing van een pacemaker om een eventuele bradycardie te voorkomen. De enige oplossing is dan een AID (automatische implanteerbare defibrillator). Alleen daarmee kan je plotselinge dood voorkomen. Maar een AID moet gecombineerd worden met een linker cervicothoracale sympathectomie (LCSD) om het aantal schokken dat de defibrillator afgeeft, te verlagen.
Conclusie
Het Jervell-Lange-Nielsen-syndroom is een zeldzame maar ernstige aandoening. Bij dit kind hebben we de diagnose gesteld tijdens een humanitaire opdracht naar aanleiding van herhaalde syncopes. Bij kinderen met een ernstige tot diepe doofheid waarvan de oorzaak niet bekend is en cardiale accidenten, moet je altijd een ecg afnemen. In geval van een JLNS moet de patiënt stressfactoren mijden en moeten er tijdens een heelkundige ingreep voorzorgsmaatregelen genomen worden. Een behandeling met bètablokkers verlaagt het overlijdensrisico. Samenwerking tussen genetici, fysiologen en artsen is wenselijk om het verband tussen het fenotype en het genotype beter te preciseren en om de therapeutische indicaties te verfijnen. Plotselinge dood bij hoogrisicopatiënten kan alleen voorkomen worden met een automatische implanteerbare defibrillator.
Referenties
- Jervell, A., Lange-Nielsen, F. Congenital deaf-mutism, functional heart disease with prolongation of the Q-T interval, and sudden death. Am Heart J, 1957, 54 (1), 59-68.
- Schwartz, P.J., Moss, A.J., Vincent GM, Crampton RS. Diagnostic criteria for the long QT syndrome. An update. Circulation, 1993, 88 (2), 782-784.
- Mayhew, J.F. Anaesthesia and undiagnosed Jervell and Lange-Nielsen syndrome (letter; comment). Anaesthesia, 1993, 48 (12), 1117-1118.
- Neyround, N., Tesson, F., Denjoy, I. A novel mutation in the potassium channel gene KVLQT1 causes the Jervell and Lange-Nielsen syndrome. Nat Genet, 1997, 15 (2), 186-189.
- Zakzouk, S., El-Sayed, Y. and Bafaqeeh, S. Consanguinity and hereditary hearing impairment among Saudi population. Ann Saudi Med, 1993, 13 (5), 447-450.
- Al Rakaf, M., Zakzoukb, S.M., Al Shahwan, S.A.. Jervell and Lange-Nielsen QT syndrome: a casereport from Saudi Arabia. Int J Pediatr Otorhinolaryngol, 1997, 39 (2), 163-168.
- Tester, D., Ackerman, M. Postmortem long QT syndrome genetic testing for sudden unexplained death in the young. J Am Coll Cardiol, 2007, 49 (2), 240-246.
- Jullien, C., Patural, H., Teyssier, G., Dacosta, A. [Ventricular repolarisation disorders and long QT syndrome: clinical and genetic study in 10 paediatric cases]. Arch Pediatr, 2008, 15 (4), 410-415.
- Gao, Y., Li, C., Liu, W., Wu, R., Qiu, X., Liang, R. et al. Genotype-phenotype analysis of three Chinese families with Jervell and Lange-Nielsen syndrome. J Cardiovasc Dis Res, 2012, 3, 67-75.
- Lupoglazoff, J., Denjoy, I., Guicheney, P., Casasoprana, A., Coumel, P. [Congenital long QT syndrome]. Arch Pediatr, 2001, 8 (5), 525-534.
- Villain, E., Denjoy, I., Lupoglazoff, J., Guicheney, P., Hainque, B., Lucet, V. et al. Low incidence of cardiac events with beta-blocking therapy in children with long QT syndrome. Eur Heart J, 2004, 25 (16), 1405-1411.
Aucun élément du site web ne peut être reproduit, modifié, diffusé, vendu, publié ou utilisé à des fins commerciales sans autorisation écrite préalable de l’éditeur. Il est également interdit de sauvegarder cette information par voie électronique ou de l’utiliser à des fins illégales.