Historische achtergrond
In de beginjaren van de elektrofysiologie was fluoroscopie de enige beschikbare beeldvormingstechniek om de positie en beweging van diagnostische katheters en ablatiekatheters in het hart te visualiseren. Initieel werd voor de registratie van elektrische signalen in het hart uitsluitend gebruikgemaakt van uni- en bipolaire katheters1. In het begin van de jaren 1990 werd voor het eerst gebruikgemaakt van multipolaire katheters (bv. 10 of 20 polen) voor de simultane registratie van elektrische activiteit in het hart, bv. om het activatiepatroon van isthmusdependente fluttercircuits in het rechter atrium te visualiseren2. Met de introductie van de eerste elektroanatomische mappingsystemen in de klinische praktijk in 1997 werd een nieuwe weg ingeslagen. Dankzij deze mappingsystemen werd het mogelijk om complexere aritmiëen in kaart te brengen en te behandelen, en dit met kortere fluoroscopie- en proceduretijden3.
Conventionele mappingsystemen
De eerste elektroanatomische mappingsystemen (EAMs) die eind jaren 1990 op de markt kwamen zijn EnSite NavX (St. Jude Medical, Minneapolis, MN, USA) en CARTO (Biosense Webster, Diamond Bar, CA, USA).
Het EnSite-systeem maakt voor het lokaliseren van katheters in het hart gebruik van een hoogfrequent elektroveld (8 kHz) dat gegenereerd wordt door het verzenden van wisselstroom tussen paren van elektrodepatches die op de borstkas van de patiënt gekleefd worden4.
Het CARTO3-systeem is een hybride systeem dat naast een elektrisch impedantiegebaseerd systeem zoals bij EnSite tevens gebruik maakt van een laag energetisch elektromagnetisch veld om de exacte locatie van de katheters in het hart te bepalen5.
Beide systemen hebben echter als belangrijkste nadeel dat de diverse EGMs en hun bijbehorende locatie in het hart punt per punt bepaald moeten worden en hun tijdsannotatie (aanduiden van het begin van het correcte EGM) vaak manueel gecorrigeerd moet worden6, waardoor dit niet zelden omslachtige en tijdrovende procedures zijn. Door deze manier van werken is het vaak onbegonnen werk om voldoende EGMs te registreren om een heel gedetailleerde map van de beoogde hartkamer te creëren (waar vaak duizenden EGMs voor nodig zijn). Door het relatief kleine aantal beschikbare EGMs gaat het systeem deze interpoleren om de map van het hart volledig op te vullen. Dit heeft als risico dat kleine littekens of re-entrycircuits soms onvoldoende in beeld gebracht kunnen worden.
Als reactie hierop werden de laatste jaren verschillende multi-elektrodemappingkatheters (MEM) ontworpen, met als doel om sneller een meer gedetailleerde mapping van de verschillende hartkamers te kunnen verkrijgen ('high-definition mapping').
High-definition mappingsystemen
Het RHYTHMIA HDx (Boston Scientific, Marlborough, MA, US) systeem is een hybride magnetisch-elektrisch, (zoals bij CARTO3) geautomatiseerd hogedensiteits-mappingsysteem, dat gebruikmaakt van een 8,5 F bidirectioneel stuurbare 64-polige geïrrigeerde 'minibasket' mappingkatheter (Intellamap Orion) (figuur 1). De basket van de Orion bestaat uit 8 splinten met telkens 8 vlakke mini-elektroden (0.4 mm2). De basket kan ontplooid worden tot een maximale diameter van 22 mm. In de neus van de katheter zit een magnetische sensor, die in relatie tot een magnetisch veld onder de onderzoekstafel de locatie van de katheter in het hart aangeeft. Verder wordt er gebruik gemaakt van impedantie-gebaseerde sensing op alle 64 mini-elektroden, waardoor de Orionkatheter een navigationele accuraatheid van ≤ 1 mm heeft7. Tijdens het opbouwen van de geometrie wordt simultaan een voltagemap (bipolair/unipolair) en een activatiemap (tijdens sinusritme, pacing of tachycardie) gemaakt. Door de hoge anatomische accuraatheid is fusie met een CT-scan vaak niet nodig. Het RHYTHMIA HDx-systeem heeft een aantal belangrijke voordelen ten aanzien van de conventionele mappingsystemen. Ten eerste kunnen door het grote aantal elektroden veel meer EGMs tegelijk geregistreerd worden (kwantiteit), gemiddeld ca. 1000 punten/ minuut8. Hierdoor is het gemakkelijker om niet-onderhouden aritmiëen te mappen, alsook aritmiëen die hemodynamische instabiliteit teweegbrengen. Het RHYTHMIA HDx-systeem accepteert hierbij enkel EGMs die geregistreerd worden binnen 2-4 mm van de opgebouwde geometrie. Door de snelheid van mapping is het ook gemakkelijker om een 're-map' te maken.
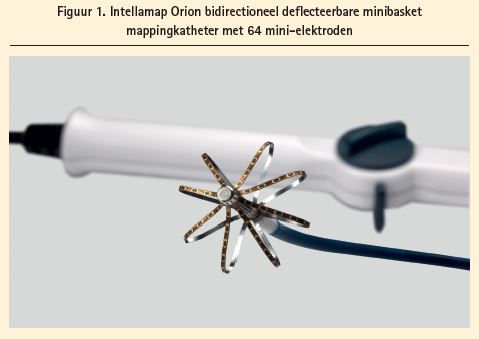
Door de kleine oppervlakte van de elektroden en doordat ze kort bij elkaar gemonteerd zijn, wordt er verder ook een veel betere resolutie (kwaliteit) bekomen in vergelijking met andere mapping katheters8. Hierdoor wordt een scherpere registratie van het 'nearfield' signaal bekomen, met minder interferentie van 'farfield' signalen en van ruis9. Dit heeft als resultaat dat gebieden met lage voltages meer gedetailleerd in kaart gebracht kunnen worden, enerzijds door meer contrast binnen de regio van interesse, maar anderzijds ook doordat heel kleine signalen nu veel beter gedetecteerd kunnen worden wegens minder interferentie van ruis (drempel voor ruis bedraagt slechts ca. 0,01 mV10) en door het gebruik van speciale filters om lage amplitudesignalen te detecteren. Zo wordt regelmatig gezien dat er binnen littekenzones nog kleine kanaaltjes van geleidend weefsel met heel lage voltages lopen, dewelke met een klassiek EAMs nooit gedetecteerd zouden worden (tot 30 % minder littekenoppervlakte < 0,5 mV bij atriale mapping bij RHYTHMIA HDx11). Verder is het ook vaker mogelijk om bij reentry-tachycardiëen een zone binnen de cirkeltachycardie te definiëren alwaar met een beperkt aantal ablatiepunten een succesvolle behandeling verkregen kan worden. Doordat de beoogde zone voor ablatie mooi gevisualiseerd kan worden, is er verder ook geen noodzaak meer voor entrainmentmanoeuvres om te confirmeren dat de ablatiekatheter zich op de plaats van het re-entrycircuit bevindt.
Het RHYTHMIA HDx-systeem heeft daarenboven een geavanceerd algoritme voor accurate automatische annotatie van zowel uni- als bipolaire EGMs, waarbij de timing wordt geannoteerd op het punt van maximale dV/dt van het unipolaire EGM en op het punt van maximale amplitude van het bipolaire EGM7. Indien op een bepaalde plaats multipele EGM's geregistreerd worden, kijkt het systeem automatisch naar EGM's in de nabije omgeving om op basis van een consistentiecriterium te beslissen welk EGM vermoedelijk het meest correcte is om te annoteren12.
Ten slotte kunnen ook artefacten aanleiding geven tot verkeerde annotatie. Deze kunnen op de map gemakkelijk onderscheiden worden doordat ze zones van inconsistente en/of onlogische kleurcodering creëren op de map. Deze punten kunnen met een muisklik gemakkelijk gecontroleerd worden en ofwel verwijderd ofwel manueel geherannoteerd worden.
Resultaten
In april 2016 werd in ons centrum als eerste in België gestart met het uitvoeren van procedures met het nieuwe RHYTHMIA HDx-mappingsysteem. In juni 2017 werd de honderdste procedure verricht. Op het moment dat u dit artikel leest, zijn we de honderdvijftigste procedure gepasseerd. De data van de eerste honderd procedures werden retrospectief verzameld en geanalyseerd om een idee te krijgen van de performantie van het systeem.
De gemiddelde leeftijd van de patiënten was 61 ± 13 jaar en 58 % was mannelijk. Het grootste deel van de procedures waren redo-ablaties (n = 77) en werden uitgevoerd wegens atriale fibrillatie (n = 53; 80 % persistent) of atypische linkszijdige fluttercircuits (n = 13). In 52 % van de patiënten die vooraf reeds een pulmonaalvene-isolatie (PVI) ondergaan hadden, werd reconnectie van één of meerdere pulmonaalvenen (PV) vastgesteld (vooral t.h.v. de rechtszijdige PV), waarvoor aansluitend een herisolatie verricht werd. Bij de overige patiënten (zonder reconnectie) werden aanvullende lijnen getrokken in het linker en/of rechter atrium. In zes procedures werd een index-PVI uitgevoerd. Zeventien procedures werden gedaan in het kader van een ectopische atriale tachycardie, waarvan 6 rechtszijdig. Verder werden in het kader van de leercurve met het systeem ook procedures bij typische rechtszijdige atriale flutter (12 procedures), AVNRT (2 procedures), ventriculaire ectopiëen (2 procedures) en littekengerelateerde ventriculaire tachycardie (1 procedure) uitgevoerd.
De gemiddelde tijd voor het maken van een map bedroeg 9,2 ± 7,2 minuten bij een gemiddeld volume van 93,8 ± 42 ml in het rechter atrium en 13,5 ± 8,5 minuten bij een gemiddeld volume van 122,2 ± 41 ml in het linker atrium. In 31 procedures werd een map van zowel het linker als het rechter atrium gemaakt. In totaal werden gemiddeld 6,710 ± 5,758 EGMs geregistreerd en automatisch geannoteerd in het rechter atrium en 11,368 ± 8,397 EGMs in het linker atrium, op respectievelijk 484 ± 478 en 926 ± 815 hartslagen. Dit relateert tot 728,1 EGMs per minuut en 13,9 EGMs per hartslag in het rechter atrium en 857,6 EGMs per minuut en 12,4 EGMs per hartslag in het linker atrium.
De techniek bleek efficiënt en veilig te zijn. In 92 % van de procedures kon een succesvolle ablatie verricht worden.
Toepassingen
Focale atriale tachycardie (figuur 2)
Bij focale atriale tachycardie is RHYTHMIA HDx het uitgelezen elektroanatomische mappingsysteem, vooral in geval van moeilijk te induceren, nietonderhouden, multipele en/of hemodynamisch instabiele tachycardiëen.
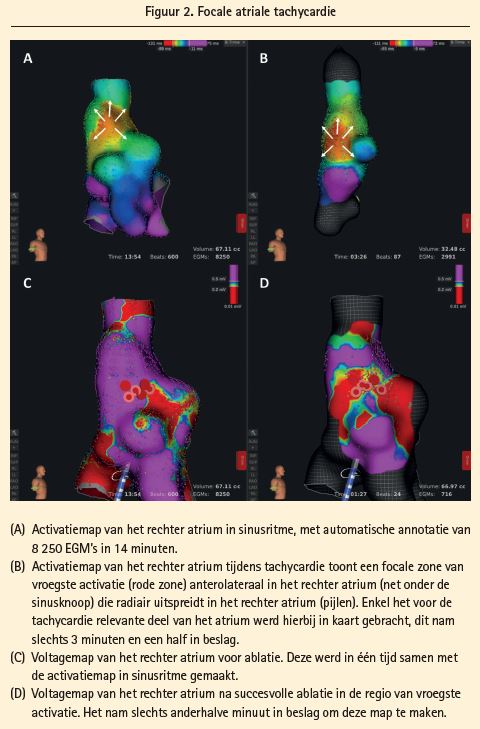
Door de snelheid van mapping kan op een korte tijdspanne reeds een accurate map van de tachycardie gemaakt worden. Indien er verschillende (bv. 3 of 4) tachycardiëen uitgelokt worden, kan er gemakkelijk telkens een nieuwe map gemaakt worden, zonder dat dit de proceduretijd met uren hoeft te verlengen.
De hoge resolutie van het systeem maakt het mogelijk om de zone van vroegste activatie heel scherp te definiëren, zodat het doelwit voor ablatie zeer nauwkeurig gemarkeerd kan worden. Soms is het zelfs mogelijk om onderliggende microre- entrycircuits te visualiseren.
Na inductie van de tachycardie gebruikt het systeem de eerste tien seconden om de gemiddelde cycluslengte te berekenen op basis van het activatiepatroon op de decapolaire referentiekatheter in de sinus coronarius7. Het systeem zal vervolgens automatisch 50 % van de cycluslengte van de tachycardie voor de referentie zetten en 50 % erna (dit kan tijdens de procedure aangepast worden). EGMs worden vervolgens automatisch geregistreerd en geannoteerd als ze voldoen aan de ingestelde acceptatiecriteria7: cycluslengtestabiliteit (bv. deviatie van 20 ms van de cycluslengte aanvaardbaar), stabiele locatie van de mappingelektrode op de Orion, stabiele relatieve timing tussen twee referentie- EGMs en respiratoire 'gating'.
Pulmonaalvene-isolatie bij voorkamerfibrillatie (figuur 3)
Index-pulmonaalvene-isolaties kunnen met en zonder hulp van een elektroanatomisch mappingsysteem (EAMs) verricht worden. Indien er gebruik gemaakt wordt van een single-shot-ablatietechniek zoals de cryoballon PVI dan is een EAMs strikt gezien niet noodzakelijk en kan er vooral op basis van fluoroscopie gewerkt worden. In geval van punt-perpunt- radiofrequente (RF) ablatie is een EAMs echter onontbeerlijk.
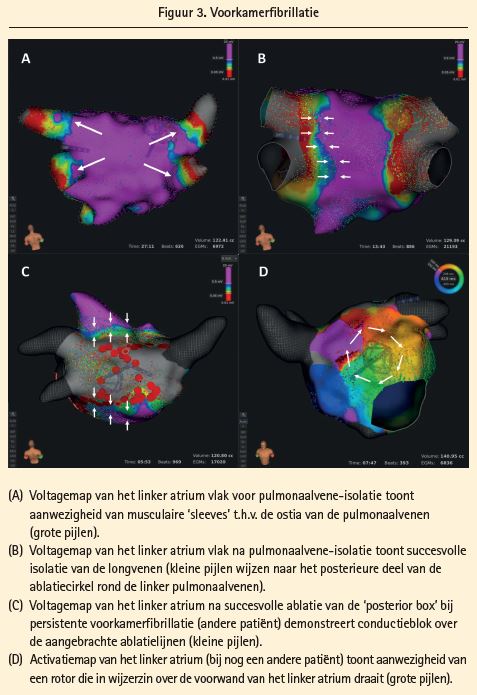
Klassiek werden de punt-per-punt-RF PVI's de afgelopen 2 decennia verricht met behulp van CARTO of EnSite-mappingsystemen, waarbij gebruikt gemaakt wordt van een multi-elektrode circulaire ('Lasso') katheter die sequentieel in de verschillende pulmonaalvenen gelegd wordt om het optreden van isolatie tijdens ablatie te beoordelen.
Echter, in vergelijking met de klassieke EAMs heeft het nieuwe RHYTHMIA HDx bij index-PVI enkele aantrekkelijke voordelen:
1) Anatomische accuraatheid. Zonder noodzaak voor fusie met een CT-scan kan op een tiental minuten een heel accurate map van het linker atrium verkregen worden. De hoge anatomische resolutie van de map is noodzakelijk gezien de grote interindividuele anatomische variatie tussen patiënten. Met name de 'ridge' tussen de linker pulmonaalvenen en het linker hartoor is een klassieke plaats waar reconnectie ontstaat bij inadequate ablatie en het meer in detail brengen van deze regio kan enkel bijdragen tot een meer succesvolle ablatie.
2) Detectie van PV-potentialen. Door de betere signaal-tot-ruisratio is het RHYTHMIA HDx-systeem gevoeliger om (na partiële ablatie) residuele PVpotentialen van lage amplitude te detecteren13. Bovendien laat het systeem toe om voor het eerst in de geschiedenis van de EAMs de musculaire 'sleeves' (spieruitlopers van de voorkamers in de pulmonaalvenen) te visualiseren. Dit is belangrijk omdat op deze plaatsen voorkamerfibrillatie ontstaat.
3) Detectie van rotors en extra-PV-triggers. Door de hoge resolutie en de snelheid van mappen is het gemakkelijker om mechanistische inzichten te verkrijgen in de aritmie en meer specifiek gerichte ablaties uit te voeren14.
4) Confirmatie van blok. De snelheid van mapping maakt dat het weinig tijd kost om na ablatie een 'remap' te maken. Door de hoge resolutie is het gemakkelijker om kleine 'gaps' in de ablatielijnen te detecteren en aanwezigheid van blok/ isolatie te confirmeren10.
Atypische linkszijdige voorkamerflutter (figuur 4)
Bij recidieve aritmie na voorgaande pulmonaalvene- isolaties worden geregeld atypische linkszijdige voorkamerflutters gedocumenteerd tijdens de redo-procedures, zeker indien er een onderliggend littekensubstraat aanwezig is in de voorkamers.
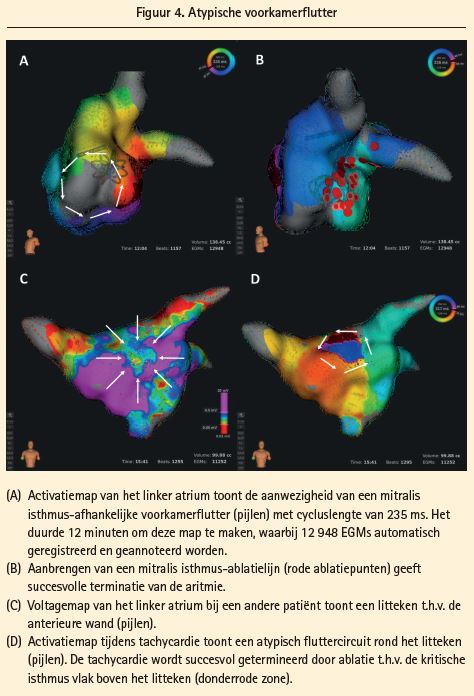
Door gebruik te maken van het RHYTHMIA HDx-systeem is het mogelijk om deze littekenzones mooi in detail te visualiseren9. Verder kan het systeem in deze littekenzones op zoek gaan naar re-entrycircuits met laag gevolteerde, langgerekte complexe gefractioneerde multicomponent-EGMs15-16, die door de klassieke EAMs ofwel moeilijk te detecteren zijn (door hun lage voltage) ofwel verkeerd geannoteerd worden (door de multipele componenten). Met behulp van het RHYTHMIA HDx-systeem is het nu mogelijk om meer dan 90 % van alle multicomponent-EGMs correct te annoteren (in tegenstelling tot ca. 70 % met andere multi-elektrodekatheters)9. Hierdoor is er ook geen noodzaak meer voor entrainment pacing (met risico dat de aritmie termineert of degenereert in een andere atriale tachycardie of fibrillatie, soms is er zelfs geen captuur in de littekenzones) ter bevestiging dat de ablatiekatheter t.h.v. het re-entrycircuit ligt.
Conclusie
High-definition mapping is een recente ontwikkeling binnen de elektroanatomische mapping systemen, waardoor het mogelijk is om op een geautomatiseerde wijze een nooit gezien aantal elektrogrammen op korte tijd te registreren en accuraat te annoteren. Dit geeft een enorme verbetering van de resolutie van de elektroanatomische map, waardoor een beter begrip van diverse aritmiëen en hun onderliggend substraat mogelijk wordt. Hierdoor kunnen de proceduretijden verkorten en verhogen de kansen op een succesvolle ablatie. Verdere gerandomiseerde gecontroleerde studies zijn echter nodig om de superioriteit van high-definition mapping aan te tonen in vergelijking met de huidige conventionele mappingtechnieken.
Referenties
- Giraud, G., Puech, P., Latour, H. The physiological electrical activity of Tawara's node and of His' bundle in man: Endocavitary electrocardiographic registration. Bull Acad Natl Med, 1960, 144, 363-366.
- Saoudi, N., Atallah, G., Kirkorian, G., Touboul, P. Catheter ablation of the atrial myocardium in human type I atrial flutter. Circulation, 1990, 81, 762-771.
- Earley, M.J., Showkathali, R., Alzetani, M., Kistler, P.M., Gupta, D., Abrams, D.J., et al. Radiofrequency ablation of arrhythmias guided by nonfluoroscopic catheter location: a prospective randomized trial. Eur Heart J, 2006, 27, 1223-1229.
- Jiang, Y., Farina, D., Bar-Tal, M., Dössel, O. An impedance based catheter positioning system for cardiac mapping and navigation. IEEE Trans Biomed Eng, 2009, 56, 1963-1970.
- Gepstein, L., Hayam, G., Ben-Haim, S.A. A novel method for nonfluoroscopic catheter-based electroanatomical mapping of the heart: In vitro and in vivo accuracy results. Circulation, 1997, 95, 1611-1622.
- Jones, D.G., McCready, J.W., Kaba, R.A., Ahsan, S.Y., Lyne, J.C., Wang, J., et al. A multipurpose spiral high-density mapping catheter: initial clinical experience in complex atrial arrhythmias. J Interv Card Electrophysiol, 2011, 31, 225-235.
- Mantziari, L., Butcher, C., Kontogeorgis, A., Panikker, S., Roy, K., Markides, V., et al. Utility of a novel rapid high-resolution mapping system in the catheter ablation of arrhythmias: An initial human experience of mapping the atria and the left ventricle. JACC: Clin Electrophysiol, 2015, 1(5), 411-420.
- Schaeffer, B., Hoffmann, B.A., Meyer, C., Akbulak, R.Ö., Moser, J., Jularic, M., et al. Characterization, mapping, and ablation of complex atrial tachycardia: initial experience with a novel method of ultra high-density 3D mapping. J Cardiovasc Electrophysiol, 2016, 27, 1139-1150.
- Anter, E., McElderry, T.H., Contreras-Valdes, F.M., Li, J., Tung, P., Leshem, E., et al. Evaluation of a novel high-resolution mapping technology for ablation of recurrent scar-related atrial tachycardias. Heart Rhythm, 2016, 13(10), 2048-2055.
- Nakagawa, H., Ikeda, A., Sharma, T., Lazzara, R., Jackman, W.M. Rapid high resolution electroanatomical mapping: Evaluation of a new system in a canine atrial linear lesion model. Circ Arrhythm Electrophysiol, 2012, 5, 417-424.
- Anter, E., Tschabrunn, C.M., Josephson, M.E. High-resolution mapping of scar-related atrial arrhythmias using smaller electrodes with closer interelectrode spacing. Circ Arrhythm Electrophysiol, 2015, 8, 537- 545.
- Bun, S.S., Laţcu, D.G., Delassi, T., Jamili, M.E., Amoura, A.A., Saoudi, N. Ultra-High-Definition Mapping of Atrial Arrhythmias. Circ J, 2016, 80(3), 579-586.
- Anter, E., Tschabrunn, C.M., Contreras-Valdes, F.M., Li, J., Josephson, M.E. Pulmonary vein isolation using the Rhythmia mapping system: Verification of intracardiac signals using the Orion mini-basket catheter. Heart Rhythm, 2015, 12, 1927-1934.
- Haissaguerre, M., Hocini, M., Denis, A., Shah, A.J., Komatsu, Y., Yamashita, S., et al. Driver domains in persistent atrial fibrillation. Circulation, 2014, 130, 530-538.
- Luther, V., Sikkel, M., Bennett, N., Guerrero, F., Leong, K., Qureshi, N., et al. Visualizing Localized Reentry With Ultra-High Density Mapping in Iatrogenic Atrial Tachycardia: Beware Pseudo-Reentry. Circ Arrhythm Electrophysiol, 2017, 10(4), e004724.
- Laţcu, D.G., Bun, S.S., Viera, F., Delassi, T., El Jamili, M., Al Amoura, A., et al. Selection of Critical Isthmus in Scar-Related Atrial Tachycardia Using a New Automated Ultrahigh Resolution Mapping System. Circ Arrhythm Electrophysiol, 2017, 10(1), e004510.
Aucun élément du site web ne peut être reproduit, modifié, diffusé, vendu, publié ou utilisé à des fins commerciales sans autorisation écrite préalable de l’éditeur. Il est également interdit de sauvegarder cette information par voie électronique ou de l’utiliser à des fins illégales.