Een greep uit de lezingen van: prof. dr. C. Steinwender, Kepler Universitäts Klinikum, Linz, Austria en dr. C. Garweg, UZ Leuven, Leuven, België
Draadloze pacingsystemen zijn een waardevol alternatief voor conventionele pacemakers met minder complicaties en met als voornaamste sterke punten de infectiereductie en het overwinnen van anatomische obstakels. De belangrijkste uitdagingen zijn het levenscyclusbeheer en het drukken van de kostprijs.
Introductie
De eerste pacemakers werden in België geplaatst in de jaren 50. Sindsdien is zowel de software als de hardware snel geëvolueerd. De ontwikkeling van atrioventriculaire stimulatie, de introductie van 'rate response' en resynchronisatietherapie - al dan niet in combinatie met een inwendige defibrillator - zijn de belangrijkste omwentelingen van de voorbije zeven decades. De voordelen van conventionele pacing zijn intussen goed gedocumenteerd. Het gebruik van een onderhuids geplaatst toestel en transveneuze draden gaat echter gepaard met een niet te onderschatten aantal complicaties, sommige zelfs levensbedreigend. In de FOLLOWPACE-studie vond men 12,4 % vroege complicaties (≤ 2 maanden na implantatie) en 9,2 % laattijdige complicaties, waarvan de meeste gerelateerd waren aan het gebruik van draden of pockethematomen.1 Met de plaatsing van de eerste draadloze pacemaker in 2015 in België, rijst de hoop om met eenzelfde efficiëntie een veiligere techniek te beheersen.
Draadloze pacemakers - Waar staan we nu?
Twee miniatuurpacemakers, NanostimTM (Abbott, voorheen St. Jude Medical) en MicraTM (Medtronic), kennen een klinische toepassing bij patiënten met nood aan eenkamerstimulatie (VVI). Door batterijproblemen bij Abbott/St. Jude Medical, is momenteel enkel de laatste commercieel beschikbaar. Beide pacemakers kunnen met een volledig stuurbaar systeem in de rechterventrikel ingeplant worden. Bij de MicraTM bestaat het toestel uit een capsule met kleine weerhaakjes, dat in de rechterventrikel wordt verankerd. De NanostimTM gebruikt een schroefsysteem. De implantatie gebeurt onder fluoroscopiegeleide via de rechterlies en vena cava inferior, al dan niet na opname van een veno- en ventriculogram.2
De capsules hebben alle moderne technologie aan boord die ook bij conventionele pacemakers beschikbaar zijn. Ze zijn compatibel met MRI (1,5-3 Tesla) en beschikken over een accelerometer en capturebeheer en zijn bestuurbaar op afstand. Een extra eigenschap is dat de toestellen bij het einde van de batterijlevensduur kunnen worden uitgezet om een tweede of zelfs derde capsule te implanteren. De batterijlevensduur wordt geschat op ongeveer 12 jaar.
Reddy et al. publiceerden de data van hun LEADLESS II-trial (NanoStimTM) in de New England Journal of Medicine in 2015. De draadloze pacemaker werd in 95,8 % van de patiënten succesvol geïmplanteerd. Ernstige complicaties traden op in 20 (6,7 %) van 300 implantaties. Als belangrijkste complicaties onthouden we dislocatie (5, 1,7 %), perforatie (4, 1,3 %) en oplopende drempels waarvoor vervanging was vereist (4, 1,3 %). Deze toestellen worden momenteel niet in de kliniek gebruikt tot de batterijproblemen zijn opgelost.3
Voor de MicraTM verschenen de resultaten van de hand van Reynolds et al. in de New England Journal of Medicine in 2016. Het implantatiesuccespercentage voor de totale populatie van 725 patiënten was 99,2 %. De efficiëntie van implantatie was zeer goed. 98,3% van de patiënten had lage en stabiele drempels. Hogere drempels ≤ 2V bij implantatie zakten bij de meeste patiënten tijdens de eerste maanden. Bij drempels > 2V bij een pulsduur van 0,24 ms moest het toestel gerepositioneerd worden.4, 5 Er traden 24 (2,69 %) majeure complicaties op tijdens de eerste 30 dagen na implantatie. De meeste hiervan waren gerelateerd aan de liespunctie (5, 069%) of perforatie (10, 1,38 %). Na twaalf maanden bleef 96 % van de patiënten vrij van complicaties. Er waren 48 % minder complicaties in vergelijking met een referentiegroep van patiënten met een conventionele pacemaker.6
De registratiestudie na goedkeuring van de MicraTM recruteerde 795 patiënten tussen juli 2015 en januari 2017. Deze studie toonde 99,6 % implantatiesucces door 149 implanteerders in 96 centra in 20 verschillende landen. Ook in onervaren handen lijkt de techniek dus zeker haalbaar. In tegenstelling tot de investigatiestudie hadden 73 patiënten voorheen een transveneuze pacemaker en 13 een ICD. Bij 20,9 % was er een belangrijke reden om geen transveneus systeem te plaatsen, bv. moeilijke veneuze toegang, voorgeschiedenis van infectie, behoud van de vene voor dialyse, trombose, kanker of kunstkleppen. De indicatie voor implantatie was voorkamerfibrillatie met bradycardie (57,7 %), AV-blok (14,7 %), syncope (14,1 %), sinusknoopziekte (8,0 %), een aantal andere indicaties zonder voorkamerfibrillatie (3,4 %) of niet gespecifieerd (2,1 %). De MicraTM werd preferentieel geïmplanteerd in het septum (52,1 %), RV-apex (39,3 %) en slechts in een minderheid in RVOT (1,9 %) of een andere positie (6,3 %). Vermoedelijk onder andere door verschuiven van de implantatielocatie van RV-apex naar septum waren er minder complicaties in de registratiestudie. Er traden 13 (1,51 %) majeure complicaties op tijdens de eerste 30 dagen na implantatie. De meeste hiervan gerelateerd aan de liespunctie (6, 0,75 %), naast perforatie (1, 0,13%) en dislocatie (1, 0,13 %). Hoogrisicopatiënten voor complicaties worden gedefinieerd als oude patiënten > 75 jaar, chronisch longlijden, vrouwen, laag BMI, ischemisch hartlijden en perorale steroïden.6, 7
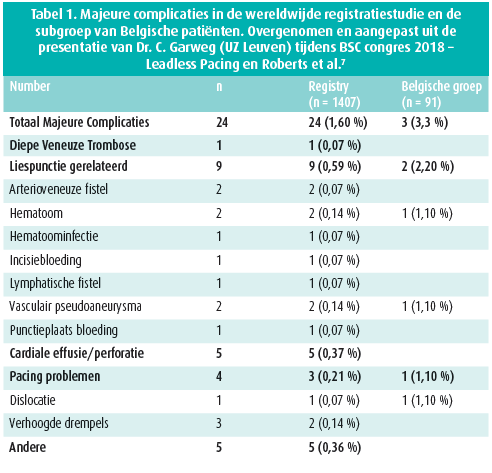
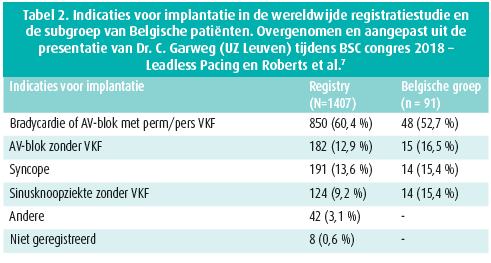
In België werden sinds juli 2015 al meer dan 220 MicraTM-toestellen geïmplanteerd in 15 actieve implantatiecentra. UZ Antwerpen, UCL en UZ Leuven namen deel aan de wereldwijde registratiestudie. In oktober 2017 bevatte deze 1 498 patiënten, waarvan 91 uit België met een gemiddelde leeftijd van 79,1 ± 9,7 jaar en een follow-up van 9,1 ± 6,2 maanden. Er waren 3 complicaties in de Belgische groep (1 lieshematoom, 1 pseudoaneurysma en 1 dislocatie). In tabel 1 en 2 zien we de indicatie- en complicatiepercentages van de registratiestudie op 31 oktober 2017 en de Belgische ervaring.
Draadloze pacemakers - Quo vadis?
Perspectief 1. Uitbreiding van indicaties
De enige klinisch toepassing is momenteel een eenkamerpacemaker (VVI) (figuur 1-1). Voorkamerfibrillatie met bradycardie en AV-blok is bijgevolg de belangrijkste indicatie voor een draadloos systeem. Dit beperkt zich echter tot 16 % van alle pacemakerindicaties. De grote aantallen patiënten met sinusritme met AV-blok (40 %), sinusknoopziekte (30 %) en sinusknoopziekte met AV-blok (10 %) worden druk onderzocht door de industrie. Bij sinusritme met AV-blok is er nood aan adequate detectie van sinusritme en synchronisatie met het ventriculair ritme. Bij sinusknoopziekte is een extra capsule met een licht gewijzigd verankeringsmechanisme vereist, noodzakelijk voor de dunnere musculatuur van het rechteratrium. Op middellange termijn verwachten we dus draadloze tweekamersystemen (figuur 1-2). De twee capsules moeten met elkaar kunnen communiceren met een lage energieconsumptie, maar met een hoge veiligheidsmarge voor interferentie. Dit blijkt moeilijker dan verwacht, maar wordt volop getest in diermodellen.
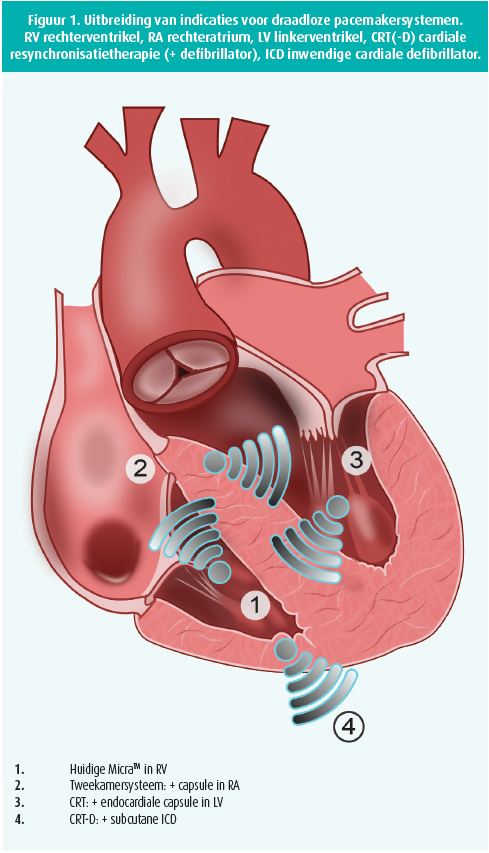
De volgende stap is draadloze resynchronisatietherapie (figuur 1-3). Dit vereist een links endocardiaal of epicardiaal ingeplant toestel. De communicatie tussen de rechts en links geïmplanteerde toestellen zou kunnen verbeteren door subcutaan ingeplante versterkers. Het WiSE-CRT-systeem (EBR Systems, Sunnyvale, California) werd ontwikkeld om de beperkingen van een positie in de sinus coronarius op te lossen. Zij gebruiken een conventioneel systeem in het rechterhart, in combinatie met een endocardiale capsule in de linkerventrikel die in verbinding staat met een subcutane ultrasound transmitter/batterij en aan de rechterzijde een conventioneel systeem. De SELECT-LV-studie toonde de klinische haalbaarheid in 35 patiënten om op deze manier synchrone biventriculaire pacing te bereiken.8
Tjong et al. publiceerden daarenboven in 2016 de eerste resultaten van een draadloze pacemaker (Boston Scientific) die gelinkt werd met een subcutane ICD om naast de klassieke VVI-mode ook antitachypacing af te leveren. Het concept werd succesvol aangetoond in een schaapmodel.9
Deze evoluties kunnen op termijn leiden tot een volledig draadloos CRT-D-systeem wat de morbiditeit door de transveneuze draden in deze populatie drastisch kan reduceren (figuur 1-4).
Perspectief 2. Reductie infectierisico
Infectie van implanteerbare toestellen lijkt een toenemend probleem te zijn. Kypta et al. toonden de mogelijkheid om een draadloos systeem te implanteren bij 6 pacemakerdependente patiënten met leadinfectie. Het draadloos systeem werd geïmplanteerd in dezelfde procedure of na korte overbrugging met temporaire pacemaker.10 Idealiter zou een draadloos systeem steeds in dezelfde procedure kunnen worden ingeplant om temporaire pacing te vermijden. De draadloze systemen hebben van nature minder infectierisico omdat er geen leads zijn, en ze daarnaast geen silicone of polyurethaan bevatten, maar louter uit een titanium capsule bestaan.
Perspectief 3. Toegangsproblemen voor transveneuze draden
Op termijn kunnen draadloze pacemakers wellicht ook gebruikt worden bij congenitale defecten of bij een biologische tricuspiedklep, waarbij transveneuze draden niet mogelijk of wenselijk zijn.
Perspectief 4. Levenscyclusbeheer
Het is minder duidelijk wat de toekomst hier zal brengen. Autopsie leerde ons dat de meeste draadloze toestellen volledig ingekapseld worden na implantatie. Er worden nieuwe extractiehulpmiddelen ontwikkeld die kunnen snijden of branden. Daarnaast zijn er experimenten om door lasering van de oppervlakte van de capsule migratie van fibroblasten te verhinderen, al vreest men hierdoor een groter infectierisico.
Een tweede mogelijkheid is om de batterijlevensduur te verlengen door elektromagnetische, piezo-elektrische of elektrostatische transducers die de beweging van het hart, drukgradiënten of bloedstroming omzetten in energie of door transthoracaal te herladen. De wetenschap hierover beperkt zich voorlopig tot technische haalbaarheid ervan en werd nog niet in vivo getest.11
Perspectief 5. Kosten en terugbetaling
De huidige prijs van draadloze pacemakers is twee tot drie keer hoger dan van conventionele pacing en er is momenteel geen specifieke terugbetaling voorzien. Bovendien worstelt men met de vraag wat het businessmodel zal worden als de toestellen 20 jaar werken, bv. leasing in plaats van aankoop.
Perspectief 6. Wat ligt er achter de horizon?
Toen Antonio Meucci de telefoon uitvond midden jaren 1850, kon hij niet vermoeden dat 150 jaar later bijna de hele wereld draadloos verbonden zou zijn. De toekomst van het pacen is ongetwijfeld ook draadloos met als voornaamste sterkte punten, de infectiereductie en het overwinnen van anatomische obstakels. In de nabije toekomst worden naast VVI-systemen ook VVD(R), AAI(R) en later ook DDD(R) en CRT-P/D verwacht. De belangrijkste uitdagingen zijn het levenscyclusbeheer en het drukken van de kostprijs.
Conclusie
Zoals met elke disruptieve technologie blijven een aantal vragen onbeantwoord. Gerandomiseerd onderzoek kan helpen om uit te maken of draadloze pacing werkelijk veiliger en even efficiënt is als conventionele pacing. De toekomst ziet er echter veelbelovend uit.
Références
- Udo, E.O., Zuithoff, N.P., van Hemel, N.M., de Cock, C.C., Hendriks, T., Doevendans, P.A., et al. Incidence and predictors of short- and long-term complications in pacemaker therapy: the FOLLOWPACE study. Heart rhythm, 2012, 9(5), 728-735.
- Kancharla, K., Deshmukh, A.J., Friedman, P.A. Leadless Pacemakers - Implant, Explant and Long-Term Safety and Efficacy Data. J Atr Fibrill, 2017, 10 (2), 1581.
- Reddy, V.Y., Exner, D.V., Cantillon, D.J., Doshi, R., Bunch, T.J., Tomassoni, G.F. et al. Percutaneous Implantation of an Entirely Intracardiac Leadless Pacemaker. N Engl J Med, 2015, 373 (12), 1125-1135.
- Piccini, J.P., Stromberg, K., Jackson, K.P., Laager, V., Duray, G.Z., El-Chami, M., et al. Long-term outcomes in leadless Micra transcatheter pacemakers with elevated thresholds at implantation: Results from the Micra Transcatheter Pacing System Global Clinical Trial. Heart rhythm, 2017, 14 (5), 685-691.
- Reynolds, D., Duray, G.Z., Omar, R., Soejima, K., Neuzil, P., Zhang, S., et al. A Leadless Intracardiac Transcatheter Pacing System. N Engl J Med, 2016, 374 (6), 533-541.
- Duray, G.Z., Ritter, P., El-Chami, M., Narasimhan, C., Omar, R., Tolosana, J.M., et al. Long-term performance of a transcatheter pacing system: 12-Month results from the Micra Transcatheter Pacing Study. Heart rhythm, 2017, 14 (5), 702-709.
- Roberts, P.R., Clementy, N., Al Samadi, F., Garweg, C., Martinez-Sande, J.L., Iacopino, S., et al. A leadless pacemaker in the real-world setting: The Micra Transcatheter Pacing System Post-Approval Registry. Heart rhythm, 2017, 14 (9), 1375-1379.
- Reddy, V.Y., Miller, M.A., Neuzil, P., Sogaard, P., Butter, C., Seifert, M., et al. Cardiac Resynchronization Therapy With Wireless Left Ventricular Endocardial Pacing: The SELECT-LV Study. JACC, 2017, 69 (17), 2119-2129.
- Tjong, F.V.Y., Brouwer, T.F., Kooiman, K.M., Smeding, L., Koop, B., Soltis, B., et al. Communicating Antitachycardia Pacing-Enabled Leadless Pacemaker and Subcutaneous Implantable Defibrillator. JACC, 2016, 67 (15), 1865-1866.
- Kypta, A., Blessberger, H., Kammler, J., Lambert, T., Lichtenauer, M., Brandstaetter, W., et al. Leadless Cardiac Pacemaker Implantation After Lead Extraction in Patients With Severe Device Infection. J Cardiovascul Electrophysiol, 2016, 27 (9), 1067-1071.
- Pfenniger A, Jonsson M, Zurbuchen A, Koch VM, Vogel R. Energy harvesting from the cardiovascular system, or how to get a little help from yourself. Ann Biomed Eng, 2013, 41 (11), 2248-2263.
Referenties
- Udo, E.O., Zuithoff, N.P., van Hemel, N.M., de Cock, C.C., Hendriks, T., Doevendans, P.A., et al. Incidence and predictors of short- and long-term complications in pacemaker therapy: the FOLLOWPACE study. Heart rhythm, 2012, 9(5), 728-735.
- Kancharla, K., Deshmukh, A.J., Friedman, P.A. Leadless Pacemakers - Implant, Explant and Long-Term Safety and Efficacy Data. J Atr Fibrill, 2017, 10 (2), 1581.
- Reddy, V.Y., Exner, D.V., Cantillon, D.J., Doshi, R., Bunch, T.J., Tomassoni, G.F. et al. Percutaneous Implantation of an Entirely Intracardiac Leadless Pacemaker. N Engl J Med, 2015, 373 (12), 1125-1135.
- Piccini, J.P., Stromberg, K., Jackson, K.P., Laager, V., Duray, G.Z., El-Chami, M., et al. Long-term outcomes in leadless Micra transcatheter pacemakers with elevated thresholds at implantation: Results from the Micra Transcatheter Pacing System Global Clinical Trial. Heart rhythm, 2017, 14 (5), 685-691.
- Reynolds, D., Duray, G.Z., Omar, R., Soejima, K., Neuzil, P., Zhang, S., et al. A Leadless Intracardiac Transcatheter Pacing System. N Engl J Med, 2016, 374 (6), 533-541.
- Duray, G.Z., Ritter, P., El-Chami, M., Narasimhan, C., Omar, R., Tolosana, J.M., et al. Long-term performance of a transcatheter pacing system: 12-Month results from the Micra Transcatheter Pacing Study. Heart rhythm, 2017, 14 (5), 702-709.
- Roberts, P.R., Clementy, N., Al Samadi, F., Garweg, C., Martinez-Sande, J.L., Iacopino, S., et al. A leadless pacemaker in the real-world setting: The Micra Transcatheter Pacing System Post-Approval Registry. Heart rhythm, 2017, 14 (9), 1375-1379.
- Reddy, V.Y., Miller, M.A., Neuzil, P., Sogaard, P., Butter, C., Seifert, M., et al. Cardiac Resynchronization Therapy With Wireless Left Ventricular Endocardial Pacing: The SELECT-LV Study. JACC, 2017, 69 (17), 2119-2129.
- Tjong, F.V.Y., Brouwer, T.F., Kooiman, K.M., Smeding, L., Koop, B., Soltis, B., et al. Communicating Antitachycardia Pacing-Enabled Leadless Pacemaker and Subcutaneous Implantable Defibrillator. JACC, 2016, 67 (15), 1865-1866.
- Kypta, A., Blessberger, H., Kammler, J., Lambert, T., Lichtenauer, M., Brandstaetter, W., et al. Leadless Cardiac Pacemaker Implantation After Lead Extraction in Patients With Severe Device Infection. J Cardiovascul Electrophysiol, 2016, 27 (9), 1067-1071.
- Pfenniger A, Jonsson M, Zurbuchen A, Koch VM, Vogel R. Energy harvesting from the cardiovascular system, or how to get a little help from yourself. Ann Biomed Eng, 2013, 41 (11), 2248-2263.
Aucun élément du site web ne peut être reproduit, modifié, diffusé, vendu, publié ou utilisé à des fins commerciales sans autorisation écrite préalable de l’éditeur. Il est également interdit de sauvegarder cette information par voie électronique ou de l’utiliser à des fins illégales.