Waarom tripeltherapie?
De patiënt met voorkamerfibrillatie die een coronaire interventie moet ondergaan is géén zeldzaamheid in onze dagelijkse praktijk. De keuze voor de meest optimale antitrombotische therapie voor deze patiënten is jammer genoeg helemaal niet eenvoudig. Hoe balanceer je een optimale trombotische en embolische bescherming met een zo laag mogelijk bloedingsrisico? Voor beroertepreventie bij VKF is een vitamine K-antagonist (VKA) of een van de directe orale anticoagulantia (DOAC) nodig. Acetylsalicylzuur of dubbele antiplaatjestherapie (DAPT) is hiervoor ongeschikt. Het omgekeerde geldt voor de preventie van stenttrombose of een nieuw coronair atherotrombotisch probleem na stentimplantatie of een acuut coronair syndroom. Het gevolg? De meeste patiënten met VKF die een coronaire interventie ondergaan, hebben in theorie een combinatie van orale anticoagulantia mét DAPT nodig, vaak tripeltherapie genoemd (TT). Het behoeft geen betoog dat dit uiteraard hun risico op bloedingscomplicaties significant verhoogt.
Dé gordiaanse knoop die ontward moet worden bij TT is dat vaak de patiënten met het hoogste risico op een bloeding ook het grootste risico op een beroerte of stenttrombose hebben. Dat is zeker bij ouderen het geval. Een minimale combinatie zonder acetylsalicylzuur en met een lage dosis DOAC kan bij een dergelijke hoogrisicopatiënt dan wel verleidelijk zijn om geen bloeding te veroorzaken, maar het stelt deze patiënt wel mogelijk bloot aan een onacceptabel hoog risico op een beroerte of stenttrombose. Bij het afwegen van alle mogelijke antitrombotische combinaties is het ontzettend belangrijk om zich te realiseren dat dit altijd een hoogst individuele overweging moet zijn. Niet alleen de CHA2DS2VASc- of HAS-BLED-scores spelen hier bij een rol, ook het risico op stenttrombose of andere nieuwe coronaire events bepalen het verdere beleid, en dat gebeurt bij voorkeur in samenspraak met de interventiecardioloog.
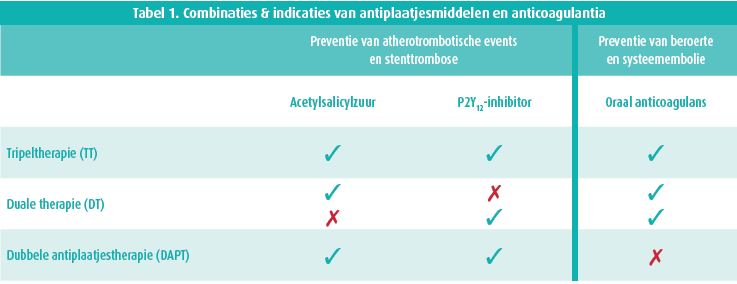
TT houdt meestal een combinatie van een lage dosis acetylsalicylzuur plus clopidogrel in, bovenop een anticoagulans. Belangrijk is om duale therapie (DT, één antiplaatjesmiddel plus anticoagulans) niet te verwarren met dubbele antiplaatjestherapie (DAPT, acetylsalicylzuur plus een P2Y12-inhibitor zoals clopidogrel, ticagrelor of prasugrel) (tabel 1). DT kan dan ook bestaan uit een oraal anticoagulans (OAC) met ofwel acetylsalicylzuur of een P2Y12-inhibitor zijn. Bij patiënten met VKF gaat de voorkeur voor OAC doorgaans uit naar een directe OAC (DOAC) eerder dan een vitamine K-antagonist, zelfs voor patiënten met een stabiele INR.1 Na PIONEER AF-PCI2 en RE-DUAL PCI3 hebben we nu met AUGUSTUS4 een derde TT-studie met een directe orale anticoagulans die meer licht werpt op de 'ideale' antitrombotische strategie voor deze steeds groter wordende populatie. PIONEER AF-PCI (n = 2124) en RE-DUAL PCI (n = 2725) toonden, niet geheel onverwacht, al duidelijk aan dat bij PCI-patiënten DT met een DOAC plus clopidogrel minder bloedingen veroorzaakt dan TT met een VKA, clopidogrel én acetylsalicylzuur.2, 3 Wat beide studies met andere woorden niet leerden is of de reductie in bloedingen te wijten was aan het weglaten van acetylsalicylzuur, het gebruik van een DOAC in plaats van een VKA, of een combinatie van beide factoren. De referentiearm was namelijk telkens TT met de klassieke combinatie VKA+clopidogrel+acetylsalicylzuur, die eigenlijk reeds vooraf inferieur bevonden werd tegenover DT met enkel VKA en clopidogrel in de WOEST-studie.5 Er was bovendien geen significante toename van trombotische of embolische complicaties na het weglaten van acetylsalicylzuur, maar het is belangrijk te onthouden dat de beperkte grootte van beide studies en het lage aantal trombotische events eigenlijk niet toelaten om definitieve conclusies te trekken, zelfs wanneer beide studies samen geanalyseerd worden.6
AUGUSTUS: primus inter pares
AUGUSTUS verschilt op enkele essentiële vlakken van de twee vorige TT-studies met een DOAC (tabel 2). Ten eerste de grootte: AUGUSTUS is bijna even groot als PIONEER en RE-DUAL samen. In tegenstelling tot zowel PIONEER als RE-DUAL, die enkel PCI-patiënten bestudeerden, werden in AUGUSTUS ook ACS-patiënten die medicamenteus behandeld werden gerandomiseerd. Zoals in RE-DUAL, maar in tegenstelling tot PIONEER, werd in AUGUSTUS enkel de 'evidence-based medicine' dosis van DOAC gebruikt die in de VKF-studies bewezen effectief was voor beroertepreventie; in PIONEER werd zowel 2 x 2,5 mg (de COMPASS-dosis) als 1 x 15 mg rivaroxaban getest, maar niet de 20 mg-dosis zoals deze werd gebruikt in ROCKET-AF. Enkel patiënten met een flink verminderde nierfunctie (slechts 10 % van de populatie) kregen 2 x 2,5 mg apixaban in AUGUSTUS, alle andere kregen de standaarddosis van 2 x 5 mg. Een ander belangrijk verschil is dat voor de eerste maal acetylsalicylzuur dubbelblind vergeleken werd met placebo. Dit betekent dat AUGUSTUS in essentie de enige DOAC-TT-studie is waarin de 'winnende' DT-combinatie (VKA+clopidogrel) uit de WOEST-studie rechtstreeks vergeleken werd met DT met een DOAC.5 Ten slotte lag het primair eindpunt van AUGUSTUS op 6 maanden, vergeleken met 1 jaar voor de twee andere studies. De meeste patiënten kregen clopidogrel als P2Y12-inhibitor in de drie studies.

AUGUSTUS: de resultaten
Zoals de twee vorige DOAC-TT-studies focust AUGUSTUS voornamelijk op ernstige bloedingscomplicaties. Majeure bloedingen waren significant lager met apixaban (10,5 %), dan met VKA (14,7 %, hazard ratio 0,69, 0,58-0,81), en dit bleek onafhankelijk van de antiplaatjestherapieën. De resultaten van AUGUSTUS tonen dan ook voor de eerste maal zwart op wit aan dat een volledige 'beroertepreventieve' dosis NOAC tot significant minder bloedingen leidt dan een VKA (INR 2-3) bij patiënten met VKF en een PCI of ACS, én dat dit onafhankelijk van eventuele bijkomende antiplaatjestherapie is. Hoewel het verschil niet significant was, werden ook bijna drie maal meer intracraniële bloedingen (0,6 % vs. 0,2 %) en tweemaal meer beroertes (2,4 % vs. 1,2 % met apixaban) waargenomen bij patiënten op VKA. Dat bevestigt eerdere observaties met apixaban bij 'gewone' VKF-patiënten in de ARISTOTLE-studie.7 Apixaban leidde in AUGUSTUS bovendien niet tot meer myocardinfarcten, stenttromboses of urgente revascularisaties vergeleken met VKA, maar wel tot significant minder hospitalisaties (-17 %).
De resultaten in de dubbelblind gerandomiseerde armen met versus zonder acetylsalicylzuur zijn op zijn minst even intrigerend. Zonder acetylsalicylzuur waren er significant minder bloedingen dan met (9,0 % vs. 16,1 %). AUGUSTUS is daarmee de eerste en enige DOAC-studie die prospectief de gunstige resultaten met een acetylsalicylzuurloze therapie in de WOEST-studie bevestigt én vertaalt naar het DOAC-universum. Het risico op overlijden of hospitalisatie was evenwel vergelijkbaar tussen de twee armen, hoewel ook deze grote TT-studie niet voldoende krachtig was om hierover een definitief oordeel te vellen. Het aantal stenttromboses was overigens laag in AUGUSTUS (< 1 %), en niet significant verschillend tussen acetylsalicylzuur en placebo. Niettemin was het aantal van gevallen met stenttrombose numeriek wel iets hoger zonder (0,9 %) dan met acetylsalicylzuur (0,5 %).
Samen genomen was de incidentie van majeure en klinisch relevante bloeding het laagst bij patiënten op apixaban en placebo (7,3 %) en het hoogst bij deze op VKA mét acetylsalicylzuur (18,7 %). Het aantal overlijdens en hospitalisaties toonde eenzelfde patroon: 22 % voor apixaban zonder acetylsalicylzuur, versus 27,5 % voor VKA plus acetylsalicylzuur. Het valt overigens op dat voor beide eindpunten de curves vrij snel na randomisatie duidelijk en substantieel divergeren: de grootste winst voor zowel apixaban vs. VKA als zonder vs. met acetylsalicylzuur valt voornamelijk in de eerste twee maanden na randomisatie te rapen.
Patiënten met een ACS die medicamenteus conservatief behandeld worden, hebben een erg hoog risico op nieuwe atherotrombotische complicaties. Deze patiënten zijn vaak ouder of fragiel en hebben meer comorbiditeit, wat hen ook gevoeliger maakt voor bloedingscomplicaties. AUGUSTUS toont nu voor de eerste (en enige) keer aan dat apixaban plus clopidogrel ook minder bloedingen veroorzaakt dan combinaties met VKA bij deze vaak moeilijk te behandelen patiëntengroep.
Wat nu?
1 Geen VKA maar DOAC voor allen
Na PIONEER en RE-DUAL geeft AUGUSTUS de ultieme doodsteek aan het VKA-keizerrijk voor VKF bij PCI-patiënten. Apixan is nu ook het enige DOAC met evidentie voor medicamenteus behandelde ACS-patiënten. Het is duidelijk dat er nu geen enkele reden meer is om een VKA te verkiezen bij DT of TT, tenzij uiteraard bij situaties waarin een DOAC niet geïndiceerd is, zoals na een mechanische kunstklep of bij dialyse.
De vraag welke dosis van iedere DOAC dan bij TT of DT best gebruikt wordt, is moeilijker te beantwoorden. Er is namelijk géén evidentie voor het relatief beroertepreventief effect van een lage dosis versus standaarddosis DOAC bij patiënten op één of meer antiplaatjesmiddelen. Observationele studies suggereren dat lagergedoseerde DOAC het risico op beroerte kunnen verhogen, in afwezigheid van nierinsufficiëntie.8 Mogelijk is een lagere dosis DOAC in afwezigheid van acetylsalicylzuur bovendien minder veilig wat betreft het risico op myocardinfarct en stenttrombose, wat gesuggereerd wordt door een numerieke toename van deze events in de acetylsalicylzuurloze 110 mg-dabigatranarm in RE-DUAL.3
Met andere woorden: ondanks de drie TT-studies blijft er onduidelijkheid over de optimale DOAC-dosis, en lijkt een pragmatische en individuele benadering van de PCI-patiënt met VKF aangewezen. Bij patiënten met een aanvaardbaar laag bloedingsrisico is het aangewezen om een normaal gedoseerde DOAC voor te schrijven; hiervoor is soliede evidentie voor zowel dabigatran (in beide doses) als apixaban.3, 4 Patiënten met een erg hoog bloedingsrisico kunnen dan weer baat hebben bij rivaroxaban in gereduceerde dosis, toch vergeleken met VKA,2 al is het niet aangetoond of 15 mg rivaroxaban überhaupt voldoende beroertepreventief werkt in afwezigheid van nierinsufficiëntie én/of 15 mg wel tot minder bloedingen leidt dan 20 mg in combinatie met clopidogrel.
2 Géén acetylsalicylzuur meer
AUGUSTUS toont voor het eerst op rigoureuze en prospectieve wijze de nefaste impact van acetylsalicylzuur op het bloedingsrisico van patiënten op een DOAC aan. Samen met de evidentie van de acetylsalicylzuurloze armen uit PIONEER en RE-DUAL is het nu na AUGUSTUS wel glashelder dat DT zonder acetylsalicylzuur steevast te verkiezen valt boven TT als standaard voor PCI-patiënten met VKF. Toch is het niet zozeer de vraag of acetylsalicylzuur nog thuishoort in de antitrombotische cocktail van deze patiënten, maar eerder wanneer het een goed moment is om acetylsalicylzuur te stoppen? Het is belangrijk om te onthouden dat patiënten in AUGUSTUS wel degelijk een korte tijd acetylsalicylzuur kregen na hun PCI of ACS. De mediane tijd tussen de PCI-procedure en randomizatie in AUGUSTUS was 6 dagen; tot dan kregen de meeste patiënten gewoon acetylsalicylzuur verder. Lage dosis acetylsalicylzuur bij en net na een coronaire interventie of acuut syndroom blijft de standaard, tenminste in de vroege acute fase.
Bij patiënten met een vrij laag atherotrombotisch risico kan op basis van AUGUSTUS en de eerdere DOAC-studies acetylsalicylzuur wel erg vroegtijdig gestopt worden. Onze standaardbenadering bij TT/DT is om acetylsalicylzuur bij ontslag te stoppen, wetende dat het antiplaatjeseffect nog meerdere dagen verder werkt. Een standaard-TT-behandeling voor één maand (en op veel plaatsen flink langer) mag dan wel aanlokkelijk veilig lijken, de snel divergerende curves vroeg na randomisatie in AUGUSTUS met een onmiddellijk voordeel in bloedingsrisico pleiten hier eigenlijk tegen.
Een kleine waarschuwing voor patiënten met een erg hoog trombotisch risico is echter wel op zijn plaats. Na complexe PCI bijvoorbeeld, eventueel voor een ACS, kan het toch beter zijn de acetylsalicylzuur niet te vroeg te stoppen. Ook hiervoor is weinig evidentie, en staat een pragmatisch aanpak in samenspraak met de interventiecardioloog centraal. Het blijft evenwel steeds belangrijk alles in het juiste perspectief te zien: toch acetylsalicylzuur geven bij hoogrisicopatiënten zal per vermeden stenttrombose gepaard gaan met 15 extra majeure bloedingscomplicaties. Dat is toch wel een flinke prijs om te betalen. En daarom blijft het belangrijk om héél goed te overwegen bij welke patiënt je acetylsalicylzuur überhaupt nog wil geven na ontslag, en om na te gaan of het sop de kolen waard is.
Het type van P2Y12-inhibitor is ook belangrijk bij het zoeken naar de beste strategie voor de individuele patiënt. Clopidogrel werkt namelijk onvoldoende bij 40 % van de patiënten, en dan kan monotherapie zonder acetylsalicylzuur mogelijk gepaard gaan met een onacceptabel hoog trombotisch risico, zelfs onder een DOAC. Hoewel wij regelmatig het antiplaatjeseffect van clopidogrel controleren in de setting van TT/DT, is hier eigenlijk géén evidentie voor. Ticagrelor in DT kan in dit geval een alternatief bieden voor TT: omdat het antiplaatjeseffect van ticagrelor meer uitgesproken en vooral véél minder variabel is, lijkt het bij ticagrelor altijd beter acetylsalicylzuur heel vroeg te stoppen voor zo goed als alle patiënten op een NOAC.9 Buiten 'label', terugbetaling of enige evidentie kan hier eventueel ook een rol zijn weggelegd voor ticagrelor 60 mg tweemaal daags, maar dit wordt best verder bestudeerd in klinische studies.
Besluit
AUGUSTUS is de kers op de taart van de TT-studies. Het velt een definitief oordeel over het mechanisme van reductie in bloedingsrisico: zowel het weglaten van acetylsalicylzuur, als kiezen voor een DOAC krijgen de voorkeur. De standaardbehandeling voor PCI- en/of ACS-patiënten met VKF is daarom nu manifest een DOAC plus P2Y12-inhibitor. Dat betekent overigens dat er geen reden meer is om te spreken van tripeltherapie, het is tijd om over te stappen op de term duale therapie. Couranter gebruik van deze term maakt dat artsen zich zullen realiseren dat TT eerder de uitzondering moet zijn, en DT de norm. TT is uiteraard nog mogelijk en in welbepaalde gevallen wenselijk, maar de reden om acetylsalicylzuur niet weg te laten moet goed overwogen worden én wordt bij voorkeur ook goed gecommuniceerd aan de patiënt in een 'shared decision'-discussie, én aan het zorgteam en de huisarts.
Referenties
- Kerneis, M., Yee, M.K., Mehran, R., Nafee, T., Bode, C., Halperin, J.L., et al. Association of International Normalized Ratio Stability and Bleeding Outcomes Among Atrial Fibrillation Patients Undergoing Percutaneous Coronary Intervention. Circ Cardiovasc Interv, 2019, 12 (2), e007124.
- Gibson, C.M., Mehran, R., Bode, C., Halperin, J., Verheugt, F.W., Wildgoose, P. et al. Prevention of Bleeding in Patients with Atrial Fibrillation Undergoing PCI. N Engl J Med, 2016, 375 (25), 2423-2434.
- Cannon, C.P., Bhatt, D.L., Oldgren, J., Lip, G.Y.H., Ellis, S.G., Kimura, T., et al. Committee R-DPS, Investigators. Dual Antithrombotic Therapy with Dabigatran after PCI in Atrial Fibrillation. N Engl J Med, 2017, 377 (16), 1513-1524.
- Lopes, R.D., Heizer, G., Aronson, R., Vora, A.N., Massaro, T., Mehran, R. et al. Antithrombotic Therapy after Acute Coronary Syndrome or PCI in Atrial Fibrillation. N Engl J Med, 2019, [E-pub before print].
- Dewilde, W.J., Oirbans, T., Verheugt, F.W., Kelder, J.C., De Smet, B.J., Herrman, J.P. et al. Use of clopidogrel with or without aspirin in patients taking oral anticoagulant therapy and undergoing percutaneous coronary intervention: an open-label, randomised, controlled trial. Lancet, 2013, 381 (9872), 1107-1115.
- Chi, G., Kerneis, M., Kalayci, A., Liu, Y., Mehran, R., Bode, C. et al. Safety and efficacy of non-vitamin K oral anticoagulant for atrial fibrillation patients after percutaneous coronary intervention: A bivariate analysis of the PIONEER AF-PCI and RE-DUAL PCI trial. Am Heart J, 2018, 203, 17-24.
- Alexander, J.H., Lopes, R.D., Thomas, L., Alings, M., Atar, D., Aylward, P., et al. Apixaban vs. warfarin with concomitant aspirin in patients with atrial fibrillation: insights from the ARISTOTLE trial. Eur Heart J, 2014, 35 (4), 224-232.
- Yao, X., Shah, N.D., Sangaralingham, L.R., Gersh, B.J., Noseworthy, P.A. Non-Vitamin K Antagonist Oral Anticoagulant Dosing in Patients With Atrial Fibrillation and Renal Dysfunction. J Am Coll Cardiol, 2017, 69 (23), 2779-2790.
- Oldgren, J., Steg, P.G., Hohnloser, S.H., Lip, G.Y.H., Kimura, T., Nordaby, M. et al. Dabigatran dual therapy with ticagrelor or clopidogrel after percutaneous coronary intervention in atrial fibrillation patients with or without acute coronary syndrome: a subgroup analysis from the RE-DUAL PCI trial. Eur Heart J, 2019, [Epub ahead of print].
Aucun élément du site web ne peut être reproduit, modifié, diffusé, vendu, publié ou utilisé à des fins commerciales sans autorisation écrite préalable de l’éditeur. Il est également interdit de sauvegarder cette information par voie électronique ou de l’utiliser à des fins illégales.