ESC-congres 2020
Symposiumverslag
Inleiding
Op het recente congres van de European Society of Cardiology (ESC) werden onder meer de nieuwe richtlijnen omtrent voorkamerfibrillatie (VKF) gepresenteerd. Naast vernieuwde aanbevelingen aangaande de diagnostiek en aanpak, werd ook het belang van een geïntegreerde en patiëntgeoriënteerde aanpak onderstreept. Zo ook in de sessie 'Anticoagulation management in non-valvular atrial fibrillation: delivering integrated patient-centred care' waarvan dit artikel verslag maakt. De sprekers waren Jan Steffel (Zürich, Zwitserland), Tatjana Potpara (Belgrado, Servië) en Hein Heidbuchel (Antwerpen, België). 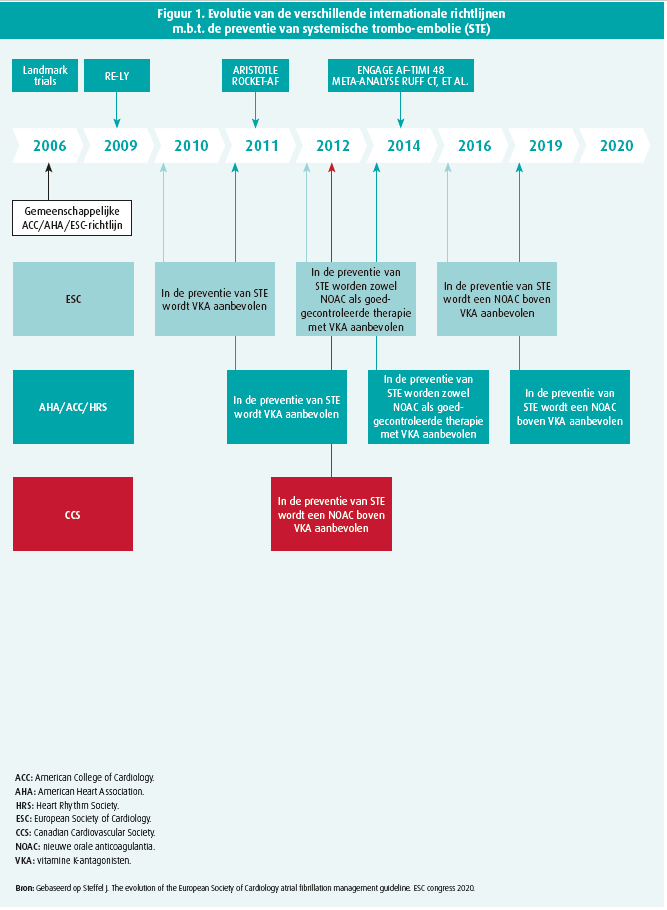
De evolutie van de ESC-richtlijnen omtrent voorkamerfibrillatie
Prof. J. Steffel
De laatste keer dat American College of Cardiology (ACC), American Heart Association (AHA) en European Society of Cardiology (ESC) een gezamenlijke richtlijn publiceerden over voorkamerfibrillatie (VKF) was in 2006.1 Hoewel dit toen een belangrijke richtlijn was, is er in tussentijd heel wat veranderd. Zo luidde de RE-LY-trial in 2009 het tijdperk van de nieuwe orale anticoagulantia (NOAC) in.2 Dabigatran bleek hierin een evenwaardig, tot zelfs een beter alternatief voor de vitamine K-antagonisten (VKA) in de preventie van systemische tromboembolie (STE) bij patiënten met een VKF. Een eerste update van de Europese VKF-richtlijnen verscheen in 2010, waarin dabigatran (op dat moment de enige NOAC) voor het eerst werd vermeld.3 Het product kreeg toen nog geen sterke aanbeveling, terwijl het gebruik van VKA nog steeds als de gouden standaard werd gezien. Bij het verschijnen van deze richtlijn was het al duidelijk dat de resultaten van enkele belangrijke studies zouden volgen, met name de ARISTOTLE-trial en ROCKET-AF-trial.4, 5 Na publicatie van deze trials werd in 2012 een nieuwe versie van de Europese richtlijnen gepubliceerd.6 Het stroomdiagram voor de aanpak van VKF leek toen voor het eerst op het stroomdiagram uit de richtlijn van 2016. Zo werd voor het eerst een onderscheid gemaakt tussen valvulaire en non-valvulaire VKF. Ook de indicatie voor orale anticoagulantia (OAC) werd voor het eerst gekoppeld aan de CHA2Ds2-VASc-score. Het gebruik van VKA werd in deze richtlijn nog als evenwaardig beschouwd aan het gebruik van NOAC, in tegenstelling tot de Canadese richtlijnen, die het gebruik van NOAC reeds verkozen boven het gebruik van VKA.
In 2014 verscheen vervolgens de ENGAGE AF-TIMI 48-trial, alsook een belangrijke vergelijkende meta-analyse van Christopher Ruff.7, 8 Hieruit bleek dat het gebruik van NOAC t.o.v. het gebruik van VKA aanleiding gaf tot een relatieve risicoreductie op een beroerte van 19 % (RR 0,81, 95 % BI: 0,73-0,91; P < 0,0001). Dat terwijl men geen stijging kon weerhouden in de incidentie van majeure bloedingen. Sterker zelfs, men zag een niet-significante daling van 14 % (RR 0,86, 95 % BI: 0,73- 1,00; P = 0,06). Voornamelijk apixaban en edoxaban bleken superieur, terwijl rivaroxaban en dabigatran non-inferieur waren.
Naast de veranderingen m.b.t. OAC zijn gedurende de jaren ook andere aspecten veranderd in de opeenvolgende richtlijnen, niet in het minst het belang van een multidisciplinaire, patiënt-georiënteerde zorg. Het belang daarvan wordt later in dit verslag toegelicht.
De nieuwe zaken in de gepubliceerde richtlijnen van 2020
Prof. T. Potpara
In de nieuwe richtlijnen wordt het acroniem 'CC to ABC' of 'BB naar ABC' als rode draad gebruikt voor de diagnostiek en aanpak van voorkamerfibrillatie (figuur 2). Voluit wordt dit: 'Confirm and Characterise atrial fibrillation and then treat it following the ABC pathway (anticoagulation - better symptom control - comorbidities/cardiovascular risk management)'. De nieuwe aanbevelingen over anticoagulatie zullen in deze paragraaf worden toegelicht. 
Zoals gekend is het belangrijk om het ischemische risico van de patiënt te bepalen aan de hand van de CHA2Ds2- VASc-score, alsook het bloedingsrisico in te schatten aan de hand van de HAS-BLED-score. Belangrijk hierbij is om de reversibele oorzaken van een hoge HAS-BLED-score aan te pakken en patiënten met een HAS-BLED-score van drie of meer frequenter op te volgen. Het bloedingsrisico (en het ischemische risico) van een patiënt is namelijk een zeer dynamisch gegeven dat verandert over de tijd en moet daarom frequent opnieuw geëvalueerd worden. Bij patiënten met een laag ischemisch risico moet een nieuwe evaluatie van dit risico al gebeuren na vier tot zes maanden. Bij een absolute contra-indicatie voor OAC kan het sluiten van het linkerhartoortje overwogen worden. Een hoge HAS-BLED-score, zonder absolute contra-indicatie voor OAC, is echter geen reden om de opstart van OAC uit te stellen. Voorts zijn er nog enkele belangrijke aanpassingen inzake OAC voor specifieke domeinen. Zo hoeft er bij de patiënten met een VKF die minder dan 24 uur aan de gang is en een laag ischemisch risico aanwezig is (CHA2Ds2-VASc 0 bij mannen of 1 bij vrouwen) geen OAC geassocieerd te worden na cardioversie. Bij patiënten met een verhoogd ischemisch risico en geplande ablatie wordt pre-procedureel het beste drie weken OAC geassocieerd of, indien niet mogelijk, een transoesofagale echocardiografie uitgevoerd ter exclusie van een trombus. Bij patiënten met VKF en een acuut coronair syndroom (ACS) wordt na een percutane coronaire interventie (PCI) aangeraden het gebruik van acetylsalicylzuur na < 1 week te stoppen en duale therapie met een P2Y12-inhibitor (bij voorkeur clopidogrel) en OAC te continueren tot 12 maanden in totaal, als het risico op stenttrombose lager is dan het potentiële bloedingsrisico. Bij een chronisch coronair syndroom geldt dezelfde aanbeveling, maar wordt de P2Y12-inhibitor slechts 6 maanden gegeven. Wat de aanpak van postoperatieve VKF betreft, wordt een onderscheid gemaakt tussen cardiale en non-cardiale heelkunde. Bij patiënten met een postoperatieve VKF bestaat in de nieuwe richtlijnen een klein nuanceverschil. De aanbeveling om OAC te initiëren bij een VKF na non-cardiale heelkunde is namelijk iets sterker dan bij cardiale heelkunde.
Het belang van de educatie van zowel arts als patiënt
Prof. H. Heidbuchel
In de afgelopen jaren heeft geïntegreerde zorg meer en meer zijn (kosten)-effectiviteit bewezen. Zo werd in 2017 de IMPACT-AF- trial gepubliceerd.12 Hierin werden 2 281 patiënten met VKF en indicatie voor OAC gerandomiseerd in twee groepen. Enerzijds een groep die de standaardbehandeling kreeg en anderzijds een groep waarbij zowel artsen als patiënten op diverse manieren educatie ontvingen. Het primaire eindpunt bestond uit het aantal patiënten dat adequate therapie met OAC ontving. Na een mediane opvolging van 12 maanden bleek het aantal correct behandelde patiënten in de interventiegroep significant hoger dan in de controlegroep (OR 3,28: 95 % BI 1,67-6,44; P = 0,0002) (figuur 3). Hoewel de studie niet genoeg statistische kracht had om klinische eindpunten te evalueren, toonde deze toch een sterke daling in de incidentie van een beroerte bij de interventiegroep (HR 0,48: 95 % BI 0,23-0,99; P = 0,043). De bevindingen van deze studie worden momenteel gevalideerd in een groot Europees project: de STEEER-AF-trial. In de eerste fase van dit project, gepubliceerd in 2018, werd de ontbrekende kennis van artsen omtrent VKF in kaart gebracht.13 In een tweede, nog lopende, fase van het project wordt onderzocht of specifieke interventies om deze kennistekorten weg te werken kunnen leiden tot een beter resultaat voor de patiënt. Naast educatie van artsen is echter ook het onderrichten van patiënten in hun ziekte van uitermate belang en wordt dit sterk aanbevolen in de nieuwe ESC-richtlijnen. Jammer genoeg wordt dit vaak als tijdrovend ervaren en bijgevolg achterwege gelaten. Om dit probleem te verhelpen zijn er diverse mogelijkheden ontwikkeld (vragenlijsten, onlinetools en smartphone-applicaties) om gerichte educatie voor de patiënt te voorzien, aangezien het nut hiervan reeds meermaals werd bewezen. Zo toonde de HELP-AF- studie in 2019 gunstige resultaten.14 Hierbij werden 627 patiënten die zich met VKF hadden gepresenteerd op de dienst spoedgevallen gerandomiseerd in twee groepen. De ene groep kreeg de standaardbehandeling, de andere groep een intensiever programma met twee huisbezoeken van een verpleegkundige of apotheker die de diverse aspecten van VKF onderwees. Na een opvolging van 24 maanden was er een significante daling in het aantal ongeplande hospitalisaties (IRR 0,74: 95 % BI 0,62-0,89; P = 0,001). Deze resultaten werden eveneens bevestigd door een grote Chinese studie uit 2020, de mAFA-studie.15 Daarbij werden 3 324 patiënten gerandomiseerd in twee groepen, waarbij de ene groep de standaardbehandeling kreeg en de andere groep eveneens gerichte educatie via een smartphone-applicatie (zowel de patiënt als de behandelende arts). Het primaire eindpunt was samengesteld uit beroerte, sterfte van alle oorzaak en rehospitalisatie. Na een mediane opvolging van ± 300 dagen zag men een significante daling op dit primaire eindpunt in de interventiegroep (HR: 0,39 95 % BI 0,22-0,67; P < 0,001). Momenteel wordt eveneens een Belgische trial georganiseerd om diverse manieren van educatie met elkaar te vergelijken. Bovenstaande zaken tonen eens te meer dat een geïntegreerde aanpak van VKF van belang is voor mens en maatschappij. 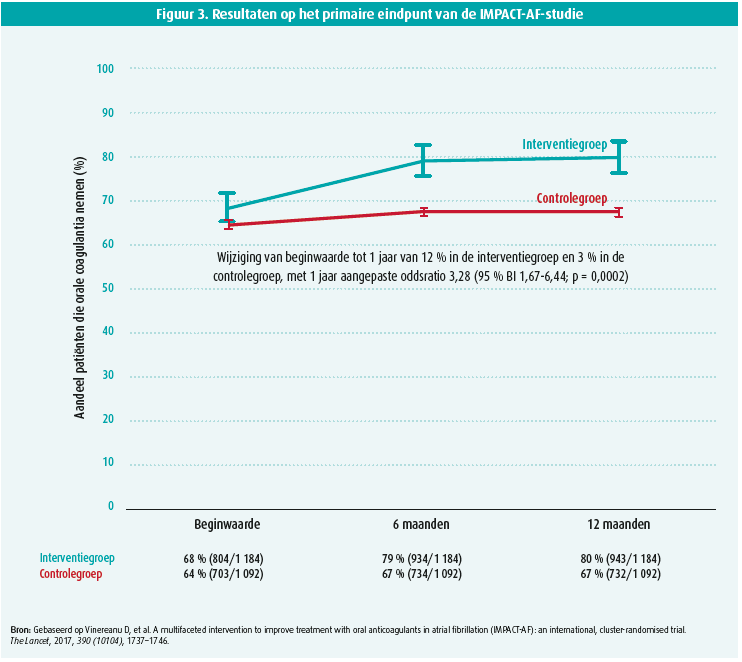
Referenties
- Fuster, V., Rydén, L.E., Cannom, D.S., Crijns, H.J., Curtis, A.B., Ellenbogen, K.A. et al. ACC/AHA/ESC 2006 guidelines for the management of patients with atrial fibrillation-executive summary: a report of the American College of Cardiology/ American Heart Association Task Force on Practice Guidelines and the European Society of Cardiology Committee for Practice Guidelines (Writing Committee to Revise the 2001 Guidelines for the Management of Patients with Atrial Fibrillation). Eur Heart J, 2006, 27 (16), 1979-2030.
- Connolly, S.J., Ezekowitz, M.D., Yusuf, S., Eikelboom, J., Oldgren, J., Parekh, A. et al. Dabigatran versus warfarin in patients with atrial fibrillation. N Engl J Med, 2009, 361 (12), 1139-1151.
- Camm, A.J., Kirchhof, P., Lip, G.Y.H., Schotten, U., Savelieva, I., Ernst, S. et al. Guidelines for the management of atrial fibrillation: the Task Force for the Management of Atrial Fibrillation of the European Society of Cardiology (ESC). Eur Heart J, 2010, 31 (19), 2369-2429.
- Granger, C.B., Alexander, J.H., McMurray, J.J.V., Lopes, R.D., Hylek, E.M., Hanna, M. et al. Apixaban versus warfarin in patients with atrial fibrillation. N Engl J Med, 2011, 365 (11), 981-992.
- Patel, M.R., Mahaffey, K.W., Garg, J., Pan, G., Singer, D.E., Hacke, W. et al. Rivaroxaban versus warfarin in nonvalvular atrial fibrillation. N Engl J Med, 2011, 365 (10), 883-891.
- Camm, A.J., Lip, G.Y.H., De Caterina, R., Savelieva, I., Atar, D., Hohnloser, S.H. et al. 2012 focused update of the ESC Guidelines for the management of atrial fibrillation: an update of the 2010 ESC Guidelines for the management of atrial fibrillation. Developed with the special contribution of the European Heart Rhythm Association. Eur Heart J, 2012, 33 (21), 2719-2747.
- Giugliano, R.P., Ruff, C.T., Braunwald, E., Murphy, S.A., Wiviott, S.D., Halperin, J.L. et al. Edoxaban versus warfarin in patients with atrial fibrillation. N Engl J Med, 2013, 369 (22), 2093-2104.
- Ruff, C.T., Giugliano, R.P., Braunwald, E., Hoffman, E.B., Deenadayalu, N., Ezekowitz, M.D. et al. Comparison of the efficacy and safety of new oral anticoagulants with warfarin in patients with atrial fibrillation: a meta-analysis of randomised trials. The Lancet, 2014, 383 (9921), 955-962.
- January, C.T., Wann, L.S., Alpert, J.S., Calkins, H., Cigarroa, J.E., Cleveland, J.C.J. et al. 2014 AHA/ACC/HRS guideline for the management of patients with atrial fibrillation: a report of the American College of Cardiology/American Heart Association Task Force on practice guidelines and the Heart Rhythm Society. Circulation, 2014, 130 (23), e199-267.
- Kirchhof, P., Benussi, S., Kotecha, D., Ahlsson, A., Atar, D., Casadei, B. 2016 ESC Guidelines for the management of atrial fibrillation developed in collaboration with EACTS. Eur Heart J, 2016, 37, 2893-2962.
- January, C.T., Wann, L.S., Calkins, H., Chen, L.Y., Cigarroa, J.E., Cleveland, J.C.J. et al. 2019 AHA/ACC/HRS Focused Update of the 2014 AHA/ACC/HRS Guideline for the Management of Patients With Atrial Fibrillation: A Report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines and the Heart Rhythm Society in Collaboration With the Society of Thoracic Surgeons. Ciruclation, 2019, 140 (2), e125-151.
- Vinereanu, D., Lopes, R.D.,, Bahit M.C., Xavier, D., Jiang, J., Al-Khalidi, H.R. et al. A multifaceted intervention to improve treatment with oral anticoagulants in atrial fibrillation (IMPACT-AF): an international, cluster-randomised trial. The Lancet, 2017, 390 (10104), 1737-1746.
- Heidbuchel, H., Dagres, N., Antz, M., Kuck, K-H., Lazure, P., Murray, S. et al. Major knowledge gaps and system barriers to guideline implementation among European physicians treating patients with atrial fibrillation: a European Society of Cardiology international educational needs assessment. Europace, 2018, 20 (12), 1919-1928.
- Sanders, P. Home-based education reduces hospitalisations in patients with atrial fibrillation. ESC Congres 2019, Parijs.
- Guo, Y., Lane, D.A., Wang, L., Zhang, H., Wang, H., Zhang, W. et al. Mobile Health Technology to Improve Care for Patients with Atrial Fibrillation. J Am Coll Cardiol, 2020, 75 (13), 1523-1534.
Aucun élément du site web ne peut être reproduit, modifié, diffusé, vendu, publié ou utilisé à des fins commerciales sans autorisation écrite préalable de l’éditeur. Il est également interdit de sauvegarder cette information par voie électronique ou de l’utiliser à des fins illégales.