EACVI - Best of Imaging 2020 Congresverslag
Er is een deel weggevallen uit de tekst: Op EACVI2020, het recente online congres van de European Association of Cardiovascular Imaging, werd een sessie gewijd aan kwantificering door middel van cardiovasculaire magnetische resonantie (CMR). Deze sessie gaf een mooi overzicht van de almaar toenemende mogelijkheden van CMR als 'virtuele biopsie' voor research, en zijn toepassingen in de klinische praktijk. CMR-experten Steffen Petersen (London, Verenigd Koninkrijk) en Matthias Friedrich (Montreal, Canada) traden op als chairmen.Myocardial tissue mapping
Daniel Messroghli (Berlijn, Duitsland)
CMR is een belangrijke niet-invasieve beeldvormingstechniek voor de oppuntstelling van cardiomyopathieën, voornamelijk omdat deze techniek ons toelaat het myocardweefsel te karakteriseren en hierbij de oorzaak van myocardiale dysfunctie te identificeren. Zo maakt conventionele CMR gebruik van T2-gewogen beelden voor het vaststellen van oedeem, wat kan wijzen op actieve inflammatie. Verder kan men focale fibrose of verlittekening detecteren door middel van laattijdige opnames na intraveneuze toediening van een gadolinium bevattend contrastmiddel, de zogenaamde late gadolinium enhancement (LGE), aangezien gadolinium accumuleert ter hoogte van collageenrijk weefsel. Een belangrijke beperking van deze conventionele technieken is dat diffuse aantasting van het myocard onvoldoende gedetecteerd wordt.
Het opsporen van diffuse myocardiale aantasting is wel mogelijk door middel van tissue mapping, waarbij de (gemiddelde) signaalintensiteit over het gehele myocard gemeten wordt. T1-mapping is een van de belangrijkste CMR-technieken om het myocardweefsel te kwantificeren en uiteindelijk te karakteriseren. (Figuur 1)
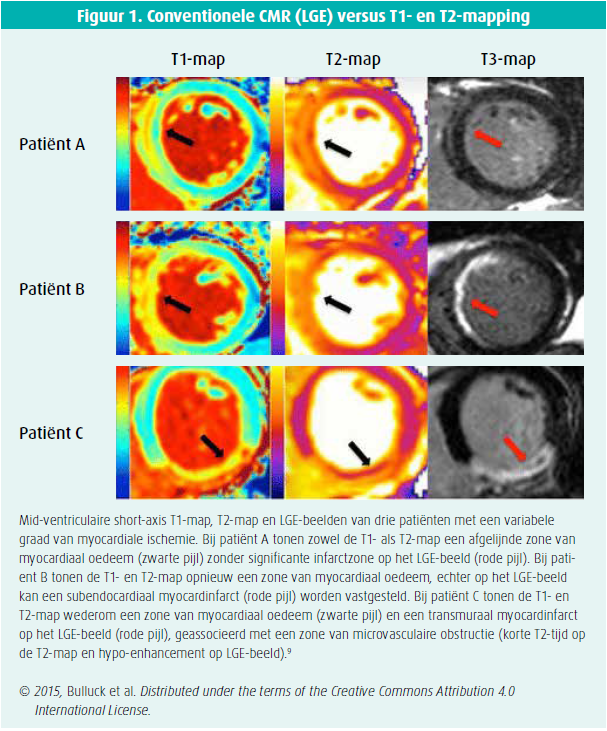
De visuele map wordt opgebouwd door middel van kleurcodes gerelateerd aan de T1-relaxatietijd. Dit is de tijd die het weefsel nodig heeft om 63 % van de originele longitudinale magnetisatie te herstellen na toediening van een radiofrequentiepuls. Deze T1-tijd is weefselspecifiek en heeft bijgevolg belangrijke additionele waarde in de diagnostiek van inflammatoire aandoeningen, diffuse myocardiale fibrose en stapelingsziekten.1 (Figuur 2) Op basis van het verschil tussen de natieve T1-tijd (voor contrasttoediening) en post-contrast T1-tijd, kan het extracellulair volume (ECV) berekend worden. De ECV-fractie stijgt in aanwezigheid van bijvoorbeeld myocardiale fibrose of amyloïdose (normaal ECV < 30 %).2 Dr. Messroghli haalt tevens aan dat de ECV-waarde een goede prognostische merker blijkt te zijn.3
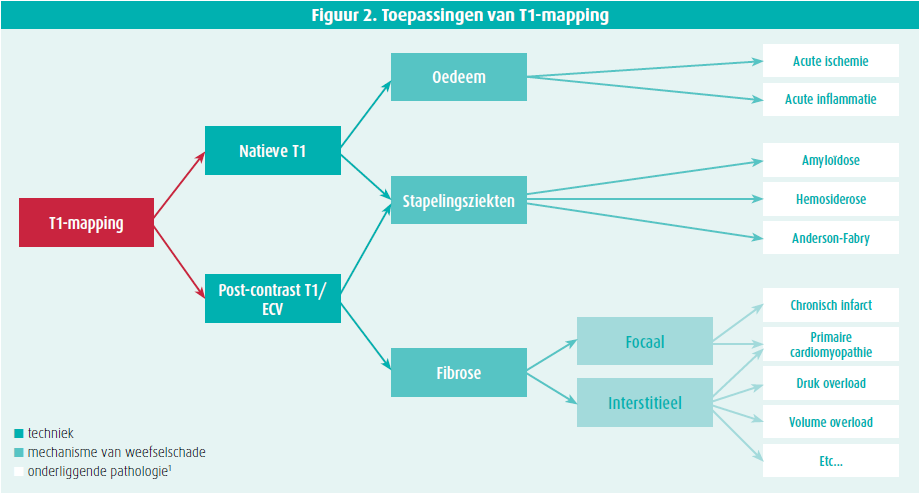
Verder zijn ook T2 en T2* belangrijke modaliteiten in tissue mapping. T2-mapping wordt voornamelijk gebruikt voor de detectie van oedeem en myocardiale inflammatie. (Figuur 1) Bij verdenking op ijzerstapeling in het myocard wordt T2*-mapping uitgevoerd.2
Ter conclusie werd gesteld dat myocardiale tissue mapping additionele waarde heeft ten opzichte van conventionele CMR in de detectie van diffuse myocardiale pathologie. Verder zijn vooral natieve T1-tijd en ECV belangrijke parameters voor het inschatten van respectievelijk de ziekteactiviteit van acute cardiale pathologie en prognose van chronische myocardiale aandoeningen.
Perfusiemapping
James Moon (London, Verenigd Koninkrijk)
Naast het evalueren van myocardiale functie en structuur, bestaat met CMR ook de mogelijkheid om perfusie noninvasief te beoordelen, bijvoorbeeld bij vermoeden van coronairlijden of microvasculair lijden. Door middel van stressperfusie- CMR wordt de doorbloeding van het myocard gevisualiseerd voor en na toediening van een intraveneuze vasodilatator (adenosine). Naar analogie van de T1-mapping, kan ook de perfusiescan gekwantificeerd worden. De myocardiale bloedflow (MBF) wordt per pixel afzonderlijk berekend in ml/g/min. Vervolgens worden de gegevens omgezet naar een map met kleurcodes en kan de gemiddelde MBF berekend worden.4 (Figuur 3)
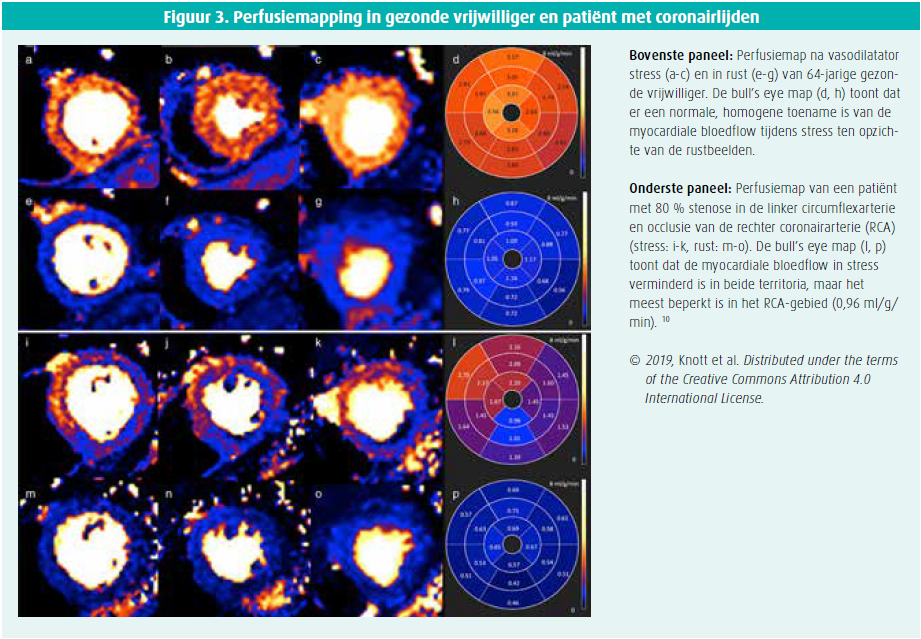
Perfusiemapping heeft enkele belangrijke voordelen ten opzichte van conventionele stressperfusie-CMR. De techniek werkt sneller, is minder operatorafhankelijk en heeft de mogelijkheid om meer (gebalanceerde) ischemie en microvasculaire dysfunctie te diagnosticeren. Ook heeft het potentieel om nieuwe biomerkers te detecteren.4
De laatste jaren werd de techniek van perfusiemapping geïmplementeerd in verschillende centra wereldwijd en kende de literatuur een toename van evidentie betreffende coronaire en ook nietcoronaire pathologie. Zo werd door de onderzoeksgroep van prof. Moon bij patiënten met hypertrofe cardiomyopathie frequent microvasculaire dysfunctie gedetecteerd door middel van perfusiemapping. Hoewel deze bevindingen gecorreleerd bleken te zijn met regionale hypertrofie en fibrose, kon ook in afwezigheid van deze criteria een gedaalde MBF worden geobserveerd na vasodilatator stress. Mogelijk bestaat er bij deze patiënten bijgevolg een rol voor perfusiemapping in de detectie van microvasculaire disfunctie vroeg in de ontwikkeling van het fenotype.5
Bovendien benadrukte prof. Moon dat recent werd aangetoond dat het kwantificeren van myocardiale perfusie eveneens van beduidend prognostisch belang is. Zo bleek een verlaagde stress-MBF onafhankelijk geassocieerd te zijn met majeure cardiovasculaire events (MACE) en overlijden in patiënten met vermoeden van coronairlijden.6
Tot slot kan geconcludeerd worden dat perfusiemapping een veelbelovende CMR-techniek is voor het kwantificeren van MBF. Het biedt de mogelijkheid om bijkomende inzichten te verwerven omtrent microvasculair lijden en heeft mogelijk een rol als nieuwe biomerker.
Myocardiale deformatie en diffusion tensor imaging
Alicia Maria Maceira Gonzalez (Valencia, Spanje)
Het analyseren van de myocardiale deformatie of vervorming door middel van CMR is een opkomende techniek en is interessant om verschillende redenen. Zo heeft het myocard een complexe architectuur waarbij deformatie in verschillende richtingen gebeurt en zijn er heel wat aandoeningen waarbij het hart niet uniform aangetast is. De meest onderzochte myocardiale deformatieparameter is strain. Dit betreft de deformatie van de myocardiale segmenten tijdens systole (= verkorting of verdikking) in relatie tot hun lengte in rusttoestand. Men kan drie types strain onderscheiden: longitudinaal, circumferentieel en radiaal. (Figuur 4) Naast strain kan ook de torsie van het myocard geëvalueerd worden. Tijdens de ventriculaire contractie bestaat er een rotatie met de klok mee in de basale segmenten en een rotatie tegen de klok in de apicale segmenten.7
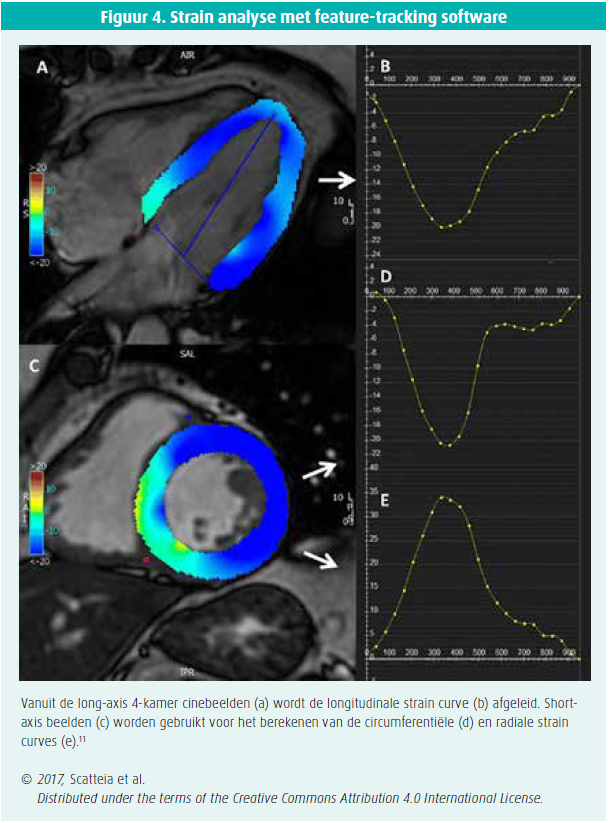
De belangrijkste klinische toepassing bestaat volgens prof. Maceira uit het detecteren van vroege myocardiale aantasting, bijvoorbeeld in de cardio-oncologie of bij amyloïdose. Verder kan men de globale en regionale functie kwantitatief beoordelen. Er bestaan echter nog onvoldoende data voor een gestandaardiseerde toepassing in de klinische praktijk.
Naast de reeds besproken macroscopische eigenschappen van myocardiale contractiliteit, kan deformatie ook op microscopisch niveau bestudeerd worden door een nieuwe techniek genaamd diffusion tensor imaging. Momenteel bevindt de ontwikkeling van deze techniek zich nog in een vroeg stadium8, maar in de toekomst heeft dit echter wel potentieel om, door het bestuderen van de cardiale microarchitectuur, nieuwe inzichten te verwerven over het cardiale fenotype.
In conclusie kan gesteld worden dat CMR als niet-invasieve techniek steeds meer mogelijkheden biedt in de diagnostiek van myocardiale aandoeningen als 'virtuele biopsie', bijvoorbeeld door geavanceerde weefselkarakterisering of het evalueren van perfusiedefecten. Hoewel tissue- en perfusiemapping hun weg al hebben gevonden naar de klinische praktijk, zullen verdere onderzoeken moeten uitwijzen wat de rol is van myocardiale deformatie en meer recent ontwikkelde technieken zoals diffusion tensor imaging.
Referenties
- Schelbert, E.B., Messroghli, D.R. State of the Art: Clinical Applications of Cardiac T1 Mapping. Radiology, 2016, 278 (3), 658-676.
- Messroghli, D.R., Moon, J.C., Ferreira, V.M., Grosse-Wortmann, L., He, T., Kellman, P. et al. Clinical recommendations for cardiovascular magnetic resonance mapping of T1, T2, T2* and extracellular volume: A consensus statement by the Society for Cardiovascular Magnetic Resonance (SCMR) endorsed by the European Association for Cardiovascular Imaging (EACVI). J Cardiovasc Magn Reson, 2017, 19 (1), 75.
- Schelbert, E.B., Piehler, K.M., Zareba, K.M., Moon, J.C., Ugander, M., Messroghli, D.R. et al. Myocardial Fibrosis Quantified by Extracellular Volume Is Associated With Subsequent Hospitalization for Heart Failure, Death, or Both Across the Spectrum of Ejection Fraction and Heart Failure Stage. J Am Heart Assoc, 2015, 4 (12).
- Kellman, P., Hansen, M.S., Nielles- Vallespin, S., Nickander, J., Themudo, R., Ugander, M. et al. Myocardial perfusion cardiovascular magnetic resonance: optimized dual sequence and reconstruction for quantification. J Cardiovasc Magn Reson, 2017, 19 (1), 43.
- Camaioni, C., Knott, K.D., Augusto, J.B., Seraphim, A., Rosmini, S., Ricci, F. et al. Inline perfusion mapping provides insights into the disease mechanism in hypertrophic cardiomyopathy. Heart, 2020, 106 (11), 824-829.
- Knott, K.D., Seraphim, A., Augusto, J.B., Xue, H., Chacko, L., Aung, N. et al. The Prognostic Significance of Quantitative Myocardial Perfusion: An Artificial Intelligence-Based Approach Using Perfusion Mapping. Circulation, 2020, 141 (16), 1282-1291.
- Vo, H.Q., Marwick, T.H., Negishi, K. MRIDerived Myocardial Strain Measures in Normal Subjects. J Am Coll Cardiol Img, 2018, 11 (2 Pt 1), 196-205.
- Nielles-Vallespin, S., Khalique, Z., Ferreira, P.F., de Silva, R., Scott, A.D., Kilner, P. et al. Assessment of Myocardial Microstructural Dynamics by In Vivo Diffusion Tensor Cardiac Magnetic Resonance. J Am Coll Cardiol, 2017, 69 (6), 661-676.
- Bulluck, H., White, S.K., Rosmini, S., Bhuva, A., Treibel, T.A., Fontana, M. et al. T1 mapping and T2 mapping at 3T for quantifying the area-at-risk in reperfused STEMI patients. J Cardiovasc Magn Reson, 2015, 17 (1), 73.
- Knott, K.D., Camaioni, C., Ramasamy, A., Augusto, J.A., Bhuva, A.N., Xue, H. et al. Quantitative myocardial perfusion in coronary artery disease: A perfusion mapping study. J Magn Reson Imaging, 2019, 50 (3), 756-762.
- Scatteia, A., Baritussio, A., Bucciarelli-Ducci, C. Strain imaging using cardiac magnetic resonance. Heart Fail Rev, 2017, 22 (4), 465-476.
Aucun élément du site web ne peut être reproduit, modifié, diffusé, vendu, publié ou utilisé à des fins commerciales sans autorisation écrite préalable de l’éditeur. Il est également interdit de sauvegarder cette information par voie électronique ou de l’utiliser à des fins illégales.