EACVI - Best of Imaging 2020 Compte rendu du congrès
Lors de l'EACVI 2020, le récent congrès virtuel de la European Association of Cardiovascular Imaging, une session a été consacrée à la quantification à l'aide de l' imagerie par résonance magnétique (IRM) cardiaque. Cette session a donné un bel aperçu des possibilités sans cesse croissantes de la IRM cardiaque en tant que « biopsie virtuelle » pour la recherche, et de ses applications en pratique clinique. Steffen Petersen (Londres, Royaume-Uni) et Matthias Friedrich (Montréal, Canada), tous deux experts en IRM cardiaque, ont présidé cette session.Myocardial tissue mapping
Daniel Messroghli (Berlin, Allemagne)
La IRM cardiaque est une importante technique d'imagerie non invasive pour la mise au point de cardiomyopathies, essentiellement parce que cette technique nous permet de caractériser le tissu myocardique et, ce faisant, d'identifier la cause d'une dysfonction myocardique. Ainsi, la IRM cardiaque conventionnelle utilise les clichés en pondération T2 pour la constatation d'un oedème, ce qui peut indiquer une inflammation active. Par ailleurs, nous pouvons détecter une fibrose focale ou la présence d'une zone cicatricielle au moyen de clichés tardifs après l'administration intraveineuse d'un produit de contraste à base de gadolinium (séquence appelée late gadolinium enhancement (LGE) ou rehaussement tardif), étant donné que le gadolinium s'accumule au niveau des tissus riches en collagène. Ces techniques conventionnelles impliquent une importante limitation, en ce sens qu'une atteinte diffuse du myocarde est insuffisamment détectée.
La détection d'une atteinte myocardique diffuse est toutefois possible grâce à la cartographie tissulaire, lors de laquelle on mesure l'intensité de signal (moyenne) au niveau de l'ensemble du myocarde. La cartographie T1 (ou T1 mapping) est l'une des principales techniques de IRM cardiaque pour quantifier le tissu myocardique et finalement le caractériser (figure 1).
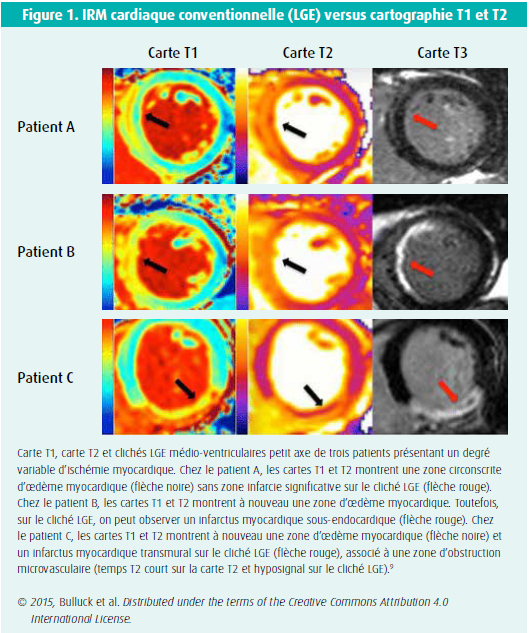
La carte visuelle est élaborée à l'aide de codes de couleurs, liés au temps de relaxation T1, qui est le temps qu'il faut au tissu pour récupérer 63 % de la magnétisation longitudinale initiale après l'administration d'une onde de radiofréquence. Ce temps T1 est spécifique aux tissus et il a par conséquent une importante valeur additionnelle pour le diagnostic des affections inflammatoires, de la fibrose myocardique diffuse et des maladies de surcharge1 (figure 2).

Sur la base de la différence entre le temps T1 natif (avant l'administration du produit de contraste) et le temps T1 post-contraste, nous pouvons calculer le volume extracellulaire (ECV). La fraction de l'ECV augmente en présence d'une fibrose myocardique ou d'une amyloïdose, par exemple (ECV normal < 30 %)2. Le Dr Messroghli a également précisé que la valeur de l'ECV paraissait être un bon marqueur pronostique3.
Par ailleurs, les séquences T2 et T2* sont aussi des modalités importantes pour la cartographie tissulaire. La cartographie T2 (ou T2 mapping) est principalement utilisée pour la détection de l'oedème et de l'inflammation myocardique (figure 1). En cas de suspicion d'accumulation de fer dans le myocarde, l'on recourt à la cartographie T2*2.
En guise de conclusion, il a été avancé que la cartographie tissulaire myocardique avait une valeur additionnelle comparativement à la IRM cardiaque conventionnelle pour la détection d'une pathologie myocardique diffuse. En outre, le temps T1 natif et l'ECV, principalement, sont des paramètres importants, respectivement pour l'évaluation de l'activité de la maladie en cas de pathologie cardiaque aiguë et le pronostic des affections myocardiques chroniques.
Perfusion mapping
James Moon (Londres, Royaume-Uni)
Outre l'évaluation de la fonction et de la structure du myocarde, la IRM cardiaque permet également d'évaluer la perfusion de manière non invasive, par exemple en cas de suspicion de maladie coronarienne ou d'atteinte microvasculaire. Grâce à la IRM cardiaque « de stress », la vascularisation du myocarde est visualisée avant et après l'administration d'un vasodilatateur intraveineux (adénosine). Par analogie avec la cartographie T1, la perfusion peut également être quantifiée. Le débit sanguin myocardique (DSM) est calculé pixel par pixel en ml/g/min. Ensuite, les données sont converties en carte avec des codes de couleurs, et le DSM moyen peut être calculé4 (figure 3).
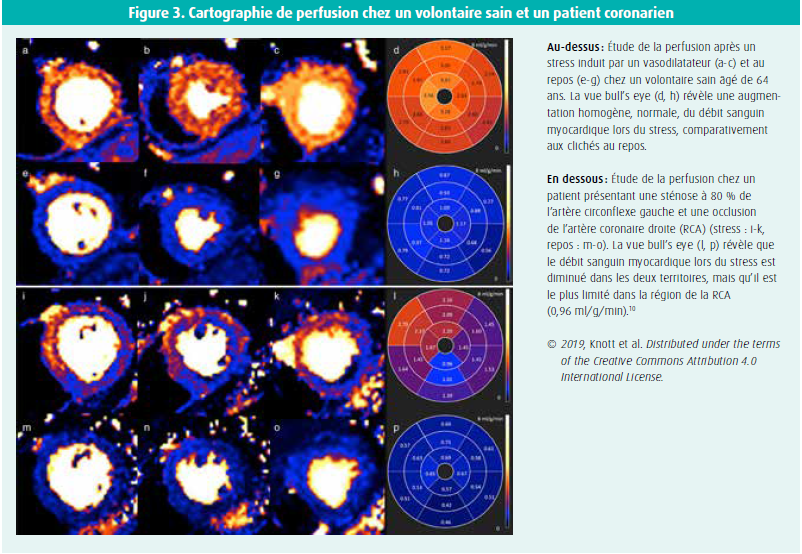
Le module « perfusion » a quelques avantages importants par rapport à la IRM cardiaque de stress conventionnelle. La technique est plus rapide, elle dépend moins de l'opérateur et permet de mieux diagnostiquer l'ischémie (compensée) et la dysfonction microvasculaire. Elle a également le potentiel de détecter de nouveaux biomarqueurs4.
Ces dernières années, le module « perfusion » a été implémenté dans différents centres dans le monde, et de plus en plus de données probantes au sujet des pathologies coronaires et non coronaires ont été publiées. Ainsi, chez des patients souffrant d'une cardiomyopathie hypertrophique, le groupe de recherche du Prof. Moon a fréquemment détecté une dysfonction microvasculaire grâce au module « perfusion ». Bien que ces observations paraissent corrélées à une hypertrophie et une fibrose régionales, on a également observé une diminution du DSM après un stress induit par un vasodilatateur en l'absence de ces critères. Par conséquent, il est possible que l'étude de la perfusion ait un rôle potentiel chez ces patients, pour détecter une dysfonction microvasculaire précocement dans le développement du phénotype5.
En outre, le Prof. Moon a souligné qu'il avait récemment été démontré que la quantification de la perfusion myocardique avait également une importance pronostique considérable. Ainsi, il est apparu qu'un DSM de stress abaissé était indépendamment associé à des événements cardiovasculaires indésirables graves (MACE) et au décès chez les patients suspects de maladie coronarienne6.
Enfin, nous pouvons conclure que l'étude de la perfusion est une technique de IRM cardiaque prometteuse pour la quantification du DSM. Elle permet d'acquérir des notions complémentaires au sujet de l'atteinte microvasculaire et a potentiellement un rôle en tant que nouveau biomarqueur.
Myocardial deformation and diffusion tensor imaging
Alicia Maria Maceira Gonzalez (Valence, Espagne)
L'analyse de la déformation myocardique à l'aide de la IRM cardiaque est une technique émergente, intéressante pour plusieurs raisons. Ainsi, le myocarde présente une architecture complexe, ce qui explique que la déformation se produise dans différentes directions. De nombreuses affections sont par ailleurs caractérisées par une atteinte non uniforme du coeur. Le paramètre de déformation myocardique le plus étudié est le strain, ou déformation des segments myocardiques pendant la systole (= raccourcissement ou épaississement) par rapport à leur longueur au repos. Nous pouvons distinguer trois types de strains : longitudinal, circonférentiel et radial (figure 4). Outre le strain, nous pouvons également évaluer la torsion du myocarde. Pendant la contraction ventriculaire, il se produit une rotation horaire dans les segments basaux, et une rotation antihoraire dans les segments apicaux.7
Selon la Prof. Maceira, la principale application clinique consiste en la détection d'une atteinte myocardique précoce, par exemple en cardio-oncologie ou en cas d'amyloïdose. Par ailleurs, nous pouvons évaluer quantitativement la fonction globale et régionale. Toutefois, les données sont encore insuffisantes pour justifier une utilisation standardisée en pratique clinique.
Outre les propriétés macroscopiques de la contractilité myocardique, déjà évoquées, la déformation peut également être étudiée au niveau microscopique à l'aide d'une nouvelle technique appelée DTI, (diffusion tensor imaging, ou IRM de diffusion). Pour le moment, le développement de cette technique en est encore à ses balbutiements8, mais à l'avenir, elle permettra sans doute d'élargir les connaissances au sujet du phénotype cardiaque, via l'étude de la microarchitecture cardiaque.
Pour conclure, nous pouvons affirmer que la IRM cardiaque, en tant que technique non invasive, offre de plus en plus de possibilités pour le diagnostic des affections myocardiques en tant que « biopsie virtuelle », par exemple grâce à la caractérisation avancée des tissus ou à l'évaluation des défauts de perfusion. Bien que la cartographie tissulaire et l'étude de la perfusion aient déjà trouvé leur voie en pratique clinique, de plus amples études devront montrer quel est le rôle de la déformation myocardique et des techniques plus récentes telles que la DTI.
Références
- Schelbert, E.B., Messroghli, D.R. State of the Art: Clinical Applications of Cardiac T1 Mapping. Radiology, 2016, 278 (3), 658-676.
- Messroghli, D.R., Moon, J.C., Ferreira, V.M., Grosse-Wortmann, L., He, T., Kellman, P. et al. Clinical recommendations for cardiovascular magnetic resonance mapping of T1, T2, T2* and extracellular volume: A consensus statement by the Society for Cardiovascular Magnetic Resonance (SCMR) endorsed by the European Association for Cardiovascular Imaging (EACVI). J Cardiovasc Magn Reson, 2017, 19 (1), 75.
- Schelbert, E.B., Piehler, K.M., Zareba, K.M., Moon, J.C., Ugander, M., Messroghli, D.R. et al. Myocardial Fibrosis Quantified by Extracellular Volume Is Associated With Subsequent Hospitalization for Heart Failure, Death, or Both Across the Spectrum of Ejection Fraction and Heart Failure Stage. J Am Heart Assoc, 2015, 4 (12).
- Kellman, P., Hansen, M.S., Nielles- Vallespin, S., Nickander, J., Themudo, R., Ugander, M. et al. Myocardial perfusion cardiovascular magnetic resonance: optimized dual sequence and reconstruction for quantification. J Cardiovasc Magn Reson, 2017, 19 (1), 43.
- Camaioni, C., Knott, K.D., Augusto, J.B., Seraphim, A., Rosmini, S., Ricci, F. et al. Inline perfusion mapping provides insights into the disease mechanism in hypertrophic cardiomyopathy. Heart, 2020, 106 (11), 824-829.
- Knott, K.D., Seraphim, A., Augusto, J.B., Xue, H., Chacko, L., Aung, N. et al. The Prognostic Significance of Quantitative Myocardial Perfusion: An Artificial Intelligence-Based Approach Using Perfusion Mapping. Circulation, 2020, 141 (16), 1282-1291.
- Vo, H.Q., Marwick, T.H., Negishi, K. MRIDerived Myocardial Strain Measures in Normal Subjects. J Am Coll Cardiol Img, 2018, 11 (2 Pt 1), 196-205.
- Nielles-Vallespin, S., Khalique, Z., Ferreira, P.F., de Silva, R., Scott, A.D., Kilner, P. et al. Assessment of Myocardial Microstructural Dynamics by In Vivo Diffusion Tensor Cardiac Magnetic Resonance. J Am Coll Cardiol, 2017, 69 (6), 661-676.
- Bulluck, H., White, S.K., Rosmini, S., Bhuva, A., Treibel, T.A., Fontana, M. et al. T1 mapping and T2 mapping at 3T for quantifying the area-at-risk in reperfused STEMI patients. J Cardiovasc Magn Reson, 2015, 17 (1), 73.
- Knott, K.D., Camaioni, C., Ramasamy, A., Augusto, J.A., Bhuva, A.N., Xue, H. et al. Quantitative myocardial perfusion in coronary artery disease: A perfusion mapping study. J Magn Reson Imaging, 2019, 50 (3), 756-762.
- Scatteia, A., Baritussio, A., Bucciarelli-Ducci, C. Strain imaging using cardiac magnetic resonance. Heart Fail Rev, 2017, 22 (4), 465-476.
Niets van de website mag gebruikt worden voor reproductie, aanpassing, verspreiding, verkoop, publicatie of commerciële doeleinden zonder voorafgaande schriftelijke toestemming van de uitgever. Het is ook verboden om deze informatie elektronisch op te slaan of te gebruiken voor onwettige doeleinden.