Wie, wanneer, hoe?
Aortaklepstenose is een frequente ziekte die 2,6 - 6 % van de 65-plussers treft.1 In 2017 waren er 12,6 miljoen gevallen en jaarlijks sterven 102 700 mensen aan aortaklepstenose.2 De prevalentie stijgt gestaag, wat ten dele toe te schrijven is aan de langere levensverwachting.3 Aortaklepstenose is makkelijk te herkennen bij hartauscultatie, vaak al in een vroeg stadium, als er nog geen hemodynamische repercussie is. De stenose verergert langzaam. Men kan de ernst ervan makkelijk evalueren met een duplexechografie. Er bestaat geen enkel geneesmiddel dat de progressie van het kleplijden kan afremmen. Noch statines4 noch andere nieuwere geneesmiddelen doen dat.5 De enige therapeutische mogelijkheid is chirurgische vervanging van de aortaklep door een mechanische of biologische kunstklep. Dankzij TAVI (transkatheter aortaklepimplantatie), een percutane techniek, kunnen we nu ook patiënten met een hoog risico, een matig risico en zelfs een laag risico behandelen, met weinig complicaties.6
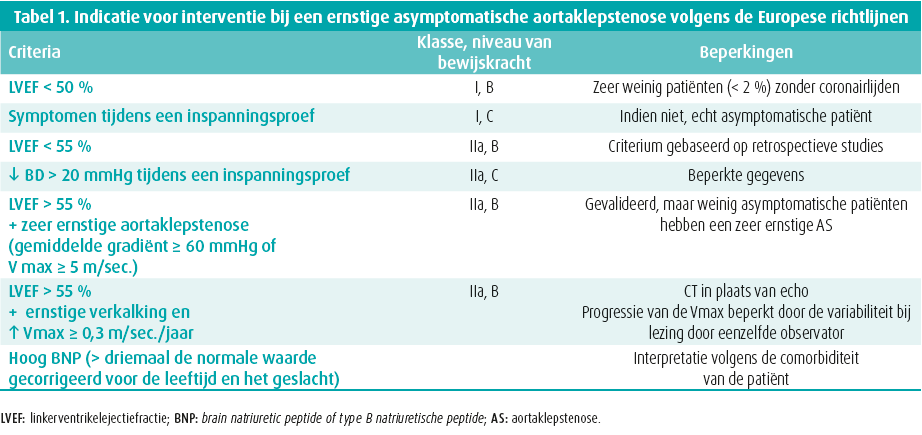
De Europese en de Amerikaanse richtlijnen zijn het eens over de indicatie tot vervanging van de aortaklep bij patiënten met een ernstige aortaklepstenose, meer bepaald als ze symptomen vertonen (en als die toe te schrijven zijn aan aortaklepstenose) of als de linkerventrikelfunctie (LVEF) < 50 % is.7, 8 Er is meer discussie over het beleid bij asymptomatische patiënten met een ernstige aortaklepstenose. Tabel 1 vat de huidige indicaties samen (criteria, klasse, niveau van bewijskracht en beperkingen).
Plaatsing van een aortakunstklep is geïndiceerd (klasse I) als de LVEF < 50 % is of als de patiënt nog een andere hartoperatie moet ondergaan (klasse I). Als de patiënt symptomen krijgt tijdens een inspanningsproef (intense dyspneu, angina pectoris, flauwte en zeker syncope) is plaatsing van een aortakunstklep ook geïndiceerd (klasse I). Men kan dergelijke patiënten echter niet als echt asymptomatische patiënten beschouwen.
Bij asymptomatische patiënten met een ernstige AS moet men zo nodig de risico's en de mogelijke voordelen ramen. De beslissing wordt door een multidisciplinair 'hartteam' genomen, idealiter in een kliniek voor hartkleplijden.9 Dat team moet meerdere vragen beantwoorden.
Heeft de patiënt echt geen symptomen?
Veel patiënten, vooral ouderen en vrouwen, 10 verminderen geleidelijk hun fysieke activiteiten om symptomen te vermijden. Sommige patiënten vertellen niets over hun symptomen of zeggen soms dat ze geen symptomen hebben. Daarom is een inspanningsproef aanbevolen bij het opsporen van symptomen of om te bevestigen dat de patiënt effectief geen symptomen heeft. Volgens meerdere studies ontwikkelt minstens een derde van de patiënten die beweren geen symptomen te hebben, symptomen tijdens een inspanningsproef en komen ze dus in aanmerking voor een interventie.11 Een normale inspanningsproef heeft een hoge negatieve voorspellende waarde. Slechts een minderheid van die patiënten zal symptomen vertonen na een follow-up van 12 maanden. De positieve voorspellende waarde is goed (79 %) bij patiënten van minder dan 70 jaar, maar is 57 % bij oudere patiënten.12 Volgens een Europese enquête is slechts bij een minderheid van de asymptomatische patiënten met een ernstige AS (6,1 %) een inspanningsproef uitgevoerd.13
Is de AS echt ernstig?
We spreken over een ernstige AS als de pieksnelheid ≥ 4 m/sec. is, de gemiddelde drukgradiënt over de klep ≥ 40 mmHg en de opening van de klep < 1 cm² (of < 0,6 cm²/m²) is. De opening kan worden onderschat en de ernst van de AS overschat als de diameter van de linkerventrikeluitstroombaan wordt onderschat (in de tweede macht in de continuïteitsvergelijking). De uitstroombaan is immers vaak ovaal en niet bolvormig, en bij een 2D-echocardiografie meet men de kleine diameter. Omgekeerd kan de drukgradiënt worden overschat door een fenomeen van drukrecuperatie. Ook kunnen de pieksnelheid en dus de drukgradiënt worden overschat als niet alle akoestische vensters worden geanalyseerd, vooral parasternaal rechts. Vaak ziet men een discordantie tussen de criteria (kleine opening en een matige drukgradiënt). Men moet meetfouten uitsluiten en extra metingen uitvoeren, zoals de permeabiliteitsindex, de verhouding tussen de maximale bloedstroom onder de aortaklep en die over de klep (< 0,25) en de calciumscore op een CT-scan (> 1 200 AU bij vrouwen en > 2 000 bij mannen).
Wat is de optimale timing voor een interventie?
Als de eerste horde genomen is (bevestiging van de ernst van de AS, uitsluiten van meetfouten en bevestiging van het asymptomatische karakter van de AS door een normale inspanningsproef), moet men de risicomarkers van een ongunstige evolutie op korte termijn opsporen (tabel 2).

Een te vroege interventie kan de patiënt blootstellen aan een risico op complicaties op lange termijn als gevolg van de kunstklep: kleptrombose, trombo-embolie, hemolyse, verslechtering van de biologische klep en eventuele noodzaak tot een nieuwe ingreep. Vroege complicaties van de interventie zijn: overlijden tijdens of kort na de procedure, bloeding, noodzaak tot plaatsing van een pacemaker, coronaire obstructie, CVA, paravalvulair lek, ontkoppeling tussen de patiënt en de prothese (de kunstklep is te klein voor de patiënt).
Een interventie bij een patiënt die echt geen symptomen heeft, zal uiteraard de levenskwaliteit niet verbeteren. Het risico op plotselinge dood is laag (< 1 % per jaar), dus lager dan het overlijdensrisico bij chirurgische plaatsing van een aortakunstklep.
Een vroegere interventie kan echter toch gewettigd zijn om meerdere redenen. Bij een ernstige AS kan het moeilijk zijn om de symptomen te evalueren. Misschien wordt de patiënt niet genoeg gevolgd: een derde van de asymptomatische patiënten met een ernstige AS komt minder dan één keer per jaar terug op spreekuur, en dat correleert met een hogere sterfte.14 Dat ziet men ook bij patiënten die om de zes maanden in een kliniek voor hartkleplijden worden gevolgd. Ze komen niet op spreekuur zodra ze symptomen krijgen. Soms is dat toe te schrijven aan mobiliteitsproblemen. Er is overigens een risico op irreversibele LV-disfunctie door fibrose van het myocard.15 Andere schadelijke gevolgen zijn een disfunctie van de linkervoorkamer, mitralisklepinsufficiëntie, pulmonale hypertensie en rechterventrikelfalen. Die markers van een ongunstige evolutie worden waargenomen bij meer dan de helft van de asymptomatische patiënten met een ernstige of matige AS.16 Het risico is hoog als de tijd tussen het verschijnen van de symptomen en de interventie te lang is.17 Bij een ernstige AS zal nagenoeg altijd een interventie vereist zijn, tenzij die zinloos zou zijn.18-20
Gecontroleerde studies
Er zijn twee gerandomiseerde, gecontroleerde studies gepubliceerd. De eerste is uitgevoerd bij 145 patiënten die werden gerandomiseerd naar chirurgische plaatsing van een aortakunstklep of geen interventie (controlegroep).21 Een van de items van het samengestelde eindpunt van overlijden tijdens de eerste 30 dagen of cardiovasculaire sterfte tijdens de hele follow-up is waargenomen bij 1 patiënt bij wie een aortakunstklep was ingeplant en bij 11 (15,2 %) van de 72 patiënten van de controlegroep. In die groep bedroeg de incidentie van plotselinge dood 4 % na vier jaar en 14 % na acht jaar. In de groep met een kunstklep is geen enkele patiënt overleden tijdens de operatie. Ook bij de patiënten van de controlegroep bij wie chirurgie is uitgevoerd wegens een acute decompensatie (17 %) is geen enkele patiënt overleden tijdens de operatie. Dat zijn uitzonderlijke resultaten. Ze zullen echter niet noodzakelijk goed zijn in alle chirurgische diensten. Zwakke punten van de studie waren: de studie is uitgevoerd bij vrij jonge patiënten (gemiddelde leeftijd: 64 jaar), van wie de meesten een bicuspide aortaklep hadden; de AS was bij alle patiënten zeer ernstig (pieksnelheid > 5 m/sec.). Sommige patiënten die symptomen hebben ontwikkeld, zijn niet geopereerd.
De tweede studie, de AVATAR-studie (Aortic Valve Replacement Versus Conservative Treatment in Asymptomatic Severe Aortic Stenosis), is uitgevoerd bij 157 patiënten van gemiddeld 67 jaar met een ernstige AS, een normale LVEF en een negatieve inspanningsproef.22 Het primaire eindpunt was een samengesteld eindpunt van overlijden ongeacht de doodsoorzaak, acuut myocardinfarct, CVA, ziekenhuisopname wegens hartfalen. Het risico op optreden van een van de items van het samengestelde eindpunt was lager in de chirurgische groep (relatief risico: 0,46). De sterfte in de chirurgische groep was 1,4 %. Het aantal patiënten was vrij klein en de studie is voortijdig stopgezet. Vaak gaat dat samen met een overschatting van het gunstige effect. De cardiovasculaire sterfte was vergelijkbaar (9,54 % in de vroegechirurgie-groep en 9,09 % in de controlegroep). Pas na 18 maanden gingen de curven van de totale sterfte en hartfalen uit elkaar. De indicaties voor electieve chirurgie in de controlegroep waren het verschijnen van symptomen (60 %), verergering van de AS (16 %) en daling van de LVEF (4 %). Die drie criteria kan men makkelijk herkennen bij een regelmatige follow-up om de zes maanden.
Er lopen ook grotere gecontroleerde studies: ESTIMATE (Early Surgery For Patients With Asymptomatic Severe AS), early TAVR (Evaluation Of Transcatheter Aortic Valve Replacement Compared To Surveillance For Patients With Asymptomatic Severe AS), EASY-AS (Early Valve Replacement In Severe, Asymptomatic Aortic Stenosis Study) en EVOLVED (Early Valve Replacement Guided By Biomarkers Of Left Ventricular Decompensation In Patients With Asymptomatic Severe Aortic Stenosis). Die studies zullen respectievelijk 360, 901, 2 844 en 1 000 patiënten rekruteren. Ze zullen zeker duidelijkheid scheppen over de ideale timing voor een interventie.
Chirurgie of transkatheterbehandeling?
De huidige richtlijnen stellen nog geen TAVI voor bij asymptomatische patiënten. We verwachten de resultaten van de Early TAVR-studie tegen maart 2024. Die zouden de zaken weleens kunnen veranderen.
De beslissing moet worden genomen door een 'hartteam', een multidisciplinaire groep met een cardioloog, een interventioneel cardioloog, een hartchirurg, een specialist in beeldvorming en monitoring tijdens de interventie, een anesthesist en andere specialisten naargelang de kenmerken van de patiënt. De patiënt moet informatie krijgen over de risico's en de te verwachten gunstige effecten en men moet rekening houden met zijn voorkeur. Ook bij asymptomatische patiënten met risicomarkers moet men een keuze maken tussen chirurgie en TAVI.
De incidentie van ernstige AS zal de komende jaren en decennia sterk stijgen. Dat zou kunnen uitmonden in een overbelasting van de afdelingen voor interventionele cardiologie en hartchirurgie, vooral als de patiënten niet op individuele basis worden geëvalueerd. De wachttijd dreigt zo langer te worden.
Naar schatting wordt een derde van de symptomatische patiënten met een ernstige AS en een klasse I-indicatie niet behandeld met chirurgie of TAVI. Omgekeerd wordt vaak een TAVI uitgevoerd bij patiënten die daar allicht weinig baat bij zullen vinden.
Conclusies
De vragen 'wie', 'wanneer' en 'hoe' moet men stapsgewijs bij elke patiënt afzonderlijk beantwoorden:
- Hoe ernstig is de aortaklepstenose en betreft het wel degelijk een asymptomatische aortaklepstenose?
- Risicomarkers opsporen: zeer ernstige aortaklepstenose, ernstige verkalking van de klep en snelle verergering, zeer hoog NT-proBNP-gehalte, LVEF < 55 %, totale longitudinale vervorming < 15 %.22
- Zijn het overlijdensrisico en het risico op complicaties als gevolg van de procedure laag?
- Is de houdbaarheid van de geselecteerde prothese langer dan de levensverwachting van de patiënt?
Bij een aantal asymptomatische patiënten is een interventie niet noodzakelijk, maar men moet hen dan wel goed volgen (om de drie tot zes maanden) met een klinisch onderzoek, een echocardiografie en een laboratoriumonderzoek, idealiter in een kliniek voor hartklepziekten.
Referenties
- Nkomo, V.T., Gardin, J.M., Skelton, T.N., Skelton, T.N., Gottdiener, J.S., Scott, C.G. et al. Burden of valvular heart disease: a population-based study. The Lancet, 2006, 368 (9540), 1005-1011.
- Yagdir, S., Johnson, C.O., Aboyans, V., Adebayo, O.M., Adedoyin, R.A., Global, Regional, and National Burden of Calcific Aortic Valve and Degenerative Mitral Valve Diseases, 1990-2017. Circulation, 2020, 141 (21), 1670-1680.
- Timmis, A., Vardas, P., Townsend, N., Torbica, A., Katus, H., De Smedt, D. et al. European Society of Cardiology: cardiovascular disease statistics 2021. Eur Heart J, 2022, 43 (8), 716-799.
- Zhao, Y., Nicoll, R., He, Y.H., Henein, M.Y. The effect of statins therapy in aortic stenosis: Meta-analysis comparison data of RCTs and observationals. Data Brief, 2016, 7, 357-361.
- Pawade, T.A., Doris, M.K., Bing, R., White, A.C., Forsyth, L., Evans, E. et al. Effect of Denosumab or Alendronic Acid on the Progression of Aortic Stenosis: A Double-Blind Randomized Controlled Trial. Circulation, 2021, 143 (25), 2418-2427.
- Vahanian, A., Beyserdorf, F., Praz, F., Milojevic, M., Baldus, S., Bauersachs, J. et al. 2021 ESC/EACTS Guidelines for the management of valvular heart disease. Eur Heart J, 2022, 43 (7), 561-632.
- Otto, C.M., Nishimura, R.A., Bonow, R.O., Carabello, B.A., Erwin, J.P., Gentile, F. et al. 2020 ACC/AHA Guideline for the Management of Patients With Valvular Heart Disease: Executive Summary: A Report of the American College of Cardiology/ American Heart Association Joint Committee on Clinical Practice Guidelines. Circulation, 2020, 143 (5), e72e227.
- Zilberszac, R., Lancellotti, P., Gilon, D., Gabriel, H., Schemper, M., Maurer, G. et al. Role of a heart valve clinic programme in the management of patients with aortic stenosis. Eur Heart J Cardiovasc Imaging, 2017, 18 (2), 138-144.
- Desjardin, J.T., Chikwe, J., Hahn, R.T., Hung, J.W., Delling, F.N. Sex Differences and Similarities in Valvular Heart Disease. Circ Res, 2022, 130 (4), 455-473.
- Rafique, A.M., Biner, S., RayI, I., Forrester, J.S., Tolstrup, K., Siegel, R.J. Meta-analysis of prognostic value of stress testing in patients with asymptomatic severe aortic stenosis. Am J Cardiol, 2009, 104 (7), 972-977.
- Das, P., Rimington, H., Chambers, J. Exercise testing to stratify risk in aortic stenosis. Eur Heart J, 2005, 26 (13), 1309-1313.
- Lung, B., Delgado, V., Rosenhek, R. et al. EORP VHDII investigators. Contemporary Presentation and Management of Valvular Heart Disease: The EURObservational Research Programme Valvular Heart Disease II Survey. Circulation, 2019, 140 (14), 1156-1165.
- Ahmed, S.V., Sorajja, P., Garberich, R.F., Farivar, R.S. Harris, K.M., Gössl, M. Association of Guideline Adherence for Serial Evaluations With Survival and Adverse Clinical Events in Patients With Asymptomatic Severe Aortic Stenosis. JAMA Cardiol, 2017, 2 (10), 1141-1146.
- Kwak, S., Everett, R.J., Treibel, T.A., Yang, S., Hwang, D., Ko, T. et al. Markers of Myocardial Damage Predict Mortality in Patients With Aortic Stenosis. J Am Coll Cardiol, 2021, 78 (6), 545-558.
- Tastet, L., Tribouilloy, C., Maréchaux, S., Mara Vollema, E., Delgado, V., Salaun, E. et al. Staging Cardiac Damage in Patients With Asymptomatic Aortic Valve Stenosis. J Am Coll Cardiol, 2019, 74 (4), 550-563.
- Elbaz-Greener, G., Masih, S., Fang, J., Ko, D.T., Lauck, S.B., Webb, J.G. et al. Temporal Trends and Clinical Consequences of Wait Times for Transcatheter Aortic Valve Replacement: A Population-Based Study. Circulation, 2018, 138 (5), 483-493.
- Puri, R., Iung, B., Cohen, D.J., Rodés-Cabau, J. TAVI or No TAVI: identifying patients unlikely to benefit from transcatheter aortic valve implantation. Eur Heart J, 2016, 37 (28), 2217-2225.
- Parik, P.B. Predicting Futility in Aortic Stenosis: What's the Holdup? J Am Coll Cardiol, 2022, 80 (8), 801-803.
- Minha, S., Marcus, G. Can We Truly Predict Futility for TAVR Based on Pre-Procedural Indices? Cardiovasc Revasc Med, 2021, 23, 77-78.
- Kang, D.H., Park, S.J., Lee, S.A. Lee, S., Kim, D-H., Kim, H-K. et al. Early Surgery or Conservative Care for Asymptomatic Aortic Stenosis. N Engl J Med, 2020, 382 (2), 111-119.
- Banovic, M., Putnik, S., Penicka, M., Doros, G., Deja, M.A., Kockova, R. et al. Aortic Valve Replacement Versus Conservative Treatment in Asymptomatic Severe Aortic Stenosis: The AVATAR Trial. Circulation, 2022, 145 (9), 648-658.
- Magne, J., Cosyns, B., Popescu, B.A., Carstensen, H.G., Dahl, J., Desai, M.Y. et al. Distribution and Prognostic Significance of Left Ventricular Global Longitudinal Strain in Asymptomatic Significant Aortic Stenosis: An Individual Participant Data Meta-Analysis. JACC Cardiovasc Imaging, 2019, 12 (1), 84-92.
Aucun élément du site web ne peut être reproduit, modifié, diffusé, vendu, publié ou utilisé à des fins commerciales sans autorisation écrite préalable de l’éditeur. Il est également interdit de sauvegarder cette information par voie électronique ou de l’utiliser à des fins illégales.