Cet article est un compte rendu de la session consacr ée à l 'imagerie multimodale lors du congr ès de la BSC 2018, au cours de laquelle le Pr Habib, le Dr Bucciarelli et le Pr Van Camp ont trait é de l 'utilisation de l 'imagerie multimodale, respectivement en cas de cardiomyopathie restrictive, hypertrophique et isch émique. Lors de cette session, l 'accent a ét é mis sur l 'imagerie dans le cadre du diagnostic et de la d étermination de l ' étiologie des diff érentes cardiomyopathies. Enfin, le Dr Claeys a analys é les r ésultats de son étude au sujet des effets du sild énafil sur la r ésistance vasculaire pulmonaire et la r éserve contractile ventriculaire droite en cas de maladie thromboembolique chronique (CTED).
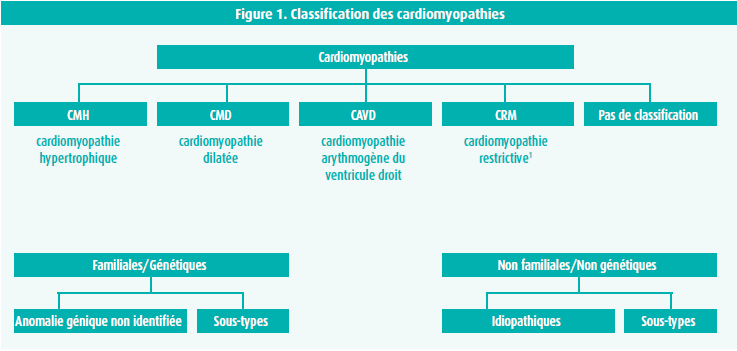
Une cardiomyopathie est une affection caract éris ée par des anomalies structurelles et fonctionnelles du muscle cardiaque, en l 'absence de maladie coronarienne, d 'hypertension, de valvulopathies ou de malformations cong énitales. Les cardiomyopathies sont class ées en diff érents groupes, en fonction de leur morphologie et du ph énotype fonctionnel, et sont subdivis ées en formes familiales et non familiales (figure 1).1
Cardiomyopathie restrictive
Les cardiomyopathies restrictives (CMR) sont caract éris ées par une physiologie ventriculaire restrictive ( él évation des pressions de remplissage ventriculaires suite à une augmentation de la rigidit é du myocarde) en pr ésence de volumes diastoliques normaux ou diminu és (d 'un ou des deux ventricules), de volumes systoliques normaux ou diminu és et d 'une épaisseur normale des parois ventriculaires. Les CMR constituent un groupe divers de maladies myocardiques avec un large spectre d ' étiologies, tant familiales ou g én étiques qu 'acquises. Plusieurs techniques d 'imagerie jouent un r ôle important sur le plan du diagnostic, du pronostic et du traitement des CMR.1
L ' échocardiographie r év èle typiquement une dysfonction diastolique et des oreillettes dilat ées (volume auriculaire gauche index é > 50 ml/m2). Le flux transmitral est de type restrictif avec un rapport E/A ≥ 2,0, un temps de d éc él ération court, ≤ 150 ms, et un temps de relaxation isovolum étrique ≤ 60-70 ms. Le flux veineux pulmonaire montre une onde S < D, la vitesse de l 'onde A est > 35 cm/s et Ap-Am est > 30 ms. Le Doppler tissulaire (TDI) r év èle une diminution des v élocit és E ' septales et lat érales < 3-4 cm/s et un rapport E/E ' > 14.
L 'IRM cardiaque (RMC) peut être utilis ée pour le typage tissulaire (T1 pour la graisse, T2 pour l 'oed ème, T2* pour les d ép ôts de fer) et la mesure pr écise des volumes et fonctions. Les diff érents types de LGE (Late Gadolinium Enhancement, rehaussement tardif) contribuent également au diagnostic diff érentiel des CMR (voir ci-dessous).
Le CT scan cardiaque (anatomie, p éricarde et observations extracardiaques), l 'imagerie nucl éaire (amylo ïdose et sarco ïdose) et les biopsies myocardiques peuvent également faciliter le diagnostic de certains types de CMR.
Voici quelques exemples de sous-types de cardiomyopathies restrictives avec leurs anomalies typiques aux diff érentes techniques d 'imagerie:
- CMR idiopathiques. L ' échocardiographie montre des oreillettes morphologiquement dilat ées et des ventricules non hypertrophiques, non dilat és, avec une fonction systolique normale du ventricule gauche (VG). Le remplissage au Doppler est de type restrictif. Le Doppler tissulaire (TDI) aide à la gradation de la fonction diastolique et au diagnostic diff érentiel avec une p éricardite constrictive (CMR E ' < 8 cm/s, E/E ' > 15, p éricardite constrictive E ' > 8 cm/s, E/E ' < 15).
- Amylo ïdose. L ' échocardiographie montre une hypertrophie du VG, non dilat é, et du septum interauriculaire avec un aspect mouchet é du myocarde, des valves épaissies et des oreillettes dilat ées. L 'analyse du 2D-strain montre des param ètres systoliques perturb és (essentiellement le strain longitudinal) avec un apex relativement épargn é (d ép ôts d 'amylo ïde pr éf érentiels dans les segments basaux). Les clich és d 'IRM r év èlent un rehaussement sous-endocardique circonf érentiel ou un rehaussement mid-myocardique (aspect 'en z èbre ').2 La scintigraphie permet de diagnostiquer une amylo ïdose et de diff érencier les divers sous-types (sensibilit é (97 %) et sp écificit é (100 %) tr ès élev ées de la scintigraphie pour la forme TTR de l 'amylo ïdose).3
- Maladie de Fabry. L ' échocardiographie montre une hypertrophie concentrique non obstructive en l 'absence d 'hypertension art érielle. On observe des vitesses r éduites au Doppler tissulaire. Les clich és d 'IRM avec un LGE r év èlent essentiellement un rehaussement des segments inf éro-lat éraux, m édians et basaux.
- Ch émotoxicit é. L ' échocardiographie r év èle un remodelage excentrique du VG avec dilatation, amincissement pari étal, fonction diastolique restrictive perturb ée et finalement aussi d ét érioration de la fonction systolique.4 Le strain longitudinal global (GLS) est un bon param ètre pour la d étection pr écoce d 'une dysfonction infraclinique du VG (diminution du GLS > 15 % par rapport à la valeur initiale).
- Fibrose endomyocardique. L ' échocardiographie r év èle une oblit ération apicale du ventricule gauche et/ou droit, un épaississement endocardique et un remplissage de type restrictif. La RMC avec un LGE constitue la r éf érence pour le diagnostic de la fibrose endomyocardique, et r év èle un rehaussement de l 'endocarde, essentiellement au niveau de l 'apex et des chambres d 'entr ée des deux ventricules. Le signe en V typique au niveau de l 'apex du VG montre un myocarde à 3 couches, un endomyocarde fibreux épaissi et un thrombus.6
Comme nous l 'avons indiqu é ci-dessus, l 'imagerie multimodale est importante pour la d étermination du diagnostic et du pronostic d 'une CMR. Par ailleurs, des examens compl émentaires tels qu 'une biopsie endomyocardique, un d épistage familial et des études g én étiques sont fr équemment n écessaires.
Cardiomyopathie hypertrophique
La cardiomyopathie hypertrophique (CMH) repr ésente une cause majeure d 'hypertrophie ventriculaire gauche (HVG) inexpliqu ée, qui a également un effet sur d 'autres structures cardiaques telles que l 'appareil valvulaire mitral, les coronaires et l 'interstitium cardiaque. La CMH est le plus souvent une affection b énigne, mais elle peut également entra îner une mort subite, une insuffisance cardiaque, une fibrillation auriculaire et une isch émie myocardique.
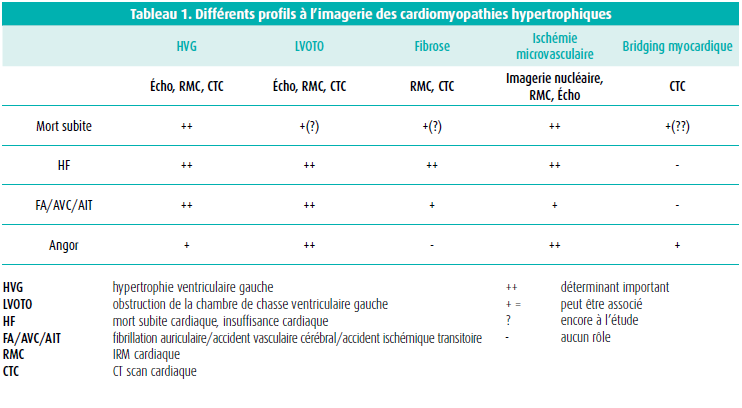
Les techniques d 'imagerie multimodale ( échocardiographie, RM cardiaque, CT scan cardiaque et imagerie nucl éaire) peuvent s 'av érer utiles pour le diagnostic et le traitement des diff érents profils cliniques des CMH (cf. tableau 1). Plus de 50 % des patients ont des anomalies au niveau de l 'appareil valvulaire mitral (> 25 % ont des anomalies des cordages), 33 % des patients ont une obstruction de la chambre de chasse ventriculaire gauche (LVOTO) (gradient max > 30 mmHg au repos ou lors de manoeuvres de provocation (Valsalva)).
Il faut r éaliser une échocardiographie tous les ans ou tous les deux ans chez les patients stables, et une RMC au moins une fois apr ès le diagnostic d 'une CMH. L ' échocardiographie est utilis ée en premi ère ligne, mais elle peut être compl ét ée d 'une RMC en cas de r ésultats douteux, d ' échographie suboptimale, d 'anomalies à l 'ecg avec une échographie normale et dans des familles ayant une échocardiographie non diagnostique.
L ' échocardiographie donne des informations au sujet de l ' épaisseur pari étale (> 15 mm, > 13 mm chez les parents au premier degr é), de la pr ésence d 'une hypertrophie septale asym étrique ou d 'une hypertrophie ventriculaire droite, des dimensions de la cavit é ventriculaire gauche, de la fonction systolique et diastolique, de la pr ésence d 'une obstruction de la LVOT et d 'un mouvement systolique ant érieur (SAM). Les mesures doivent être pr écises, effectu ées en fin de diastole et à plusieurs niveaux en vue petit axe, si n écessaire avec adjonction de contraste. La RM cardiaque se r év èle sup érieure pour la d étermination de l 'HVG (volume, masse), pour la distribution de l 'hypertrophie (asym étrique ou non, apicale ou non), la pr ésence d 'une obstruction de la LVOT ou mi-cavitaire et l 'implication de l 'appareil valvulaire mitral. Le degr é et la distribution de la fibrose (LGE) contribuent au diagnostic diff érentiel des CMH: en cas de CMH, le rehaussement se situe essentiellement au niveau des points d 'insertion ventriculaires droits et au niveau intramural. En outre, la quantit é de fibrose est un signe de progression de la maladie, et donc un él ément pr édictif d 'arythmies.8 On a sugg ér é d 'ajouter éventuellement ceci à l 'avenir au calculateur de mort subite en cas de CMH (Soci ét é europ éenne de Cardiologie) (http://www. doc2do.com/hcm/webHCM.html).
Cardiomyopathie isch émique
Lors de la session consacr ée à l 'imagerie multimodale en cas de cardiomyopathie isch émique (CMI), l 'accent a ét é mis sur l 'imagerie pour la d étection de l 'isch émie en cas de maladies coronariennes stables. Chez les patients ayant des plaintes suspectes de maladie coronarienne stable, il faut r éaliser le bilan standard suivant: ecg au repos, analyse de sang, échocardiographie au repos et éventuellement un Holter. Par apr ès, il faut suivre un plan en 3 étapes:
Tout d 'abord, il faut d éterminer la probabilit é pr étest (PPT). En cas de PPT faible (< 15 %) ou élev ée (> 85 %), un test (de stress) non invasif a peu de sens, car le risque de maladie coronarienne stable reste respectivement faible et élev é, ind épendamment du r ésultat du test. Ensuite, le diagnostic de maladie coronarienne stable peut être pos é au moyen (d 'une combinaison) de tests non invasifs (CT scan coronaire, ergom étrie et imagerie de stress avec échocardiographie, RMC, SPECT ou PET) chez les patients ayant une PPT interm édiaire de 15-85 %. Enfin, il est important d ' évaluer le risque d ' év énement pour d éterminer s 'il faut pratiquer une revascularisation (en cas de risque élev é d ' év énement avec une mortalit é ≥ 3 %/an ou éventuellement en cas de risque interm édiaire, 1-3 %/an).9 Un traitement m édicamenteux optimal reste en effet la pierre angulaire du traitement, étant donn é que l ' étude COURAGE a d émontr é que la survie des patients souffrant d 'isch émie prouv ée, chez qui on implantait un stent, n ' était pas meilleure que celle des patients recevant un traitement m édicamenteux optimal.10, 11 La mesure invasive de la r éserve coronaire (Fractional Flow Reserve, FFR) avec une valeur < 0,80 correspond à une st énose susceptible d 'induire de l 'isch émie à l 'effort, et qui a donc int ér êt à être revascularis ée (meilleurs r ésultats en cas de revascularisation). Les patients ayant des tests d 'isch émie non invasifs anormaux ont toutefois souvent une FFR normale. Les études DEFER et FAME-I ont d émontr é qu 'il est plus sûr de ne pas revasculariser si la FFR est n égative.12, 13 Le CT scan cardiaque coupl é à la FFR semble prometteur pour le futur, et il doit être compar é aux tests d 'isch émie non invasifs classiques dans des études randomis ées.9
Pour terminer cette session au sujet de l 'imagerie multimodale, le Dr Claeys (UZ Leuven) a pr ésent é son étude au sujet de l 'effet du sild énafil chez les patients souffrant d 'une maladie thromboembolique chronique (CTED). Ces patients ont une capacit é à l 'effort r éduite, en d épit de l 'absence d 'hypertension pulmonaire au repos. Les tests de stress peuvent r év éler une maladie l ég ère (r ésistance vasculaire pulmonaire anormale avec une pente P/Q > 3 mmHg.L-1.min et des anomalies de la r éserve contractile du ventricule droit). Le sild énafil peut am éliorer la capacit é à l 'effort en diminuant la postcharge ventriculaire droite, proportionnellement à la s év érit é de la maladie.
L 'imagerie multimodale est importante pour la d étermination du diagnostic, pour le diagnostic diff érentiel et le pronostic des diff érentes cardiomyopathies. De plus amples études devront encore d émontrer quelle combinaison de techniques d 'imagerie est pr éf érable pour chaque forme de cardiomyopathie. à l 'avenir, on pourra peut être int égrer un LGE à la RMC (signant donc une fibrose) dans le calculateur de mort subite en cas de CMH. Une isch émie en cas de CMI peut être d étect ée par des tests de stress non invasifs mais, pour le moment, on ne dispose pas d ' études d émontrant que les personnes revascularis ées sur la base de ces tests obtiennent de meilleurs r ésultats que les personnes sous traitement m édicamenteux optimal. La FFR invasive a prouv é que la revascularisation donne de meilleurs r ésultats. Pour cette raison, un CT avec FFR semble prometteur à l 'avenir, mais de plus amples études sont en cours.
R éf érences
- Elliott, P., Andersson, B., Arbustini, E. et al. Classification of the cardiomyopathies: a position statement from the european society of cardiology working group on myocardial and pericardial diseases. Eur Heart J, 2007, 29, 270-276. doi:10.1093/eurheartj/ ehm342.
- Habib, G., Bucciarelli-Ducci, C., Caforio, A.L.P. et al. Multimodality imaging in restrictive cardiomyopathies: an EACVI expert consensus document. Eur Heart J - Cardiovasc Imaging, 2017, 18, 1090-1121. doi:10.1093/ ehjci/jex034.
- Di Bella, G., Pizzino, F., Minutoli, F. et al. The mosaic of the cardiac amyloidosis diagnosis: role of imaging in subtypes and stages of the disease. Eur Heart J - Cardiovasc Imaging, 2014, 15, 1307-1315. doi:10.1093/ehjci/ jeu158.
- Habib, G., Bucciarelli-Ducci, C., Caforio, A.L.P. et al. Multimodality imaging in restrictive cardiomyopathies: an EACVI expert consensus document. Eur Heart J - Cardiovasc Imaging, 2017, 18, 1090-1121. doi:10.1093/ ehjci/jex034.
- Plana, J.C., Galderisi, M., Barac, A. et al. Expert consensus for multimodality imaging evaluation of adult patients during and after cancer therapy: a report from the American Society of Echocardiography and the European Association of Cardiovascular Imaging. J Am Soc Echocardiogr, 2014, 27, 911-939. doi:10.1016/j.echo.2014.07.012.
- Salemi, V.M.C., Rochitte, C.E., Shiozaki, A.A. et al. Late gadolinium enhancement magnetic resonance imaging in the diagnosis and prognosis of endomyocardial fibrosis patients. Circ Cardiovasc Imaging, 2011, 4, 304-311. doi:10.1161/CIRCIMAGING. 110.950675.
- Cardim, N., Galderisi, M., Edvardsen, T. et al. Role of multimodality cardiac imaging in the management of patients with hypertrophic cardiomyopathy: an expert consensus of the European Association of Cardiovascular Imaging Endorsed by the Saudi Heart Association. Eur Heart J - Cardiovasc Imaging, 2015, 16, 280-280. doi:10.1093/ehjci/jeu291.
- Cardim, N., Galderisi, M., Edvardsen, T. et al. Role of multimodality cardiac imaging in the management of patients with hypertrophic cardiomyopathy: an expert consensus of the European Association of Cardiovascular Imaging Endorsed by the Saudi Heart Association. Eur Heart J - Cardiovasc Imaging, 2015, 16, 280-280. doi:10.1093/ehjci/jeu291.
- Montalescot, G., Sechtem, U., Achenbach, S. et al. 2013 ESC guidelines on the management of stable coronary artery disease. Eur Heart J, 2013, 34, 2949-3003. doi:10.1093/eurheartj/eht296.
- Boden, W.E., O 'Rourke, R.A., Teo, K.K. et al. Optimal medical therapy with or without PCI for stable coronary disease. N Engl J Med, 2007, 356, 1503-1506. doi:10.1056/NEJMoa070829.
- Shaw, L.J., Berman, D.S., Maron, D.J. et al. Optimal medical therapy with or without percutaneous coronary intervention to reduce ischemic burden: results from the Clinical Outcomes Utilizing Revascularization and Aggressive Drug Evaluation (COURAGE) trial nuclear substudy. Circulation, 2008, 117, 1283-1291. doi:10.1161/CIRCULATIONAHA.107.743963.
- Pijls, N.H.J., van Schaardenburgh, P., Manoharan, G. et al. Percutaneous Coronary Intervention of Functionally Nonsignificant Stenosis: 5-Year Follow-Up of the DEFER Study. J Am Coll Cardiol, 2007, 49, 2105-2111. doi:10.1016/J.JACC.2007.01.087.
- De Bruyne, B., Fearon, W.F., Pijls, N.H.J. et al. Fractional Flow Reserve -Guided PCI for Stable Coronary Artery Disease. N Engl J Med, 2014, 371, 1208-1217. doi:10.1056/NEJMoa1408758.
Aucun élément du site web ne peut être reproduit, modifié, diffusé, vendu, publié ou utilisé à des fins commerciales sans autorisation écrite préalable de l’éditeur. Il est également interdit de sauvegarder cette information par voie électronique ou de l’utiliser à des fins illégales.