Compte rendu d'une session de la BSC - session 21
Lors du 40e congrès annuel de la Belgian Society of Cardiology, une session a traité de sujets d'actualité dans le domaine de l'insuffisance cardiaque. Le rôle du traitement martial et l'importante étude AFFIRMAHF ont été abordés lors de la première partie. La deuxième partie a quant à elle porté sur le traitement de l'hyperkaliémie en cas d'insuffisance cardiaque. Voici un compte rendu de cette session.
Traitement martial en cas d'insuffisance cardiaque
Anne-Catherine Pouleur (Cliniques Universitaires Saint-Luc, Bruxelles)
La carence en fer - définie comme une concentration de ferritine inférieure à 100 μg/dl ou une concentration de ferritine comprise entre 100 et 299 μg/dl en association avec une saturation de la transferrine inférieure à 20 % - est un problème fréquent, dont la prévalence atteint 30 à 50 % chez les patients atteints d'insuffisance cardiaque chronique et 50 à 80 % chez les patients atteints d'insuffisance cardiaque aiguë1. Cette carence en fer est associée à une réduction de la capacité à l'effort, à une diminution de la qualité de vie, à un risque accru d'hospitalisation et à une augmentation du risque de mortalité et des coûts de santé. L'effet d'une carence en fer sur le pronostic se manifeste chez les patients avec ou sans anémie. Toutefois, le traitement de la carence en fer à l'aide de préparations administrées par voie orale n'améliore pas le pronostic à court terme2. Ceci peut s'expliquer par la physiopathologie sous-jacente, dans laquelle l'insuffisance cardiaque inhibe l'absorption intestinale du fer par le biais de l'inflammation et de l'activation neuro-hormonale1. Ces dernières années, il a cependant été montré que le traitement de la carence en fer à l'aide d'une préparation de carboxymaltose ferrique administrée par voie intraveineuse pouvait améliorer la dyspnée d'effort, la capacité à l'effort et la qualité de vie des patients atteints d'insuffisance cardiaque à fraction d'éjection ventriculaire gauche réduite (HFrEF)3,4, et ce dernier a reçu une recommandation de classe IIa dans les directives européennes récentes5. L'étude AFFIRM-AHF a récemment évalué si le carboxymaltose ferrique administré par voie intraveineuse pouvait également améliorer le nombre d'hospitalisations dues à une insuffisance cardiaque ainsi que la mortalité chez les patients présentant une HFrEF et une carence en fer6.
L'étude AFFIRM-AHF était une étude randomisée en double aveugle, menée auprès de 1 108 patients hospitalisés en raison d'une insuffisance cardiaque, présentant une fraction d'éjection ventriculaire gauche (FEVG) inférieure à 50 % et une carence en fer. Elle a évalué l'effet du carboxymaltose ferrique sur un critère d'évaluation principal composite associant le nombre total d'hospitalisations pour cause d'insuffisance cardiaque et la mortalité cardiovasculaire. La population étudiée se caractérisait par une utilisation élevée de médicaments contre l'insuffisance cardiaque, mais aussi par un risque élevé, avec un NT-proBNP médian d'environ 4700 pg/ml. Environ la moitié des patients étaient également atteints d'anémie. Après un an, le critère d'évaluation principal avait diminué de 21 % (73/100 personnes-années, contre 57/100 personnes-années), mais ne remplissait pas les critères de significativité (p = 0,059) (figure 1). En outre, aucune différence n'était observée en ce qui concerne le critère d'évaluation principal dans différents sous-groupes. La présence d'une anémie, la FEVG, la concentration de NT-proBNP, le sexe, la fonction rénale, la concentration de ferritine et la saturation de la transferrine n'influençaient pas l'effet du carboxymaltose ferrique. Lorsque le critère d'évaluation principal a été scindé, une réduction significative de 26 % du nombre total d'hospitalisations pour cause d'insuffisance cardiaque (43/100 personnes-années, contre 32/100 personnes-années) a été observée, mais aucun effet sur la mortalité cardiovasculaire (16/100 personnes-années, contre 16/100 personnes-années). L'administration de carboxymaltose ferrique était sûre, sans différence avec le groupe recevant le placebo en ce qui concerne les événements indésirables. En raison de l'effet potentiel de la pandémie de Covid- 19 sur les résultats, une analyse de sensibilité, dans laquelle tous les patients ont été inclus, a été réalisée, mais seules les données antérieures à la pandémie ont été utilisées. Une réduction significative de 25 % du critère d'évaluation principal a été observée lors de cette analyse de sensibilité.
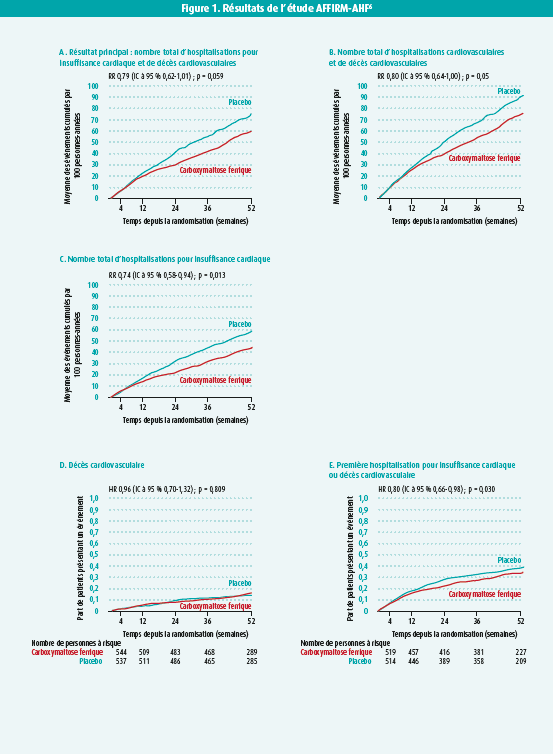
Durant la discussion qui a suivi la présentation, l'accent a été mis sur l'importance du dépistage de la carence en fer chez les patients insuffisants cardiaques. En outre, il est important de toujours traiter la carence en fer par voie intraveineuse. En résumé, l'étude AFFIRM-AHF a montré pour la première fois que l'administration de carboxymaltose par voie intraveineuse chez les patients à haut risque présentant une HFrEF et une carence en fer réduisait de 26 % le nombre d'hospitalisations pour insuffisance cardiaque. Cette étude a donc confirmé le rôle important de la carence en fer et de son traitement dans le cadre de la HFrEF.
Hyperkaliémie dans l'insuffisance cardiaque
Peter van der Meer (UMC Groningen, Pays-Bas)
L'hyperkaliémie (> 5,5 mmol/l) est fréquente chez les patients traités par inhibiteurs du système rénine-angiotensine- aldostérone (SRAA), qui sont l'une des pierres angulaires du traitement de l'insuffisance cardiaque. Bien que ces classes de médicaments aient montré lors de plusieurs études qu'elles pouvaient réduire la mortalité et le nombre d'hospitalisations pour cause d'insuffisance cardiaque chez les patients atteints d'HFrEF, l'augmentation de la posologie est souvent compliquée par l'hyperkaliémie. Lors d'études récentes dans lesquelles des inhibiteurs de l'enzyme de conversion de l'angiotensine (ACE) et des antagonistes des récepteurs de l'angiotensine (ARB) ont été combinés à des antagonistes des récepteurs des minéralocorticoïdes (MRA), une hyperkaliémie est survenue chez 12 à 16 % des patients7-9. Différents facteurs sont associés à un risque accru d'hyperkaliémie chez les patients insuffisants cardiaques : hypertension, âge avancé, fonction rénale dégradée, diabète, gravité de l'insuffisance cardiaque et médicaments tels que les inhibiteurs du SRAA10,11. Cependant, bien que l'hyperkaliémie soit associée à une mortalité plus élevée, le risque de mortalité reste inférieur chez les patients traités par MRA, par rapport au placebo12.
En outre, chez les patients dont la dose de traitement contre l'insuffisance cardiaque n'a pas été augmentée jusqu'au niveau optimal, la mortalité est plus élevée, et l'hyperkaliémie freine souvent l'augmentation de la dose des inhibiteurs du SRAA13.
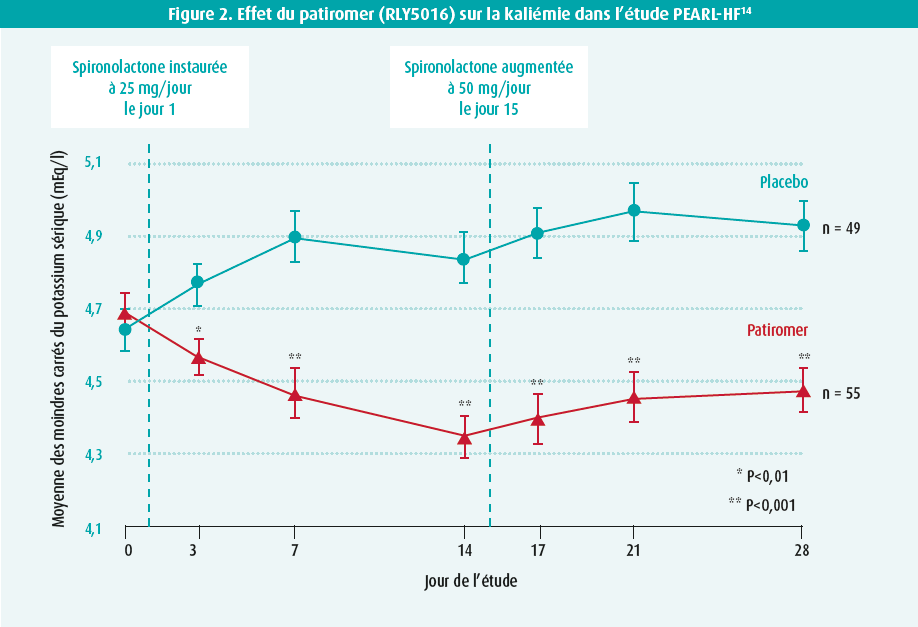
De nouveaux traitements de l'hyperkaliémie ont récemment été mis à disposition : le patiromer et le cyclosilicate de zirconium sodique (ZS-9). Tous deux sont des échangeurs ioniques qui échangent le calcium (patiromer) ou le sodium (ZS-9) contre du potassium dans le tube digestif. Il convient de se demander si le traitement de l'hyperkaliémie par ces médicaments pourrait faciliter l'augmentation de la dose d'inhibiteurs du SRAA et, ainsi, améliorer éventuellement le pronostic des patients. Voici déjà dix ans, l'étude randomisée PEARL-HF a évalué l'utilisation du patiromer chez 104 patients insuffisants cardiaques présentant des antécédents d'hyperkaliémie ou un débit de filtration glomérulaire (DFG) inférieur à 60 ml/min/1,73 m² et a pu montrer que le patiromer pouvait effectivement faire diminuer le taux de potassium de 0,45 mEq/l14 (figure 2). Il faut souligner que chez les patients qui ont reçu le patiromer, la dose de spironolactone était significativement plus souvent augmentée à 50 mg (91 %, contre 74 %). Jusqu'à présent, il n'existe toutefois aucune donnée probante indiquant que l'utilisation de fixateurs du potassium puisse améliorer le pronostic. L'étude DIAMOND (NCT03888066) évalue actuellement si le patiromer peut améliorer le critère d'évaluation composite de l'hospitalisation cardiovasculaire ou de la mortalité cardiovasculaire chez 2400 patients atteints d'HFrEF qui présentent une hyperkaliémie (> 5 mmol) sous traitement sous-optimal par inhibiteurs du SRAA ou qui ont présenté une hyperkaliémie au cours des douze derniers mois, ayant entraîné une diminution ou un arrêt de la dose d'inhibiteurs du SRAA. Tous les patients recevront du patiromer pendant un maximum de 12 mois. Durant cette période de démarrage, la dose d'inhibiteurs du SRAA sera augmentée jusqu'à la dose tolérée maximale. Ensuite, la moitié des patients sera randomisée pour arrêter le patiromer. Cette étude de phase III est en cours dans 439 centres à travers le monde et pourra apporter des réponses au sujet du rôle du patiromer dans le traitement de l'insuffisance cardiaque.
La discussion suivant la présentation a abordé l'importance du dépistage dans la pratique clinique. Actuellement, les inhibiteurs de l'ACE, les ARB et les MRA sont souvent prescrits sans contrôle de routine de la kaliémie et de la fonction rénale, ce qui comporte certains risques étant donné la prévalence élevée de l'hyperkaliémie et la mortalité accrue associée. Par conséquent, lors de l'instauration d'inhibiteurs du SRAA, un suivi de la kaliémie doit idéalement toujours être intégré dans la suite du plan de traitement.
Références
- Rocha, B.M.L., Cunha, G.J.L., Menezes Falcão, L.F. The Burden of Iron Deficiency in Heart Failure: Therapeutic Approach. J Am Coll Cardiol, 2018, 71 (7), 782-793.
- Lewis, G.D., Malhotra, R., Hernandez, A.F., McNulty, S.E., Smith, A., Michael Felker, G. et al. Effect of oral iron repletion on exercise capacity in patients with heart failure with reduced ejection fraction and iron deficiency the IRONOUT HF randomized clinical trial. JAMA, 2017, 317 (19), 1958-1966.
- Anker, S.D., Comin Colet, J., Filippatos, G., Willenheimer, R., Dickstein, K., Drexler, H. et al. Ferric Carboxymaltose in Patients with Heart Failure and Iron Deficiency. N Engl J Med, 2009, 361 (25), 2436-2448.
- Ponikowski, P., Van Veldhuisen, D.J., Comin-Colet, J., Ertl, G., Komajda, M., Mareev, V. et al. Beneficial effects of long-term intravenous iron therapy with ferric carboxymaltose in patients with symptomatic heart failure and iron deficiency. Eur Heart J, 2015, 36 (11), 657- 668.
- Ponikowski, P., Voors, A.A., Anker, S.D., Bueno, H., Cleland, J.G.F., Coats, A.J.S. et al. 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J, 2016, 37 (27), 2129-2200.
- Ponikowski, P., Kirwan, B.A., Anker, S.D., McDonagh, T., Dorobantu, M., Drozdz, J. et al. Ferric carboxymaltose for iron deficiency at discharge after acute heart failure: a multicentre, double-blind, randomised, controlled trial. The Lancet, 2020, 396 (10266), 1895-1904.
- Pitt, B., Zannad, F., Remme, W.J., Cody, R., Castaigne, A., Perez, A. et al. The Effect of Spironolactone on Morbidity and Mortality in Patients with Severe Heart Failure. N Engl J Med, 1999, 341 (10), 709-717.
- Pitt, B., Remme, W., Zannad, F., Neaton, J., Martinez, F., Roniker, B. et al. Eplerenone, a Selective Aldosterone Blocker, in Patients with Left Ventricular Dysfunction after Myocardial Infarction. N Engl J Med, 2003, 348 (14), 1309-1321.
- Zannad, F., McMurray, J.J.V., Krum, H., van Veldhuisen, D.J., Swedberg, K., Shi, H. et al. Eplerenone in Patients with Systolic Heart Failure and Mild Symptoms. N Engl J Med, 2011, 364 (1), 11-21.
- Tromp, J., Van Der Meer, P. Hyperkalaemia: Aetiology, epidemiology, and clinical significance. Eur Hear J Suppl, 2019, 21, A6-11.
- Martens, P., Kooij, J., Maessen, L., Dauw, J., Dupont, M., Mullens, W. The importance of developing hyperkalaemia in heart failure during long-term follow-up. Acta Cardiol [Internet], 2020, 1-9. Available from: https:// doi.org/10.1080/00015385.2020.1748346
- Vardeny, O., Claggett, B., Anand, I., Rossignol, P., Desai, A.S., Zannad, F. et al. Incidence, predictors, and outcomes related to hypo- and hyperkalemia in patients with severe heart failure treated with a mineralocorticoid receptor antagonist. Circ Heart Fail. 2014, 7 (4), 573-579.
- Beusekamp, J.C., Tromp, J., van der Wal, H.H., Anker, S.D., Cleland, J.G., Dickstein, K. et al. Potassium and the use of renin- angiotensin-aldosterone system inhibitors in heart failure with reduced ejection fraction: data from BIOSTAT-CHF. Eur J Heart Fail, 2018, 20 (5), 923-930.
- Pitt, B., Anker, S.D., Bushinsky, D.A., Kitzman, D.W., Zannad, F., Huang, I.Z. Evaluation of the efficacy and safety of RLY5016, a polymeric potassium binder, in a double-blind, placebocontrolled study in patients with chronic heart failure (the PEARL-HF) trial. Eur Heart J, 2011, 32 (7), 820-828.
Aucun élément du site web ne peut être reproduit, modifié, diffusé, vendu, publié ou utilisé à des fins commerciales sans autorisation écrite préalable de l’éditeur. Il est également interdit de sauvegarder cette information par voie électronique ou de l’utiliser à des fins illégales.