Compte rendu du congrès de la BSC - S2
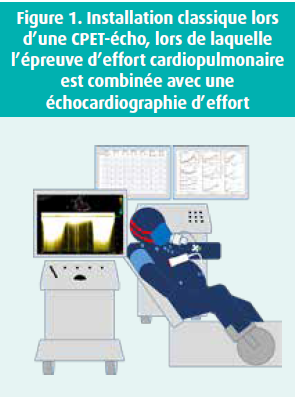
Le jeudi matin, le symposium sur la CPET-écho (cardiopulmonary exercise testing ou ergospirométrie combinée avec l'échocardiographie d'effort, figure 1) organisé par le BWGNICI (Belgian Working Group on Non-Invasive Cardiac Imaging) s'est tenu dans la salle 2 de Brussels Expo. Des sujets d'actualité tels que l'utilisation de la CPET-écho chez les athlètes et les patients souffrant de valvulopathies ou de dyspnée inexpliquée ont été abordés. La session s'est clôturée par la présentation du meilleur résumé de 2022 dans le domaine de l'imagerie cardiaque.
La CPET-écho en cas de valvulopathies avec des symptômes discordants
Jan Verweft - Jessa Ziekenhuis
Jan Verwerft a expliqué le rôle de la CPET-écho chez les patients présentant une discordance entre leurs symptômes et la sévérité de leur valvulopathie. L'écho d'effort est utile pour évaluer la sévérité de la valvulopathie (débit cardiaque, gradients et Doppler couleur), la réserve fonctionnelle du coeur et la charge hémodynamique ou les pressions artérielles pulmonaires (PAP).1, 2
Les recommandations de 2021 sur les valves préconisent toujours un remplacement de la valve aortique lorsque des patients qui se considèrent comme asymptomatiques développent malgré tout des symptômes lors d'une épreuve d'effort, lorsqu'il est clair que les symptômes sont dus à la sténose valvulaire aortique.3 Ce dernier point reflète dès lors la valeur ajoutée d'une ergospirométrie concomitante : parallèlement aux symptômes, il est également possible d'objectiver une diminution de la capacité à l'effort (absorption d'oxygène ou VO2 max) et d'exclure une cause non cardiaque comme une limitation pulmonaire, un déconditionnement (diminution de l'extraction d'oxygène) ou une épreuve sous-maximale.4
À l'aide d'un cas clinique, Jan Verwerft a illustré comment une CPET-écho a révélé une diminution de la capacité à l'effort et une hypertension pulmonaire à l'effort, sans augmentation du gradient valvulaire aortique chez un patient présentant une sténose valvulaire aortique modérée symptomatique.5 L'ergospirométrie a suggéré un important facteur précapillaire (désaturation à l'effort et ventilation très inefficace [pente VE/ VCO2 > 36 ou augmentation anormale de la ventilation par litre de CO2 produit]). Les symptômes n'étaient donc pas dus à la sténose valvulaire aortique, et il n'y a donc pas d'indication de chirurgie valvulaire. Un deuxième cas concernait un patient asymptomatique présentant une régurgitation mitrale sévère (prolapsus) et une légère dilatation du ventricule gauche (VG). La CPET-écho a montré une réserve cardiaque normale, avec une PAP proportionnelle au débit cardiaque maximal normal-haut et à l'absorption d'oxygène. La sévérité de la fuite valvulaire n'a pas augmenté durant l'effort. Un VO2 max normal combiné avec une déformation systolique élevée du VG (strain) au repos est associé à un excellent pronostic si ces patients sont suivis attentivement.6 Néanmoins, il reste important de compiler des données prospectives dans ce domaine passionnant.
La CPET-écho dans le bilan des athlètes
Guido Claessen - UZ Leuven
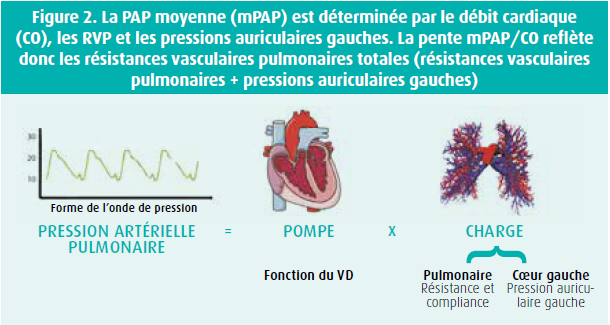
Guido Claessen a clairement indiqué que le coeur de l'athlète est par excellence une machine qui doit être testée lorsqu'elle fait ce pour quoi elle est faite et entraînée : fournir un effort. Il a illustré ceci à l'aide du cas d'un cycliste de haut niveau présentant des douleurs thoraciques atypiques, qui avait une fraction d'éjection (FEVG) de 46 %, ce qui n'est pas rare dans la cohorte Pro@Heart (6 % des cyclistes de haut niveau). Étant donné que le père de cet athlète souffrait d'une cardiomyopathie, on a néanmoins pratiqué des examens complémentaires. Le Holter ecg était normal et le bilan génétique était en cours. Dans ce contexte, une CPET-écho se révèle particulièrement utile. En effet, comme on peut s'y attendre chez des athlètes en bonne santé, cet athlète avait une FEVG à l'effort > 63 % et une augmentation absolue de la FEVG > 11 %.7 Guido Claessen a ensuite expliqué que les résistances vasculaires pulmonaires, les pressions auriculaires gauches et le débit cardiaque déterminent la pression artérielle pulmonaire (PAP) lors d'un effort (figure 2).8 Il a évoqué le cas d'un patient souffrant de dyspnée à l'effort, qui est resté symptomatique après une embolie pulmonaire, alors qu'il ne présentait pas d'hypertension pulmonaire au repos. La CPET-écho a montré que les symptômes étaient dus à des séquelles de l'embolie pulmonaire, car la PAP augmentait de façon disproportionnée par rapport au débit cardiaque (pente PAP moyenne/ CO de 2,3 mmHg/l/min, normale < 2 mmHg/l/min dans une population jeune), avec une désaturation importante et une pente VE/VCO2 remarquablement élevée, témoignant d'un déséquilibre ventilation/perfusion.9 Après une endartériectomie pulmonaire, ces anomalies ont disparu. Dans ce cas également, l'évaluation échocardiographique à l'effort a apporté une importante plus-value.
Dyspnée inexpliquée : CPET-écho versus cathétérisme ?
Frederik Verbrugge - UZ Brussel
Frederik Verbrugge a ensuite expliqué comment la CPET-écho et l'ergospirométrie avec mesure invasive de la pression (iCPET) sont complémentaires dans l'évaluation de la dyspnée inexpliquée et le diagnostic de l'insuffisance cardiaque avec FE > 50 % (HFpEF). Il a proposé une approche par étapes, impliquant tout d'abord une échocardiographie détaillée et un test de fonction pulmonaire, suivies d'une CPET-écho et d'une iCPET en dernier recours. Alors que des taux bas de peptides natriurétiques (NT-proBNP) n'excluent pas une HFpEF cliniquement pertinente, une pression capillaire pulmonaire normale lors d'un effort l'exclut.10 Une pression capillaire pulmonaire > 25 mmHg est la référence pour le diagnostic de l'HFpEF. La CPET-écho s'avère souvent suffisante en cas de risque intermédiaire d'HFpEF selon le score H2FPEF (1-5 points sur la base de critères cliniques et échocardiographiques simples), en combinaison avec un rapport E/e' élevé (rapport entre la vitesse du flux sanguin à travers la valve mitrale et la vitesse diastolique précoce à travers l'anneau valvulaire mitral) et avec une hypertension pulmonaire à l'effort (figure 3).11, 12 Frederik Verbrugge a toutefois signalé que la CPET-écho présente des limites: le débit cardiaque à l'effort est systématiquement sous-estimé et, si les pressions auriculaires droites augmentent fortement, les pressions pulmonaires risquent également d'être sous-estimées, de sorte que le rapport des deux - la pente mPAP/ CO - reste précis.13De ce fait, lorsqu'un phénotypage détaillé est nécessaire pour prendre des décisions thérapeutiques, l'iCPET apporte une valeur ajoutée par rapport à la CPET-écho. En effet, des interventions pour l'HFpEF sont en vue, comme les dispositifs de shunt pour l'HFpEF avec des résistances vasculaires pulmonaires basses à l'effort, et la péricardiotomie percutanée pour l'HFpEF avec une égalisation des pressions de remplissage droites et gauches en raison d'une augmentation de la pression péricardique avec des dépôts graisseux épicardiques.

Best Abstract: Outcome penalty of guidelines surgical triggers in severe aortic regurgitation
Vincent Hanet - UCLouvain
Enfin, Vincent Hanet, qui a remporté le prix du meilleur résumé en imagerie cardiaque, a pu présenter ses travaux sous la forme d'un résumé oral. Pour l'insuffisance aortique (IA) asymptomatique sévère, les dernières recommandations internationales sur les valves enseignent qu'il y a des indications strictes (classe I) de remplacement de la valve aortique (FE ≤ 50 % et diamètre du VG > 55 mm ou 25 mm/m²) et de nouvelles indications de moindre classe (IIa) (FE ≤ 55 % et diamètre du VG 20 mm/m²). Vincent Hanet a présenté la survie à 10 ans d'une cohorte mondiale (AVIATOR) de 1 899 patients opérés suite à une IA sévère. Des études précédentes avaient déjà montré que la chirurgie valvulaire aortique à partir de l'indication conservatrice (classe I) est associée à une moins bonne survie qu'une intervention plus précoce.14 Le tout est de savoir si les patients n'en font pas les frais, si l'intervention est effectuée sur la base des indications moins conservatrices (classe IIa). Les résultats de l'étude de Vincent Hanet confirment que les symptômes préopératoires, une FE < 50 % et un diamètre > 50 mm et 25 mm/m², prédisent une moins bonne survie. Chez les patients ayant subi une chirurgie valvulaire aortique sur la base d'un diamètre préopératoire > 20 mm/m² et d'une FE < 55 %, on ne notait pas de diminution de la survie postopératoire. Une étude randomisée devrait donner une réponse définitive à ce sujet. Les modérateurs ont toutefois signalé que la cohorte étudiée était constituée d'une population très sélectionnée issue de centres d'expertise, ce qui témoigne d'un taux très élevé de réparation valvulaire dans cette cohorte.
Références
- Lancellotti, P., Pellikka, P.A., Budts, W., Chaudhry, F.A., Donal, E., Dulgheru, R. et al. The clinical use of stress echocardiography in non-ischaemic heart disease: recommendations from the European Association of Cardiovascular Imaging and the American Society of Echocardiography. Eur Heart J Cardiovasc Imaging, 2016, 17 (11), 1191-229.
- Vahanian, A., Beyersdorf, F., Praz, F., Milojevic, M., Baldus, S., Bauersachs, J. et al. 2021 ESC/ EACTS Guidelines for the management of valvular heart disease. Eur Heart J, 2021.
- Martens, P., Herbots, L., Timmermans, P., Verbrugge, F.H., Dendale, P., Borlaug, B.A. et al. Cardiopulmonary Exercise Testing with Echocardiography to Identify Mechanisms of Unexplained Dyspnea. J Cardiovasc Transl Res, 2022, 15 (1), 116-130.
- Stassen, J., Ewe, S.H., Butcher, S.C., Amanullah, M.R., Hirasawa, K., Singh, G.K. et al. Moderate aortic stenosis: importance of symptoms and left ventricular ejection fraction. Eur Heart J Cardiovasc Imaging, 2021, 23 (6), 790-799.
- Mentias, A., Naji, P., Gillinov, A.M., Rodriguez, L.L., Reed, G., Mihaljevic, T. et al. Strain Echocardiography and Functional Capacity in Asymptomatic Primary Mitral Regurgitation With Preserved Ejection Fraction. J Am Coll Cardiol, 2016, 68 (18), 1974-1986.
- Claessen, G., Schnell, F., Bogaert, J., Claeys, M., Pattyn, N., De Buck, F. et al. Exercise cardiac magnetic resonance to differentiate athlete's heart from structural heart disease. Eur Heart J Cardiovasc Imaging, 2018, 19 (9), 1062-1070.
- La Gerche, A., MacIsaac, A.I., Burns, A.T., Mooney, D.J., Inder, W.J., Voigt, J.U. et al. Pulmonary transit of agitated contrast is associated with enhanced pulmonary vascular reserve and right ventricular function during exercise. J Appl Physiol, 1985, 2010, 109 (5), 1307-1317.
- Lewis, G.D., Bossone, E., Naeije, R., Grünig, E., Saggar, R., Lancellotti, P. et al. Pulmonary vascular hemodynamic response to exercise in cardiopulmonary diseases. Circulation, 2013, 128 (13), 1470-1479.
- Verbrugge, F.H., Omote, K., Reddy, Y.N.V., Sorimachi, H., Obokata, M., Borlaug, B.A. Heart failure with preserved ejection fraction in patients with normal natriuretic peptide levels is associated with increased morbidity and mortality. Eur Heart J, 2022, 43 (20), 1941-1951.
- Reddy, Y.N.V., Carter, R.E., Obokata, M., Redfield, M.M., Borlaug, B.A. A Simple, Evidence-Based Approach to Help Guide Diagnosis of Heart Failure With Preserved Ejection Fraction. Circulation, 2018, 138 (9), 861-870.
- Pieske, B., Tschope, C., de Boer, R.A., Fraser, A.G., Anker, S.D., Donal, E. et al. How to diagnose heart failure with preserved ejection fraction: the HFA-PEFF diagnostic algorithm: a consensus recommendation from the Heart Failure Association (HFA) of the European Society of Cardiology (ESC). Eur Heart J, 2019, 40 (40), 3297-3317.
- Claessen, G., La Gerche, A., Voigt, J.U., Dymarkowski, S., Schnell, F., Petit, T. et al. Accuracy of Echocardiography to Evaluate Pulmonary Vascular and RV Function During Exercise. JACC Cardiovasc Imaging, 2016, 9 (5), 532-543.
- de Meester, C., Gerber, B.L., Vancraeynest, D., Pouleur, A-C., Noirhomme, P., Pasquet, A. et al. Do Guideline-Based Indications Result in an Outcome Penalty for Patients With Severe Aortic Regurgitation? JACC Cardiovasc Imaging, 2019, 12 (11), 2126-2138.
Aucun élément du site web ne peut être reproduit, modifié, diffusé, vendu, publié ou utilisé à des fins commerciales sans autorisation écrite préalable de l’éditeur. Il est également interdit de sauvegarder cette information par voie électronique ou de l’utiliser à des fins illégales.