Compte rendu du congrès de l'ESC
Cette session, présidée par Iacopo Olivotto (Florence, Italie) et Michelle Michels (Rotterdam, Pays-Bas) a été consacrée au mavacamten, un nouveau traitement médicamenteux désormais disponible pour les patients souffrant d'une cardiomyopathie hypertrophique obstructive (CMPHO) symptomatique. Au cours de cette session, on a discuté des principales données scientifiques, qui ont également été incluses dans les toutes récentes recommandations de l'ESC pour le diagnostic et le traitement des patients souffrant de cardiomyopathies.1
La cardiomyopathie hypertrophique est une des maladies génétiques du coeur les plus fréquentes. Elle se caractérise par un épaississement inapproprié du muscle cardiaque, qui peut s'accentuer tout au long de la vie. La cause physiopathologique exacte de cet épaississement n'est pas tout à fait claire, mais elle n'est pas due à des facteurs externes comme l'hypertension ou une augmentation de la postcharge, comme en cas de sténose aortique. Il est également important de mentionner qu'il s'agit d'une affection qui se limite au coeur et qu'elle ne s'inscrit pas dans le cadre d'une affection secondaire systémique telle que les maladies de surcharge (p. ex. l'amylose ou la maladie de Fabry) ou les affections mitochondriales ou neuromusculaires. On pense que la prévalence varie entre 1 patient sur 200 et 1 sur 500 (20 millions de patients dans le monde et un peu moins de 20 000 en Belgique), une grande partie des cas étant sous-diagnostiquée, étant donné le caractère aspecifique a- ou paucisymptomatique de l'affection. Les symptômes possibles sont une dyspnée (surtout à l'effort ou postprandiale), des douleurs thoraciques, des palpitations, une syncope et parfois une mort subite. Ces symptômes surviennent principalement lorsque l'hypertrophie du muscle cardiaque se produit au niveau du septum et provoque une obstruction de la chambre de chasse (CMPHO), ce qui est le cas chez environ deux tiers des patients. Jusqu'à présent, les patients symptomatiques ne peuvent être traités que par bêtabloquants, antagonistes calciques et parfois disopyramide. à ce sujet, on ne dispose que de données très limitées. Les patients réfractaires au traitement, présentant une CMPHO marquée peuvent également entrer en ligne de compte pour un traitement de réduction septale (TRS), en l'occurrence une myomectomie chirurgicale ou une alcoolisation du septum. Ces deux types de TRS réduisent les symptômes mais sont invasifs et l'efficacité et la sécurité sont clairement meilleurs dans les centres ayant une grande expérience.
La mutation génétique la plus fréquente se situe au niveau des protéines du sarcomère, ce qui entraîne une formation excessive de ponts croisés entre les filaments de myosine cardiaque et d'actine, de sorte que le myocarde devient hypercontractile. Le mavacamten est un inhibiteur de la myosine, le premier de sa catégorie, qui réduit ces ponts croisés et normalise la contractilité. C'est également le seul traitement qui agit sur la physiopathologie sous-jacente.
L'efficacité de mavacamten a été évaluée dans le cadre de l'étude clinique de phase III (EXPLORER-HCM) dans laquelle le mavacamten a été étudié pendant 30 semaines en double aveugle versus un placebo chez 251 patients présentant une CMPHO symptomatique.2 Dans ce contexte, l'épaisseur maximale de la paroi du ventricule gauche devait atteindre au moins 15 mm (ou 13 mm en cas d'antécédents familiaux), le gradient au niveau de la chambre de chasse (LVOT) devait être supérieur à 50 mmHg au repos ou après un test de provocation comme, par exemple, la manoeuvre de Valsalva, ou après un effort. La fraction d'éjection ventriculaire gauche (FEVG) devait être supérieure à 55 %, et ceci a également fait l'objet d'une évaluation échocardiographique centrale. Ces patients ne pouvaient prendre que des bêtabloquants ou des antagonistes calciques (pas d'association), ils ne devaient pas être fortement symptomatiques (e. a. classe NYHA IV, troubles du rythme ventriculaire actifs, syncope récente ou FA persistante) et ils ne devaient pas être programmés pour un TRS.
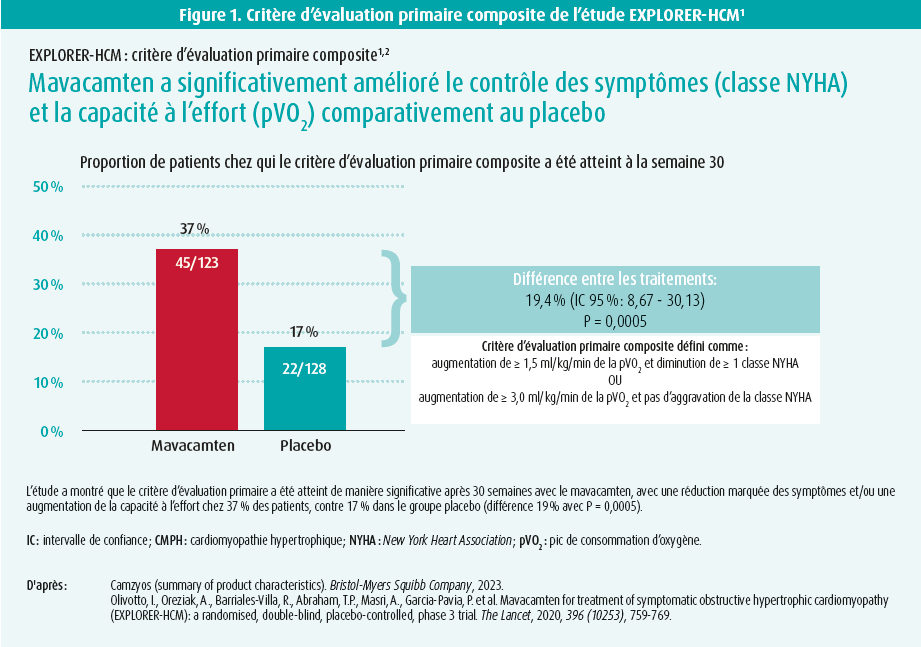
Le critère d'évaluation primaire consistait en une augmentation d'au moins 1,5 ml/ kg/min du pic de VO2max (ergospirométrie) et une amélioration d'au moins un grade de la classe NYHA ou une augmentation d'au moins 3 ml/kg/min du pic de VO2 sans aggravation de la classe NYHA. D'autres critères d'évaluation secondaire étaient le gradient LVOT après l'effort, la modification de la VO2max, la classe NYHA, le score KCCQ-23 et les scores HCSMSQ-SOB. Ces derniers sont des scores rapportés par les patients (PROM) qui évaluent l'impact de l'affection sur le fonctionnement quotidien du patient.
L'âge moyen des patients était de 59 ans, 72 % d'entre eux étaient en classe NYHA II ou moins et environ 75 % prenaient des bêtabloquants et un peu moins de 20 % des antagonistes calciques. L'étude a montré que le critère d'évaluation primaire a été atteint de manière significative après 30 semaines avec le mavacamten, avec une réduction marquée des symptômes et/ou une augmentation de la capacité à l'effort chez 37 % des patients, contre 17 % dans le groupe placebo (différence 19 % avec P = 0,0005) (figure 1). Ceci s'est également reflété par une réduction moyenne de 47 mmHg du gradient LVOT après l'effort dans le groupe mavacamten, contre 10 mmHg dans le groupe placebo (P < 0,0001). Le pic de VO2max, la classe NYHA et les scores PROM ont également évolué favorablement grâce au mavacamten. Le traitement par mavacamten était également bien toléré et son profil de sécurité est comparable à celui du placebo. La fraction d'éjection ventriculaire gauche est également restée quasi stable tout au long de l'étude. Quelques patients ont présenté une diminution transitoire de la FEVG, qui a disparu après réduction de la dose.
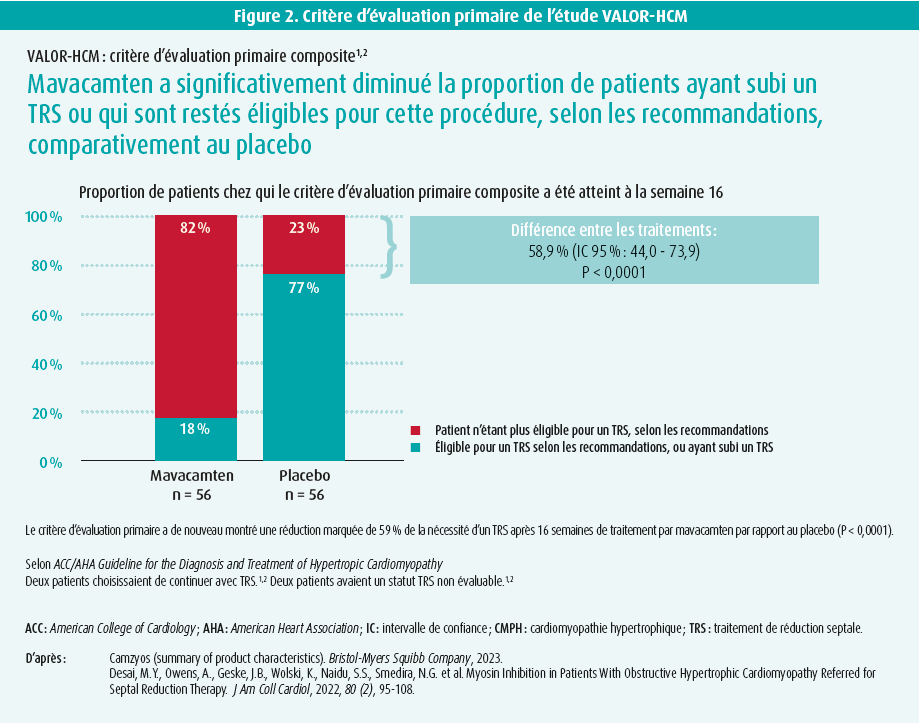
Dans une autre étude randomisée, en double aveugle, contrôlée par placebo, de phase III (VALOR-HCM), on a examiné si le mavacamten pouvait réduire la nécessité d'un TRS après 16 semaines chez 112 patients chez qui ce traitement était planifié.3 Ces patients étaient donc plus symptomatiques en raison d'une CMPHO et, outre les critères susmentionnés de l'étude EXPLORER-HCM, ils pouvaient également être en classe NYHA IV, prendre une combinaison de bêtabloquants, d'antagonistes calciques et de disopyramide (patients réfractaires au traitement médicamenteux) et avoir présenté une syncope récente. Le critère d'évaluation primaire était la nécessité persistante d'un TRS selon le patient ou selon les critères des recommandations (NYHA II avec [quasi] syncope liée à l'effort ou NYHA III-IV sous traitement médical maximal, ainsi qu'un gradient LVOT > 50 mmHg, provoqué ou non).
Ces patients étaient âgés de 59 ans en moyenne, et plus de 90 % d'entre eux étaient en classe NYHA III ou IV. Ici aussi, le critère d'évaluation primaire a montré une réduction nette de 59 % de la nécessité de recourir au TRS après 16 semaines de traitement par mavacamten comparativement au placebo (P < 0,0001) (figure 2). à nouveau, on a observé une réduction significative marquée du gradient LVOT après l'effort de 37 mmHg par rapport au placebo, avec une amélioration de la classe NYHA, du KCCQ-23, du NT-proBNP et de la troponine cardiaque I. Le profil de sécurité du mavacamten était comparable à celui du placebo.
Ces deux études ont donc montré un effet bénéfique du mavacamten sur le critère d'évaluation primaire et tous les critères d'évaluation secondaires chez les patients souffrant d'une CMPHO symptomatique. Le mavacamten a également diminué la nécessité de recourir au TRS chez les patients très symptomatiques.
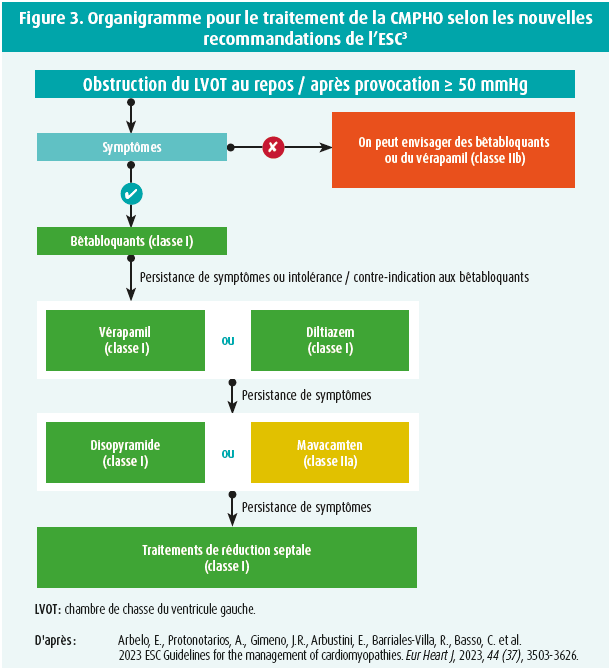
Les résultats de ces études ont également été inclus dans les nouvelles recommandations de l'ESC (figure 3), dans lesquelles le mavacamten a reçu une recommandation de classe IIa pour le traitement de la CMPHO symptomatique, si l'effet des bêtabloquants ou des antagonistes calciques est insuffisant. En Europe, le mavacamten est approuvé pour cette indication depuis avril 2023 et il sera bientôt disponible.
Enfin, durant cette session, on a abordé plus en détail l'utilisation pratique du mavacamten en termes de posologie et d'interactions médicamenteuses, telles qu'elles ont été utilisées dans les études de phase III. Le mavacamten est métabolisé par le cytochrome CYP2C19 et l'activité métabolique doit être déterminée au préalable (métaboliseur faible ou normal) à l'aide d'une analyse de sang. Chez les métaboliseurs normaux, on peut commencer à une dose de 5 mg un fois par jour. Initialement, la fraction d'éjection et le gradient LVOT doivent être évalués toutes les quatre semaines. La FEVG doit rester supérieure à 55 % et le gradient LVOT doit tomber en dessous de 30 mmHg après 12 semaines de traitement. Ce n'est qu'à ce moment-là qu'on peut commencer à titrer la dose, jusqu'à un maximum de 15 mg. Si le gradient tombe en dessous de 20 mmHg, la dose doit être diminuée de moitié et si la FEVG tombe < 50 %, le traitement doit être temporairement interrompu. Chez les métaboliseurs lents ou dont le statut est inconnu, il faut être plus prudent et débuter avec une dose de 2,5 mg. Il convient également de faire attention avec d'autres médicaments qui inhibent (fortement) le CYP2C19, comme le fluconazole.
Références
- Arbelo, E., Protonotarios, A., Gimeno, J.R., Arbustini, E., Barriales-Villa, R., Basso, C. et al. 2023 ESC Guidelines for the management of cardiomyopathies Developed by the task force on the management of cardiomyopathies of the European Society of Cardiology (ESC) (United Kingdom). Eur Heart J, 2023, 1-124.
- Olivotto, I., Oreziak, A., Barriales-Villa, R., Abraham, T.P., Masri, A., Garcia-Pavia, P. et al. Mavacamten for treatment of symptomatic obstructive hypertrophic cardiomyopathy (EXPLORER-HCM): a randomised, double-blind, placebocontrolled, phase 3 trial. The Lancet, 2020, 396 (10253), 759-769.
- Desai, M.Y., Owens, A., Geske, J.B., Wolski, K., Saberi, S., Wang, A. et al. Dose- Blinded Myosin Inhibition in Patients with Obstructive Hypertrophic Cardiomyopathy Referred for Septal Reduction Therapy: Outcomes Through 32 Weeks. Circulation, 2023, 147 (11), 850-863.
Aucun élément du site web ne peut être reproduit, modifié, diffusé, vendu, publié ou utilisé à des fins commerciales sans autorisation écrite préalable de l’éditeur. Il est également interdit de sauvegarder cette information par voie électronique ou de l’utiliser à des fins illégales.