ESC-congresverslag
Deze sessie was gewijd aan mavacamten, een nieuwe medicamenteuze therapie die ter beschikking is gekomen voor patiënten met symptomatische obstructieve hypertrofische cardiomyopathie (HOCMP). Deze sessie werd voorgezeten door Iacopo Olivotto (Firenze, Italië) en Michelle Michels (Rotterdam, Nederland). Tijdens deze sessie werden de voornaamste wetenschappelijke data gepresenteerd en bediscussieerd. Deze werden eveneens opgenomen in de net gepubliceerde ESC-richtlijnen voor de diagnose en behandeling van patiënten met cardiomyopathiën.1
Hypertrofische cardiomyopathie is een van de meest frequente genetische aandoeningen van het hart waarbij er een onaangepaste verdikking van de hartspier optreedt die kan toenemen gedurende het leven. De exacte pathofysiologische oorzaak van deze verdikking is niet helemaal duidelijk, maar is niet te wijten aan externe factoren zoals hypertensie of toename van de afterload zoals aortaklepstenose. Belangrijk is eveneens te melden dat het in dit verband ook gaat over een aandoening die beperkt is tot het hart en geen deel uitmaakt van een systemische secundaire aandoening zoals stapelingsziekten (bv. amyloïdose of de ziekte van Fabry) of bv. mitochondriale of neuromusculaire aandoeningen. De prevalentie bedraagt vermoedelijk tussen 1 op 200 en 1 op 500 (20 miljoen patiënten wereldwijd, een kleine 20 000 in België) waarvan een groot deel ondergediagnosticeerd is, gezien aspecifieke beperkte of afwezige symptomen. De symptomen die voorkomen zijn kortademigheid (vooral bij inspanning of na de maaltijd), pijn op de borst, hartkloppingen, syncope en soms plotse dood. Deze klachten treden vooral op wanneer de hypertrofie van de hartspier optreedt ter hoogte van het septum en uitstroombaanobstructie veroorzaakt (HOCMP), wat ongeveer in twee derde van de patiënten het geval is. Tot nu toe kunnen symptomatische patiënten enkel worden behandeld met bètablokkade, calciumantagonisten en soms ook disopyramide. Hiervoor is er slechts zeer beperkte evidentie. Therapierefractaire patiënten met een duidelijke HOCMP kunnen ook in aanmerking komen voor septale reductietherapie (SRT), hetzij chirurgische myomectomie of alcoholseptale ablatie. Beide SRT's verminderen de klachten maar zijn agressief en de doeltreffendheid en veiligheid is duidelijk beter in centra met veel ervaring.
De meest voorkomende genetische mutatie is ter hoogte van de sarcomeereiwitten, wat leidt tot excessieve actieve en crossbridge vorming tussen de myosine en actine-filamenten waardoor het myocard in een hyperactieve contractiele status komt. Mavacamten is een eersteklas cardiale myosine-inhibitor, wat deze crossbridges vermindert en de contractiliteit terug normaliseert. Het is eveneens de enige behandeling die op de onderliggende pathofysiologie werkt.
De werking van mavacamten werd onderzocht in de klinische fase III-studie (EXPLORER-HCM) waarbij mavacamten werd bestudeerd gedurende 30 weken op een placebo, dubbelblind gecontroleerde manier in 251 patiënten met symptomatische HOCMP.2 Hierbij moest de linkerventriculaire maximale wanddikte minstens 15 mm dik zijn (of 13 mm in geval van familiale voorgeschiedenis), de gradiënt over de uitstroombaan (LVOT) meer dan 50 mmHg bedragen in rust, of na een provocatietest zoals bijvoorbeeld bij het valsalvamanoeuvre of na inspanning. De linkerventrikelejectiefractie (LVEF) moest meer dan 55 % bedragen en dat werd eveneens geverifieerd via een echocardiografie core labo. Deze patiënten mochten enkel bètablokkers of calciumblokkers nemen (geen combinatie) en niet zwaar symptomatisch zijn (onder andere NYHA klasse-IV, actieve ventriculaire ritmestoornissen, recente syncope of persisterende VKF) en niet gepland voor een SRT.
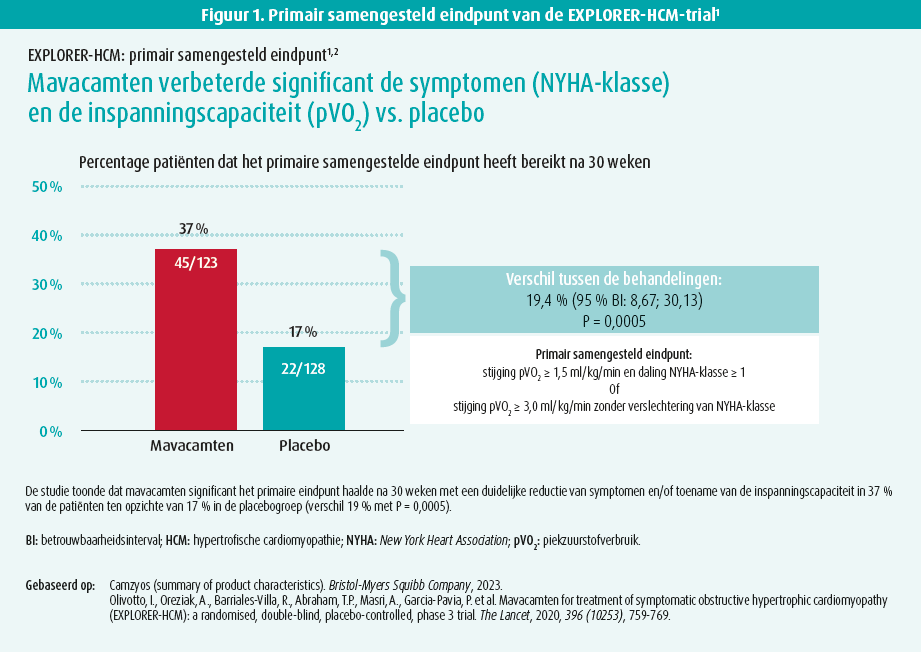
Het primaire eindpunt bestond uit een toename van minstens 1,5 ml/kg/min van piek VO2max (ergospirometrie) en een verbetering van minstens één NYHA-klasse ofwel een toename van minstens 3 ml/kg/min van piek VO2 zonder verergering van de NYHA-klasse. Andere secundaire eindpunten waren post-inspanning LVOT-gradiënt, verandering in piek VO2, NYHA-klasse, KCCQ-23-score en HCSMSQSOB-scores. Die laatste zijn patiëntgerapporteerde scores (PROM's) die de weerslag van de aandoening op het dagelijkse functioneren van de patiënt evalueren.
De gemiddelde leeftijd was 59 jaar, waarvan 72 % van de patiënten onder NYHA-klasse II valt en ongeveer 75 % bètablokkade en een kleine 20 % calciumantagonisten nam. De studie toonde dat mavacamten significant het primaire eindpunt haalde na 30 weken met een duidelijke reductie van symptomen en/ of toename van de inspanningscapaciteit in 37 % van de patiënten ten opzichte van 17 % in de placebogroep (verschil 19 % met P = 0,0005) (figuur 1). Dit weerspiegelde zich eveneens in een gemiddelde 47 mmHg post-inspanning LVOT-gradiëntreductie in de mavacamten-groep ten opzichte van 10 mmHg in de placebogroep (P < 0,0001). De piek VO2max, NYHA-klasse, en PROM-scores evolueerde eveneens gunstig ten voordele van mavacamten. De behandeling met mavacamten werd eveneens goed verdragen met een veiligheidsprofiel in vergelijking met placebo. De LVEF bleef eveneens quasi-stabiel gedurende de studie. Enkele patiënten toonden een tijdelijke daling die recupereerde na dosisreductie.
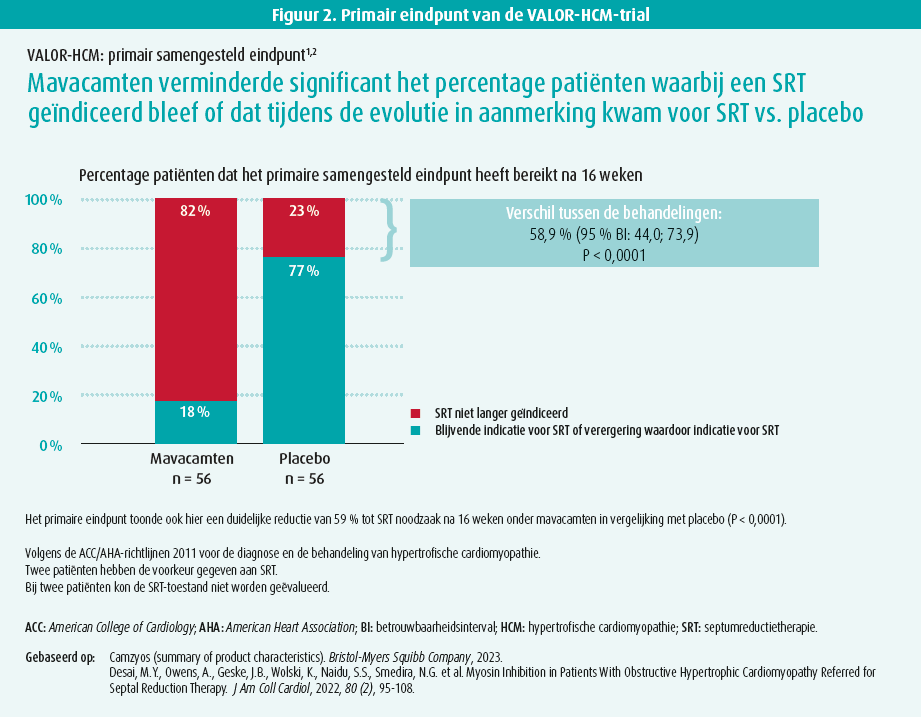
In een andere fase III, gerandomiseerde, dubbelblinde, placebogecontroleerde studie (VALOR-HCM) werd onderzocht of mavacamten de nood tot SRT kon verminderen na 16 weken bij 112 patiënten die hiervoor gepland waren.3 Dat waren dus patiënten die meer symptomatisch waren door een HOCMP, en naast de voorheen genoemde criteria van de EXPLORER-HCM, ook in NYHA-klasse IV mochten zijn, een combinatie van bètablokkade, calciumantagonisten en disopyramide mochten nemen (medicatierefractair) en ook recente syncope konden hebben doorgemaakt. Het primaire eindpunt bestond uit de nog aanwezige noodzaak tot SRT volgens de patiënt of volgens de richtlijnencriteria (NYHA II met inspanningsgebonden [bijna] syncope of NYHA III-IV onder maximale medische therapie, én een LVOT-gradiënt van > 50 mmHg, al dan niet geprovoceerd).
Deze patiënten waren gemiddeld 59 jaar oud, meer dan 90 % in NYHA III of IV. Het primaire eindpunt toonde ook hier een duidelijke reductie van 59 % tot SRT-noodzaak na 16 weken onder mavacamten in vergelijking met placebo (P < 0,0001) (figuur 2). Ook hier was er een uitgesproken significante reductie van de post-inspanning LVOT-gradiënt van 37 mmHg in vergelijking met placebo, met een verbetering van de NYHA-klasse, KCCQ-23 en eveneens NT-proBNP en cardiaal tropinine I. Het veiligheidsprofiel van mavacamten was ook hier vergelijkbaar met placebo.
Beide trials toonden dus een gunstig effect van mavacamten op de primaire en al de secundaire eindpunten bij patienten met een symptomische HOCMP. Het verminderde eveneens de noodzaak tot SRT bij de heel symptomatische patienten.
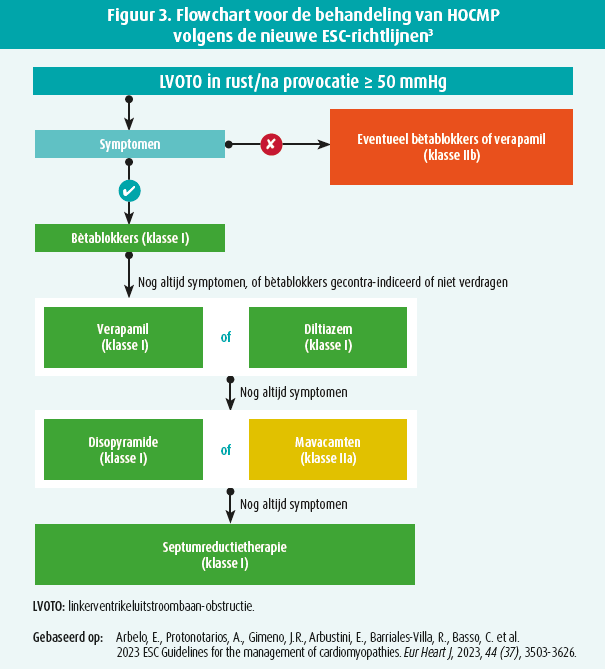
De bevindingen van deze trials zijn eveneens opgenomen in de nieuwe ESC-richtlijnen (figuur 3) waarbij mavacamten een klasse IIa-aanbeveling heeft gekregen voor de behandeling van symptomatische HOCMP als er onvoldoende effect met bètablokkade of calciumantagonisten bekomen wordt. In Europa is mavacamten goedgekeurd voor deze indicatie sedert april dit jaar en zal het weldra ook beschikbaar zijn.
Tot slot werd er tijdens de sessie verder ingegaan op het praktische gebruik van mavacamten in verband met dosering en interactie zoals die ook in de fase III-studies hebben plaatsgevonden. Mavacamten wordt gemetaboliseerd door het cytochroom CYPC219 en de metabole activiteit moet op voorhand worden bepaald (poor versus normal metaboliser) via een bloedanalyse. Bij normale metaboliseerders kan worden gestart aan 5 mg eenmaal daags. Initieel moet vierwekelijks de ejectiefractie en de LVOT-gradiënt worden beoordeeld. De LVEF moet boven de 55 % blijven en de LVOT-gradiënt moet onder de 30 mmHg komen na 12 weken behandeling. Er kan dan pas verder worden opgetitreerd, tot maximaal 15 mg. Als de gradiënt onder de 20 mmHg zakt, moet de dosis worden gehalveerd en als de LVEF < 50 % komt, moet de behandeling tijdelijk worden onderbroken. Bij trage metaboliseerders of van onbekende status moet voorzichtiger aan 2,5 mg worden gestart. Er moet eveneens worden opgelet met andere medicatie die het CYPC219 (sterk) inhiberen, zoals bv. fluconazole.
Referenties
- Arbelo, E., Protonotarios, A., Gimeno, J.R., Arbustini, E., Barriales-Villa, R., Basso, C. et al. 2023 ESC Guidelines for the management of cardiomyopathies Developed by the task force on the management of cardiomyopathies of the European Society of Cardiology (ESC) (United Kingdom). Eur Heart J, 2023, 1-124.
- Olivotto, I., Oreziak, A., Barriales-Villa, R., Abraham, T.P., Masri, A., Garcia-Pavia, P. et al. Mavacamten for treatment of symptomatic obstructive hypertrophic cardiomyopathy (EXPLORER-HCM): a randomised, double-blind, placebocontrolled, phase 3 trial. The Lancet, 2020, 396 (10253), 759-769.
- Desai, M.Y., Owens, A., Geske, J.B., Wolski, K., Saberi, S., Wang, A. et al. Dose- Blinded Myosin Inhibition in Patients with Obstructive Hypertrophic Cardiomyopathy Referred for Septal Reduction Therapy: Outcomes Through 32 Weeks. Circulation, 2023, 147 (11), 850-863.
Niets van de website mag gebruikt worden voor reproductie, aanpassing, verspreiding, verkoop, publicatie of commerciële doeleinden zonder voorafgaande schriftelijke toestemming van de uitgever. Het is ook verboden om deze informatie elektronisch op te slaan of te gebruiken voor onwettige doeleinden.