Cardiovasculaire ziekte blijft tot op vandaag een belangrijke oorzaak van morbiditeit en mortaliteit in de westerse samenleving ondanks preventieve behandeling.1 Hypercholesterolemie is een van de belangrijkste risicofactoren. 2-3 De gebruikelijke cholesterolverlagende therapie bestaat uit statines en/of ezetimibe. Het verlagen van LDL-cholesterol met 40 mg/dL gedurende 5 jaar gaat gepaard met een 22% verminderd risico op majeure cardiovasculaire events, ongeacht statinetherapie of niet en ongeacht de baseline LDL-cholesterolwaarde.2 Sommige patiëntengroepen bereiken de LDL-streefwaarde niet, zoals patiënten in secundaire preventie, patiënten met familiale hypercholesterolemie, patiënten met statine-intolerantie en tot slot diabetici. Diabetici ondervinden dezelfde relatieve risicoreductie als niet-diabetici onder behandeling met statines, maar ze hebben een hoger baseline cardiovasculair risico.4 Daarom kan het aangewezen zijn om een verdere reductie van LDL-cholesterol na te streven en is een combinatie van cholesterolverlagende middelen soms noodzakelijk.3
Door het toevoegen van ezetimibe aan de behandeling met een statine wordt een bijkomende LDL-cholesteroldaling van 20-25 % bereikt en het is aangetoond dat hierdoor het cardiovasculair risico verder daalt.5 Vandaar wordt momenteel aanbevolen om ezetimibe aan de behandeling toe te voegen wanneer de LDL-cholesterolstreefwaarde niet wordt bereikt ondanks behandeling met de maximaal tolereerbare dosis statine.6 Nadien zijn de PCSK9-inhibitoren (proprotein convertase subtilisin/kexin type 9) op de markt gekomen, de monoclonale antilichamen alirocumab (Praluent®, Sanofi) en evolocumab (Repatha®, Amgen). Met beide producten is een bijkomende daling van LDL-cholesterol van 50-60 % mogelijk.7, 8 Met de FOURIER-studie werd aangetoond dat het toevoegen van een PCSK9-inhibitor (evolocumab 140 mg om de 2 weken of 420 mg om de maand) aan een statine een verdere en significante reductie van het risico op cardiovasculaire events veroorzaakt en dit is in lijn met het voorspelde benefit uit metaregressieanalyse. 9
Ondertussen is er bijkomend onderzoek gebeurd naar de effecten en veiligheid van behandeling met PCSK9-inhibitoren bij patiënten met diabetes. In dit overzicht wordt ingegaan op resultaten van de subanalyse van de FOURIER-studie bij diabetespatiënten,10 de ODYSSEY DM-INSULIN-studie en de ODYSSEY DM-DYSLIPIDEMIA-studie.11, 12
FOURIER in Diabetes
In FOURIER hadden 11 031 (of 40 %) van de 27 564 deelnemers diabetes (97 % type 2 diabetes, 3 % type 1 diabetes).10 Diabetici waren frequenter vrouwen, ze hadden een ietwat hogere BMI en hogere triglyceriden, en hadden vaker hypertensie, een lagere eGFR, en een voorgeschiedenis van beroerte en perifeer vaatlijden. Een eerste opvallende bevinding was dat patiënten met diabetes (maar niet prediabetes) en een cardiovasculaire voorgeschiedenis een substantieel hoger risico hadden op cardiovasculaire morbiditeit en mortaliteit. Ten tweede, de behandeling met evolocumab leidde tot een significante daling van het LDL-cholesterol, zowel in de diabetessubgroep (-57 %) als in de niet-diabetessubgroep (-60 %) met bereiken van een LDL-cholesterol van 32 mg/dL in beide subgroepen. Het primair eindpunt - een samenstelling van cardiovasculaire dood, myocardinfarct, beroerte, hospitalisatie voor onstabiele angor of coronaire revascularisatie - was gedaald in beide groepen na een mediane follow-up van 2,2 jaar: de hazard ratio was 0,83 (95 % CI 0,75-0,93; p = 0,0008) voor patiënten met diabetes en 0,87 (0,79-0,96; p = 0,0052) voor patiënten zonder diabetes. Vanwege het hogere baselinerisico op cardiovasculaire events, hadden patiënten met diabetes een grotere daling van het absoluut risico na behandeling met evolocumab (resulterend in een number needed to treat van 37 voor patiënten met diabetes, en 62 voor patiënten zonder diabetes, en dit na behandeling gedurende 3 jaar met evolocumab om één primair event te vermijden).
De aanwezigheid van nevenwerkingen was niet significant verschillend tussen beide groepen. Neveneffecten zoals neurocognitieve events of spiergerelateerde events kwamen niet frequenter voor met evolocumab. Er was geen verhoogd risico op het ontwikkelen van diabetes tijdens 2,2 jaar follow-up, noch voor patiënten zonder diabetes (HR 1,05, 0,94-1,17), noch voor patiënten met prediabetes (HR 1,00, 0,89-1,13). De levels van HbA1c en nuchtere glycemie waren vergelijkbaar bij alle patiëntengroepen.
ODYSSEY DM-INSULIN
In ODYSSEY DM-INSULIN bestond de populatie uitsluitend uit met insuline behandelde type 2- (n = 441) en type 1- (n = 76) diabetespatiënten.11 Geïncludeerde patiënten hadden een hoog cardiovasculair risico en LDL-cholesterollevels boven de 70 mg/dl onder maximaal tolereerbare dosis statine of waren statine-intolerant, of ze kregen andere cholesterolverlagende therapie. De BMI van de populatie bedroeg 32 kg/m2. Wat de diabetes betreft, bedroeg de anciënniteit van de ziekte 15 jaar bij de type 2-diabetici, maar de mediane diabetesduur bij de type 1-diabetici was veel hoger (35 jaar). Hetzelfde was ook het geval met de duur van de insulinebehandeling, 35 jaar bij type 1-diabetici versus 6 jaar bij type 2-diabetici. De patiënten werden gerandomiseerd met een verhouding 2:1 tot alirocumab:placebo, dat om de 2 weken subcutaan werd toegediend gedurende 24 weken. In de alirocumabgroep werd gestart met een dosis van 75 mg; deze werd eventueel blind verhoogd tot 150 mg in week 12 als het LDL-cholesterolgehalte > 70 mg/ dL bedroeg in week 8.
Na 24 weken behandeling met alirocumab werd een significante daling van het LDL-cholesterol gezien van 48,2 % bij de type 2-diabetici en van 51,8 % bij de type 1-diabetici, ten opzichte van respectievelijk +0,8 % en -3,9 % in de placebogroepen (beide p < 0,0001) (figuur 1). Bij slechts 22,6 % van de patiënten was er een dosisverhoging van alirocumab van 75 mg naar 150 mg nodig. De bereikte LDL-cholesteroldaling was zeer vergelijkbaar en dus consistent met de andere studies uit het ODYSSEY-programma. Bij 76,4 % van de type 2 en 70,2 % van de type 1-diabetespatiënten werd een LDL-cholesterol < 70 mg/dL bereikt (versus respectievelijk 7,4 % en 5,1 % in de placebogroepen). Eveneens consistent waren de daling van non-HDL-cholesterol (-38,7%), apolipoproteïne B (-36,7 %), totaal cholesterol (-27,6 %) en lp(a) (-18,4 %)(allemaal p < 0,0001), alsook een significante stijging van HDL-cholesterol (+4,4 %, p < 0,01).

De ODYSSEY DM-INSULIN-studie was eveneens belangrijk om de veiligheid te evalueren van het gelijktijdig gebruik van een biologisch agens (insuline) met een monoclonale antistof (alirocumab). Aangezien het gebruik van een hoge dosis statines wordt geassocieerd met een verhoogd risico op diabetes en aangezien er aanwijzingen zijn dat PCSK9 gelinkt wordt met glucosehomeostase, wordt er nauwlettend gekeken naar de mogelijke effecten van PCSK9-inhibitoren op glycemiecontrole.13-16 In de ODYSSEY DM-INSULIN-studie werden geen veranderingen gezien in HbA1c en nuchtere glycemiewaarden, zowel bij de type 2- als type 1-diabetici, en ook de totale dagelijkse insulinedosis en het aantal van andere glucoseverlagende geneesmiddelen bleef onveranderd tijdens de totale duur van de studie. Het uitblijven van een nadelige invloed op de glycemiecontrole werd ook vastgesteld bij de andere PCSK9-inhibitor, evolocumab.17 Uiteraard moet men kritisch blijven en is het wachten op studies met een langere therapieduur (> 2 jaar) om mogelijke nadelige effecten van PCSK9-inhibitoren op glycemiecontrole te evalueren.
Andere aandachtspunten waren allergische reacties ter hoogte van de injectieplaats, neurologische en neurocognitieve nevenwerkingen en de aanwezigheid van antistoffen tegen de PCSK9-inhibitor. Ook hier zijn de problemen uiterst beperkt (en niet verschillend van placebo) en zeer consistent met andere studies.
ODYSSEY DM-DYSLIPIDEMIA
Vooral bij patiënten met type 2 diabetes en gemengde dyslipidemie wordt non-HDL-cholesterol beschouwd als een betere predictor voor cardiovasculair risico.18 Non-HDL-cholesterol bevat namelijk alle circulerende atherogene cholesterol die aanwezig is in apoB-bevattende lipoproteïnenpartikels, zoals VLDL, IDL, LDL en lp(a). In de recente ESC-guidelines wordt zelfs aangeraden om non-HDL-cholesterol als alternatief behandelingsdoel te gebruiken.6 Probleem is dat het effect van cholesterolverlagende therapie op deze parameter minder uitvoerig bestudeerd werd.De meeste guidelines suggereren een non-HDL-cholesterol van 30mg/dL boven de LDL-cholesterolwaarde. Dus voor diabetici met een hoog tot zeer hoog cardiovasculair risico met een LDL-cholesterolstreefwaarde respectievelijk van < 70 of < 100 mg/dL, zou de non-HDL-cholesterolstreefwaarde dan < 100 of < 130 mg/dL bedragen.6 Non-HDL-cholesterol kan gemakkelijk berekend worden uit de routinebloedname: non-HDL-cholesterol = totaal cholesterol - HDL-cholesterol.19
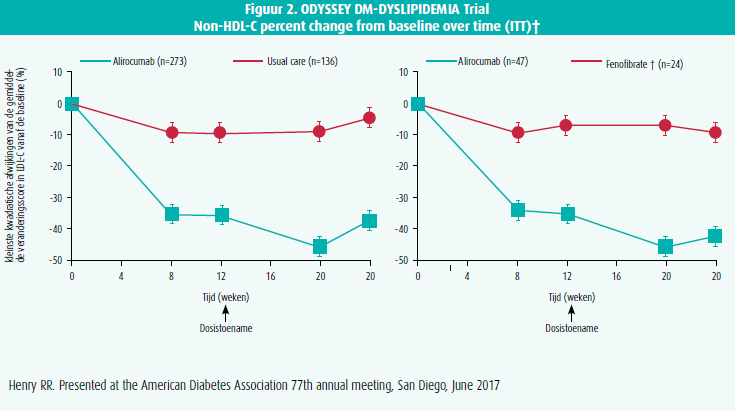
In ODYSSEY DM-DYSLIPIDEMIA bestond de studiepopulatie uit 413 type 2-diabetici met gedocumenteerde cardiovasculaire ziekte of ≥ 1 bijkomende cardiovasculaire risicofactor en gemengde dyslipidemie, gedefinieerd als non-HDL ≥ 100 mg/dL en triglyceriden ≥ 150 en < 500 mg/dL, behandeld met een maximaal tolereerbare dosis statine.12 De verandering in non-HDL-cholesterol na 24 weken behandeling met alirocumab versus gebruikelijke therapie (randomisatie 2:1) was het primair eindpunt van de studie. Ingeval van randomisatie tot gebruikelijke therapie werd er naast het statine een bijkomend cholesterolverlagend middel toegevoegd zoals ezetimibe, fenofibraat, omega 3-vetzuren of nicotinezuur. Na 24 weken behandeling met alirocumab werd een significante daling van het non-HDL-cholesterol gezien van 33,3 % ten opzichte van behandeling met fenofibraat (p < 0,0001) (figuur 2). Bij 65,2 % van de patiënten behandeld met alirocumab werd een non-HDL-cholesterol < 100 mg/dL bereikt, versus 10,1 % bij de patiënten behandeld met fenofibraat. Ook in deze studie bleek alirocumab goed getolereerd te worden en was er geen nadelig effect op HbA1c of nuchtere glycemie.
Besluit
In de subanalyse van FOURIER blijken diabetespatiënten een verhoogd baselinerisico op cardiovasculaire events te hebben.10 Onder behandeling met evolocumab hebben diabetespatiënten een hogere absolute risicoreductie ten opzichte van niet-diabetici leidend tot een verminderd aantal cardiovasculaire events.
Uit de ODYSSEY DM-INSULIN-studie onthouden we dat het gelijktijdig gebruik van alirocumab en insuline bij zowel type 1- als type 2-diabetespatiënten met hypercholesterolemie en een hoog cardiovasculair risico efficiënt is met een significante LDL-cholesterolreductie tot gevolg en bovendien veilig is zonder nadelige invloed op de glycemiecontrole.11
Alirocumab blijkt in de ODYSSEY DM-DYSLIPIDEMIA- studie superieur te zijn in het reduceren van non-HDL-cholesterol ten opzichte van gebruikelijke therapie of ten opzichte van fenofibraat.12
PCSK9-inhibitoren openen dus de weg naar een nieuwe aanpak van cholesterolverlaging, zeker in een hoogrisicopopulatie en in de toekomst mogelijk ook bij diabetespatiënten. Voorlopig blijft het belangrijk eerst de bestaande therapie met statines en ezetimibe te optimaliseren conform hun grote wetenschappelijke bewijslast en de huidige richtlijnen, alvorens een PCSK9-inhibitor te starten.
Referenties - 2013 ACC/AHA guideline on the treatment of blood cholesterol to reduce atherosclerotic cardiovascular risk in adults: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines. GUIDELINE SUMMARY NGC:010477 2014 JUL 1. American College of Cardiology Foundation.
- Silverman, M.G., Ference, B.A., Im, K., Wiviott, S.D., Giugliano, R.P., Grundy, S.M., et al. Association between lowering LDL-C and cardiovascular risk reduction among different therapeutic interventions: a systematic review and meta-analysis. JAMA, 2016, 316, 1289-1297.
- Ference, B.A., Ginsberg, H.N., Graham, I., Ray, K.K., Packard, C.J., Bruckert, E., et al. Low-density lipoproteins cause atherosclerotic cardiovascular disease. 1. Evidence from genetic, epidemiologic, and clinical studies. A consensus statement from the European Atherosclerosis Society Consensus Panel. Eur Heart J, 2017, 38, 2459-2472.
- Heart Protection Study Collaborative Group. MRC/BHF Heart Protection Study of cholesterol lowering with simvastatin in 20536 high-risk individuals: a randomised placebo- controlled trial. Lancet, 2002, 360, 7-22.
- Cannon, C.P., Blazing, M.A., Giugliano, R.P., McCagg, A., White, J.A., Theroux, P., et al. Ezetimibe added to statin therapy after acute coronary syndromes. N Engl J Med, 2015, 372, 2387-2397.
- Piepoli, M.F., Hoes, A.W., Agewall, S., Brotons, C., Catapano, A.L., Cooney, M-T., et al. 2016 European Guidelines on cardiovascular disease prevention in clinical practice. Eur Heart J, 2016, 37, 2315-2381.
- Sabatine, M.S., Giugliano, R.P., Wiviott, S.D., Raal, F.J., Blom, D.J., Robinson, J., et al. Efficacy and safety of evolocumab in reducing lipids and cardiovascular events. N Engl J Med, 2015, 372, 1500-1509.
- Robinson, J.G., Farnier, M., Krempf, M., Bergeron, J., Luc, G., Averna, M., et al. Efficacy and safety of alirocumab in reducing lipids and cardiovascular events. N Engl J Med, 2015, 372, 1489-1499.
- Sabatine, M.S., Giugliano, R.P., Keech, A.C., Honarpour, N., Wiviott, S.D., Murphy, S.A., et al. Evolocumab and clinical outcomes in patients with cardiovascular disease. N Engl J Med, 2017, 376, 1713-1722.
- Sabatine, M.S., Leiter, L.A., Wiviott, S.D., Giuglano, R.P., Deedwania, P., De Ferrari, G.M., et al. Cardiovascular safety and efficacy of the PCSK9 inhibitor evolocumab in patients with and without diabetes and the effect of evolocumab on glycaemia and risk of new-onset diabetes: a prespecified analysis of the FOURIER randomised controlled trial. Lancet Diabetes Endocrinol, 2017, 5, 941-950.
- Leiter, L.A., Cariou, B., Müller-Wieland, D., Colhoun, H.M., Del Prato, S., Tinahones, F.J., et al. Efficacy and safety of alirocumab in insulin- treated individuals with type 1 or type 2 diabetes and high cardiovascular risk: The ODYSSEY DM-INSULIN randomized trial. Diabetes Obes Metab, 2017, 19, 1781-1792.
- Müller-Wieland, D., Leiter, L.A., Cariou, B., Letierce, A., Colhoun, H.M., Del Prato, S., et al. Design and rationale of the ODYSSEY DM-DYSLIPIDEMIA trial: lipid-lowering efficacy of alirocumab in individuals with type 2 diabetes and mixed dyslipidemia at high cardiovascular risk. Cardiovasc Diabetol, 2017, 16: 70 (DOI 10.1186/s12933-017-0552-4)
- Ridker, P.M., Pradhan, A., MacFadyen, J.G., Libby, P., Glynn, R.J. Cardiovascular benefits and diabetes risks of statin therapy in primary prevention: an analysis from the JUPITER trial. Lancet, 2012, 380, 565-571.
- Sattar, N., Preiss, D., Murray, H.M., Welsh, P., Buckley, B.M., de Craen, A.J.M., et al. Statins and risk of incident diabetes: a collaborative meta-analysis of randomised statin trials. Lancet, 2010, 375, 735-742.
- Preiss, D., Seshasai, S.R., Welsh, P., Murphy, S.A., Ho, J.E., Waters, D.D., et al. Risk of incident diabetes with intensive-dose compared with moderate-dose statin therapy: a meta-analysis. JAMA, 2011, 305, 2556-2564.
- Schmidt, A.F., Swerdlow, D.I., Holmes, M.V., Patel, R.S., Fairhurst-Hunter, Z., Lyall, D.M., et al. PCSK9 genetic variants and risk of type 2 diabetes: a mendelian randomisation study. Lancet Diabetes Endocrinol, 2017, 5, 97-105.
- Blom, D.J., Koren, M.J., Roth, E., Monsalvo, M.L., Djedjos, C.S., Nelson, P., et al. Evaluation of the efficacy, safety and glycemic effects of evolocumab (AMG 145) in hypercholesterolaemic patients stratified by glycemic status and metabolic syndrome. Diabetes Obes Metab, 2017, 19, 98-107.
- Verbeek, R., Hovingh, G.K., Boekholdt, S.M. Non-high-density lipoprotein cholesterol: current status as cardiovascular marker. Curr Opin Lipidol, 2015, 26, 502-510.
- de Vries, M., Klop, B., Castro Cabezas, M. The use of the non-fasting lipid profile for lipid-lowering therapy in clinical practice- point of view. Atherosclerosis, 2014, 234, 473-475.
Aucun élément du site web ne peut être reproduit, modifié, diffusé, vendu, publié ou utilisé à des fins commerciales sans autorisation écrite préalable de l’éditeur. Il est également interdit de sauvegarder cette information par voie électronique ou de l’utiliser à des fins illégales.