De PCSK9-inhibitoren zijn een zeer beloftevolle nieuwe geneesmiddelenklasse voor de preventie van cardiovasculaire aandoeningen dankzij hun potentie om het serum-LDL-cholesterol sterk te reduceren. Deze monoclonale antilichamen bereiken deze LDL-reductie door inhibitie van het proprotein convertase subtilisin/kexin type 9 (PCSK9), wat resulteert in een verminderde LDL-receptordegradatie en een stijging van de recirculatie van de receptor aan het celoppervlak van hepatocyten. Deze LDL-cholesteroldaling blijft echter een surrogaatmerker, want harde data over effectieve benefits van de PCSK9- inhibitoren op de klinische cardiovasculaire outcome ontbreken nog. In dit satellietsymposium onderbouwden prof. dr. Wolfgang Koenig (Deutsches Herzzentrum Münich) en prof. dr. Kausik Ray (Imperial College London) de te verwachten klinische impact van deze nieuwe geneesmiddelenklasse, in afwachting van verdere studies met als doel een reductie van coronaire atheromatose en cardiovasculaire events aan te tonen.
PCSK9-inhibitoren: impact op plaqueregressie?
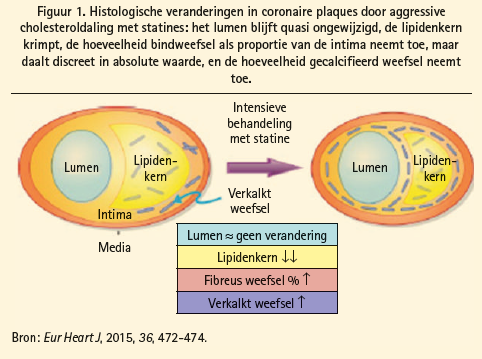
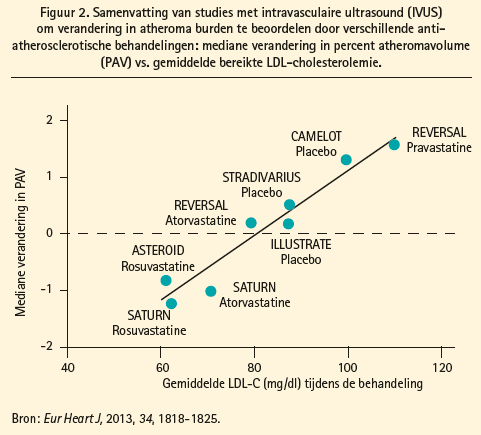
De laatste 20 jaar werd in klinische studies stellig bewezen dat LDL-daling (voornamelijk door statines) in staat is het risico op acute coronaire syndromen en ischemische beroerte te reduceren. Het mechanisme dat tot deze verbetering van klinische outcome leidt, blijft echter controversieel. De cholesteroldaling reduceert namelijk slechts minimaal de luminale stenosegraad in angiografische studies, maar bereikt waarschijnlijk zijn klinisch effect door plaquestabilisatie, waardoor deze plaques minder aanleiding geven tot trombotische complicaties. Histologisch leidde intensieve behandeling met statines tot een afname van de lipidenkern, een toename van het percentage van bindweefsel in relatie tot de intimadikte en een toename van de calcificatiegraad1 (figuur 1). In een meta-analyse van studies met intravasculaire ultrasound (IVUS) werd een duidelijke lineaire relatie tussen de LDLcholesteroldaling en de reductie van het percentage van atheromavorming in de kransslagaders aangetoond (figuur 2), wat dan weer gecorreleerd is met daling van het risico op cardiovasculaire events.2
De GLAGOV-studie bestudeerde of een incrementele daling van de LDL-cholesterol door toevoeging van de PCSK9- inhibitor evolocumab aan de maximaal getolereerde dosis statine, resulteerde in een verdere regressie van het coronair atheromavolume.3 Nu zijn er interessante recente data die suggereren dat de effecten van de PCSK9-inhibitoren op plaqueregressie niet enkel via daling van de LDL-cholesterolemie zouden verkregen worden. Het PCSK9 zou namelijk ook op een directe lokale manier via het promoten van inflammatie tot plaquevorming bijdragen. In de ATHEROREMO- IVUS-studie was de serum PCSK9- waarde lineair gecorreleerd met de fractie en hoeveelheid aan necrotische kern in atherosclerotische plaques, en dit onafhankelijk van de LDL-cholesterolemie.4 PCSK9-serumwaarden zijn ook gecorreleerd met klinische outcome: Leander et al. demonstreerden een duidelijk relatie tussen de serumconcentratie van PCSK9 en het toekomstig risico op cardiovasculaire aandoeningen, na correctie voor andere klassieke cardiovasculaire risicofactoren; 5 en ook in de carotiden was de serum PCSK9-concentratie gecorreleerd met de progressie van atheromatose over een periode van 10 jaar, ook nu weer onafhankelijk van de LDL-cholesterol.6 In afwachting van de gretig verlangde klinische outcomestudies zal de GLAGOV- studie alvast belangrijke mechanistische, efficaciteits- en veiligheidsgegevens over de PCSK9-inhibitoren verschaffen. De resultaten van deze studie zullen gepresenteerd worden op het American Heart Association congres in november 2016.
PCSK9-inhibitoren: doelpopulatie voor cardiovasculaire preventie?
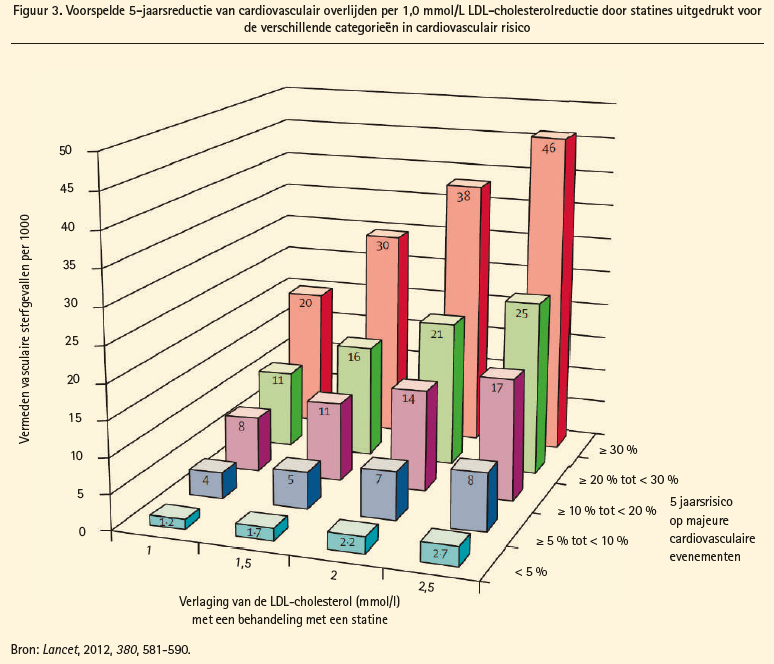
Statinegemedieerde LDL-cholesteroldaling faalt nog altijd om meer dan de helft aan cardiovasculaire events te voorkomen. Het grootste klinische benefit van de statines wordt gezien bij die patiënten met het hoogste baseline cardiovasculaire risico, en die waarbij statines de grootste LDL-reductie bereiken7 (figuur 3). In de IMPROVE-IT-studie werd een extra daling van de LDL-cholesterol verkregen door toevoeging van ezetimibe aan een behandeling met simvastatine, wat leidde tot een significante daling van cardiovasculaire events in vergelijking met statinemonotherapie. 8 Daarom is er grote hoop voor de PCSK9-inhibitoren, die in staat zijn om de LDL-cholesterolemie zelfs 55 tot 75 % extra te reduceren bij patiënten die al onder behandeling met een statine staan. Ook in patiënten met familiale hypercholesterolemie wordt met deze nieuwe medicatie tot 60 % daling van de LDL-cholesterolemie verkregen, ongeacht de onderliggende mutatie.9
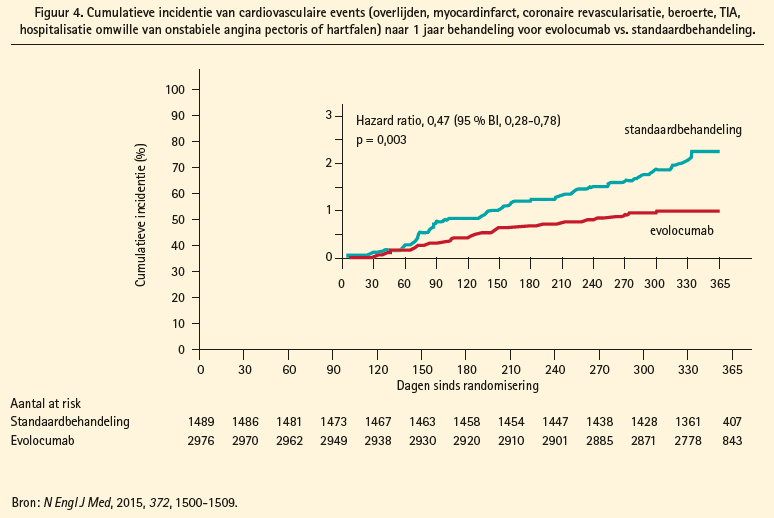
Statines in maximaal getolereerde dosis blijven de hoeksteen van cardiovasculaire preventie in hoogrisicopatiënten, maar patiënten met blijvend hoge LDLcholesterolemie ondanks statine-inname, met familiale hypercholesterolemie of met intolerantie voor statines vormen in eerste instantie een attractieve doelgroep voor onderhoudsbehandeling met een PCSK9-inhibitor. Deze doelgroep kan potentieel nog verruimen als uit de lopende klinische outcomestudies zou blijken dat een verdere daling van de LDL-cholesterol resulteert in verbetering van cardiovasculaire outcome, zonder ernstige nevenwerkingen. Een vooraf gespecifieerde exploratieve analyse na 1 jaar evolocumabbehandeling toonde alvast gunstige resultaten met betere cardiovasculaire outcome10 (figuur 4), maar deze resultaten zijn nog voorbarig. Bijwerkingen werden even frequent gerapporteerd in de PCSK9- als in de placeboarm, behalve neurocognitieve events, die frequenter voorkwamen in de PCSK9-arm (onafhankelijk van de toenmalige LDL-waarde). Vier grote klinische outcomestudies (FOURRIER, ODYSSEY, SPIRE-1 en SPIRE-2) zijn momenteel lopende, en zullen het voordeel op de cardiovasculaire outcome en de veiligheid van de PCSK9-inhibitoren evalueren. De eerste resultaten hiervan worden verwacht in 2017.
Referenties
- Libby, P. How does lipid lowering prevent coronary events? New insights from human imaging trials. Eur Heart J, 2015, 36, 472-474.
- Nicholls, S.J., Hsu, A., Wolski, K., Hu, B., Bayturan, O., Lavoie, A. et al. Intravascular ultrasound-derived measures of coronary atherosclerotic plaque burden and clinical outcome. J Am Coll Cardiol, 2010, 55, 2399-2407.
- Puri, R., Nissen, S.E., Somaratne, R., Cho, L., Kastelein, J.J., Ballantyne, C.M., et al. Impact of PCSK9 inhibition on coronary atheroma progression: Rationale and design of Global Assessment of Plaque Regression with a PCSK9 Antibody as Measured by Intravascular Ultrasound (GLAGOV). Am Heart J, 2016, 176, 83-92.
- Cheng, J.M., Oemrawsingh, R.M., Garcia-Garcia, H.M., Boersma, E., van Geuns, R.J., Serruys, P.W. et al. PCSK9 in relation to coronary plaque inflammation: Results of the ATHEROREMO-IVUS study. Atherosclerosis, 2016, 248, 117-122.
- Leander, K., Mälarstig, A., Van't Hooft, F.M., Hyde, C., Hellénius, M.L., Troutt, J.S. et al. Circulating Proprotein Convertase Subtilisin/Kexin Type 9 (PCSK9) Predicts Future Risk of Cardiovascular Events Independently of Established Risk Factors. Circulation, 2016, 133, 1230-1239.
- Xie, W., Liu, J., Wang, W., Wang, M., Qi, Y., Zhao, F. et al. Association between plasma PCSK9 levels and 10-year progression of carotid atherosclerosis beyond LDL-C: A cohort study. Int J Cardiol, 2016, 215, 293- 298.
- Cholesterol Treatment Trialists' (CTT) Collaborators, Mihaylova, B., Emberson, J., Blackwell, L., Keech, A., Simes, J. et al. The effects of lowering LDL cholesterol with statin therapy in people at low risk of vascular disease: meta-analysis of individual data from 27 randomized trials. Lancet, 2012, 380, 581-590.
- Cannon, C.P., Blazing, M.A., Giugliano, R.P., McCagg, A., White, J.A., Theroux, P., et al. Ezetimibe Added to Statin Therapy after Acute Coronary Syndromes. N Engl J Med, 2015, 372, 2387-2397.
- Raal, F.J., Stein, E.A., Dufour, R., Turner, T., Civeira, F., Burgess, L., et al. PCSK9 inhibition with evolocumab (AMG 145) in heterozygous familial hypercholesterolaemia (RUTHERFORD-2): a randomized, doubleblind, placebo-controlled trial. Lancet, 2015, 385, 331-340.
- Sabatine, M.S., Giugliano, R.P., Wiviott, S.D., Raal, F.J., Blom, D.J., Robinson, J., et al. Efficacy and safety of evolocumab in reducing lipids and cardiovascular events. N Engl J Med, 2015, 372, 1500-1509.
Niets van de website mag gebruikt worden voor reproductie, aanpassing, verspreiding, verkoop, publicatie of commerciële doeleinden zonder voorafgaande schriftelijke toestemming van de uitgever. Het is ook verboden om deze informatie elektronisch op te slaan of te gebruiken voor onwettige doeleinden.