Inleiding
Eerder dit jaar werden de resultaten van de REPAIR-studie gepubliceerd in The Journal of Heart and Lung Transplantation. 1 Dit was de eerste multicentrische studie waarin het gunstige effect van macitentan werd aangetoond door middel van cardiale MRI en rechterhartkatheterisatie bij patiënten die lijden aan pulmonale arteriële hypertensie (PAH). Zowel het slagvolume van het rechterventrikel (RVSV) als de pulmonale vasculaire weerstand (PVW) bleken na 26 weken behandeling significant beter. Ook op de secundaire eindpunten bleek macitentan een gunstig effect te vertonen. Dit artikel beoogt een overzicht van deze studieresultaten te geven.
Achtergrond
PAH is een zeldzame en chronisch progressieve aandoening, gekarakteriseerd door een verhoogde weerstand in het pulmonair vaatbed. Onbehandeld geeft de ziekte aanleiding tot de ontwikkeling van rechterhartfalen en de dood.2 De prevalentie in Europa wordt geschat op 15-60 per miljoen inwoners.2 Vroege symptomen zijn vaak verraderlijk en aspecifiek (bijvoorbeeld dyspnoe, vermoeidheid en duizeligheid), waardoor het tijdig stellen van een correcte diagnose vaak erg moeilijk blijkt.3 Het uitvoeren van een rechterhartkatheterisatie vormt daarom een essentieel onderdeel, waarbij de gemiddelde pulmonale arteriële druk (mPAP) in rust meer dan 25 mmHg moet bedragen en de wiggedruk minder dan 15 mmHg.2
Tot op heden is er voor deze aandoening geen curatieve therapie voorhanden en richt het beschikbare arsenaal aan geneesmiddelen zich voornamelijk op symptoomreductie en preventie van ziekteprogressie. In de laatste decennia zijn in dit kader diverse middelen goedgekeurd door de internationale autoriteiten. Globaal zijn er drie belangrijke signaalwegen (Engels: pathways) die een rol spelen in de pathogenese van PAH en als doelwit voor therapie worden gebruikt: de stikstofmonoxide/cGMP pathway, de prostacycline pathway en de endotheline pathway.4 Macitentan richt zich op de laatst genoemde pathway door de endothelinereceptor te inhiberen. Het middel werd in 2013 goedgekeurd door zowel de Amerikaanse als de Europese autoriteiten.4 Hiervoor baseerde men zich voornamelijk op data uit de SERAPHIN-trial, waaruit bleek dat een behandeling met macitentan aanleiding gaf tot een significante daling in de morbiditeit en mortaliteit van 45 %.5 Vergeleken met de andere endothelinereceptorantagonisten (bosentan en ambrisentan) blijkt macitentan bovendien geassocieerd te zijn met minder geneesmiddelinteracties, een verlengde receptorbindingsactiviteit, een betere weefselpenetratie, een sterker inhiberend effect en een gunstiger bijwerkingsprofiel.4 Het effect van dit geneesmiddel op de rechterventrikelfunctie, een van de belangrijkste determinanten van prognose van PAHpatiënten, werd voorheen nog niet onderzocht door middel van een cardiale MRI en hierin is deze studie dus de eerste in zijn soort.
Methodes
De REPAIR-studie was een open label, niet-placebogecontroleerde, multicentrische, fase 4-studie waarin patiënten gedurende 52 weken werden behandeld met macitentan 10 mg daags. Het primaire eindpunt bestond uit twee factoren, gemeten op week 26 na de start van de behandeling (figuur 1). Enerzijds het RVSV, gemeten door middel van een cardiale MRI, en anderzijds de PVW, gemeten door middel van rechterhartkatheterisatie. Beide waarden werden vergeleken met de respectievelijke uitgangswaarden bij de start van het onderzoek. Secundaire eindpunten werden eveneens gemeten op week 26 en vergeleken met hun respectievelijke uitgangswaarden. Deze waren: rechterventrikelvolumes en -myocardmassa, afstand op een 6 minutenwandeltest (6MWT) en WHO-PAH functionele klasse (WHO-FC). Daarnaast werden nog enkele exploratieve eindpunten onderzocht, waaronder het verschil in NT-proBNP, mPAP, gemiddelde rechter atriale druk (mRAP) en cardiale index.

Voorts werden drie behandelgroepen gedefinieerd: ten eerste PAH-patiënten zonder actieve behandeling, waarbij macitentan in monotherapie werd gestart, ten tweede patiënten zonder actieve behandeling waarbij meteen een combinatietherapie werd gestart (macitentan + een fosfodiësterase 5-remmer (FD5R)) en ten derde PAH-patiënten die reeds onder stabiele behandeling met een FD5R stonden op het moment van inclusie en waarbij macitentan geassocieerd werd aan de therapie.
Voor de start van de studie werd een statistische poweranalyse uitgevoerd op basis van voorgaande studies waaruit bleek dat een stijging in RVSV van 8 ml en een daling in PVW van 18 % als klinisch relevant mocht worden beschouwd.
Op basis van deze analyse had men 100 patiënten moeten includeren, maar beide primaire eindpunten bleken al significant bij een interimanalyse van de eerste 42 patiënten. Bijgevolg werd de studie-inclusie vroegtijdig gestopt. Het uiteindelijke aantal geïncludeerde patiënten waarbij de volledige studie werd doorlopen bedroeg 71. Voorts werden potentiële bijwerkingen opgevolgd bij iedereen die minstens één dosis macitentan had ontvangen (87 patiënten), en dit tot 30 dagen na de behandeling.
De belangrijkste inclusiecriteria waren leeftijd (18-74 jaar), etiologie van de PAH (idiopathisch, erfelijk, geneesmiddelgeïnduceerd, geassocieerd met bindweefselaandoeningen of congenitaal hartlijden), WHO-FC I-III en een afstand op een 6MWT van meer dan 150 m op het moment van screening. Op het moment van screening mochten patiënten nog geen PAH-therapie innemen, tenzij een PD5R met stabiele dosis gedurende meer dan 3 maanden. De belangrijkste exclusiecriteria waren het concomitantgebruik van andere endothelinereceptorantagonisten of een andere klasse van PAH-medicatie (anders dan PD5R).
Resultaten
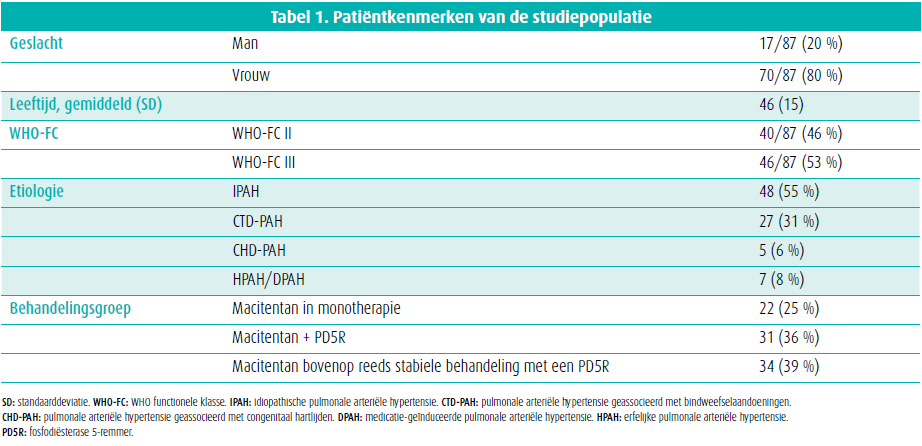
De kenmerken van de uiteindelijke patiëntenpopulatie worden weergeven in tabel 1. De gemiddelde leeftijd bedroeg 46 jaar en het merendeel (80 %) was vrouwelijk. Bovendien bevonden de meeste patiënten zich in een WHO-FC II (46 %) of III (53 %). Bij 25 % van de patiënten werd macitentan gestart als monotherapie, bij 36 % simultaan met een FD5R en bij nog eens 39 % van de patiënten als toevoeging op een reeds bestaande behandeling met een FD5R.
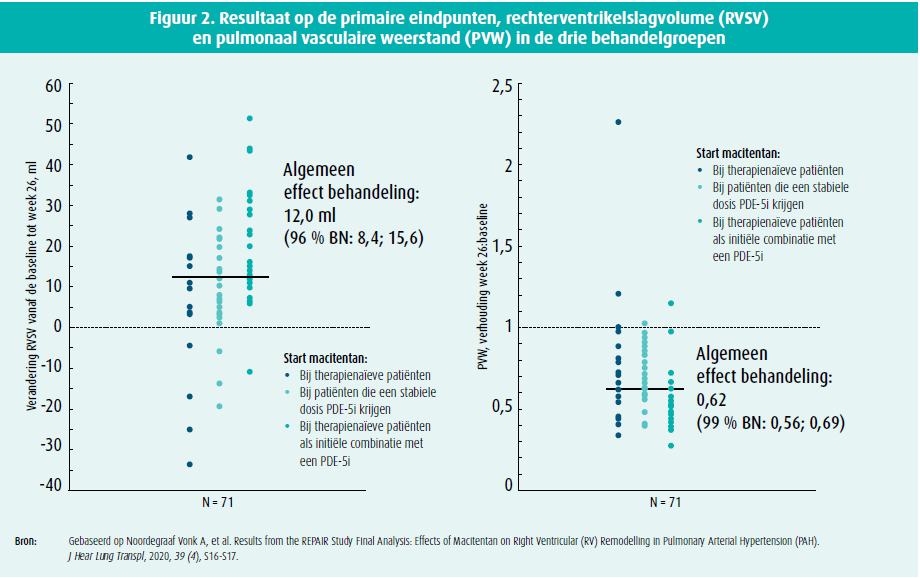
De resultaten van de studie worden weergeven in tabel 2. Wat het primaire eindpunt betreft, bleek op week 26 van de behandeling het RVSV gestegen met 12 ml (96 % BI 8,4 - 15,6; P-waarde < 0,0001) en de PVW gedaald met 38 % (ratio 0,62; 99 % BI 0,56 - 0,69; P-waarde < 0,0001) (figuur 2). Ook werden betekenisvolle verschillen opgemerkt bij de secundaire eindpunten: een daling in zowel het rechterventrikel eind diastolisch volume, als eind systolisch volume (resp. 6,2 ml en 16,1 ml), een daling in rechterventrikelmyocardmassa van 10,5 g, een stijging in rechterventrikelejectiefractie van 10,6 % en een stijging in afstand tijdens een 6MWT van 36 meter. Tevens bleek 56,3 % van de patiënten een betere WHO-FC te hebben na 26 weken, terwijl de overige patiënten zich in dezelfde klasse bevonden. Daarnaast zag men een significante daling in mPAP (- 7,73 mmHg), stijging in cardiale index (0,54 l/min/m²) en een niet-significante daling in mRAP (0,32 mmHg).

De meest voorkomende bijwerkingen waren het optreden van perifeer oedeem (21,8 %), hoofdpijnklachten (20,7 %) en duizeligheid (13,8 %).
Conclusie
De REPAIR-studie is de eerste in zijn soort waarin door middel van een cardiale MRI en rechterhartkatheterisatie wordt aangetoond dat een behandeling met macitentan aanleiding geeft tot een verbeterde rechterventrikelfunctie en -hemodynamiek bij patiënten die lijden aan pulmonale arteriële hypertensie en dit zowel in monotherapie als gecombineerd met een fosfodiësterase 5-remmer.
Referenties
- Noordegraaf Vonk, A., Channick, R., Cottreel, E., Kiely, D., Martin, N., Moiseeva, O. et al. Results from the REPAIR Study Final Analysis: Effects of Macitentan on Right Ventricular (RV) Remodelling in Pulmonary Arterial Hypertension (PAH). J Hear Lung Transpl, 2020, 39 (4), S16-S17.
- Galiè, N., Humbert, M., Vachiery, J-L., Gibbs, S., Lang, I., Torbicki, A. et al. 2015 ESC/ERS Guidelines for the diagnosis and treatment of pulmonary hypertension: The Joint Task Force for the Diagnosis and Treatment of Pulmonary Hypertension of the European Society of Cardiology (ESC) and the European Respiratory Society (ERS): Endorsed by: Association for European Paediatric and Congenital Cardiology (AEPC), International Society for Heart and Lung Transplantation (ISHLT). Eur Heart J, 2016, 37 (1), 67-119.
- Lai, Y-C., Potoka, K.C., Champion, H.C., Mora, A.L., Gladwin, M.T. Pulmonary arterial hypertension: the clinical syndrome. Circ Res, 2014, 115 (1), 115-130.
- Bedan, M., Grimm, D., Wehland, M., Simonsen, U., Infanger, M., Krüger, M. A Focus on Macitentan in the Treatment of Pulmonary Arterial Hypertension. Basic Clin Pharmacol Toxicol, 2018, 123 (2), 103-113.
- Pulido, T., Adzerikho, I., Channick, R.N., Delcroix, M., Galiè, N., Ghofrani, H-A. et al. Macitentan and morbidity and mortality in pulmonary arterial hypertension. N Engl J Med, 2013, 369 (9), 809-818.
Niets van de website mag gebruikt worden voor reproductie, aanpassing, verspreiding, verkoop, publicatie of commerciële doeleinden zonder voorafgaande schriftelijke toestemming van de uitgever. Het is ook verboden om deze informatie elektronisch op te slaan of te gebruiken voor onwettige doeleinden.