Het EuroValve-congres ging dit jaar door in Barcelona en de organisatie ging opnieuw uit van leden van de European Association of Cardiovascular Imaging (EACVI) en van de ESC Working Group on Valvular Heart Disease.
Het accent lag de eerste dag op hoe we de zorg voor patiënten met kleplijden kunnen verbeteren en op de nieuwe behandelingsmethoden van aortaklepstenose. We willen daarop dieper ingaan.
Zowel John Chambers (kleplijden), als Gilbert Habib (endocarditis) legde de nadruk op de multidisciplinaire aanpak van deze patiënten. Dat vertaalt zich in de noodzaak om zich te organiseren in een hartklepkliniek en een endocarditisteam samen te stellen. De nood aan een multidisciplinair overleg voor patiënten met kleplijden ligt voor de hand in een tijdperk waarin de patiënt met kleplijden complexer wordt (ouder, fragieler, met multicomorbiditeit). Bovendien is het behandelingsarsenaal voor de patiënt met kleplijden ook uitgebreider geworden en speelt niet alleen de hartchirurg maar ook de cardioloog daarin een rol. De snelheid waarmee nieuwe technologie evolueert, maakt de correcte benadering van de patiënt met kleplijden nog moeilijker. Zowel binnen de interventionele cardiologie, als de hartchirurgie zijn er de laatste jaren belangrijke nieuwe technieken ontwikkeld.
Het principe van de hartklepkliniek werd voor het eerst duidelijk gepromoot met het artikel van Lancellotti et al., ook al gebied de eerlijkheid te vermelden dat ziekenhuizen zoals in Wenen al lang zo georganiseerd zijn.1 Het standaardmodel dat in figuur 1 voorgesteld wordt, spreekt voor zichzelf.
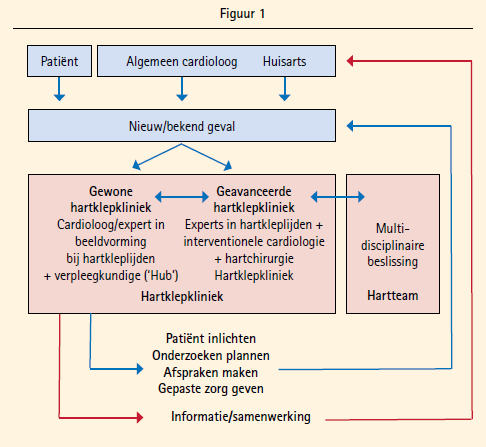
Of men zich in het ziekenhuis organiseert in een 'standard' klepkliniek of een 'advanced' klepkliniek zal afhangen of men werkt in een ziekenhuis met interventionele cardiologie en cardiochirurgie, ofwel of men eerder samenwerkt met een ziekenhuis die deze diensten aanbiedt. Meestal bestaat de draaiende motor van de klepkliniek uit een cardioloog, gespecialiseerd in beeldvorming, en een verpleegkundige. Zij moeten de klepkliniek zo organiseren dat te gepasten tijde een multidisciplinair team samenkomt om, waar nodig, patiënten multidisciplinair te bespreken.
Infectieuze endocarditis (IE) blijft een hartaandoening met een torenhoge inziekenhuismortaliteit. Ook hier stelt de Europese Vereniging van Cardiologie voor een multidisciplinaire aanpak te promoten binnen het ziekenhuis met het oprichten van een endocarditisteam.2 De bedoeling is om zeer snel, bij het begin van de diagnose of het vermoeden ervan, multidisciplinair de aanpak te bepalen voor wat betreft diagnose (microbiologie, beeldvorming) en aanpak (spoed, urgente of electieve chirurgie versus medicamenteuze aanpak met gepaste antibioticakeuze en duur) (tabel 1).
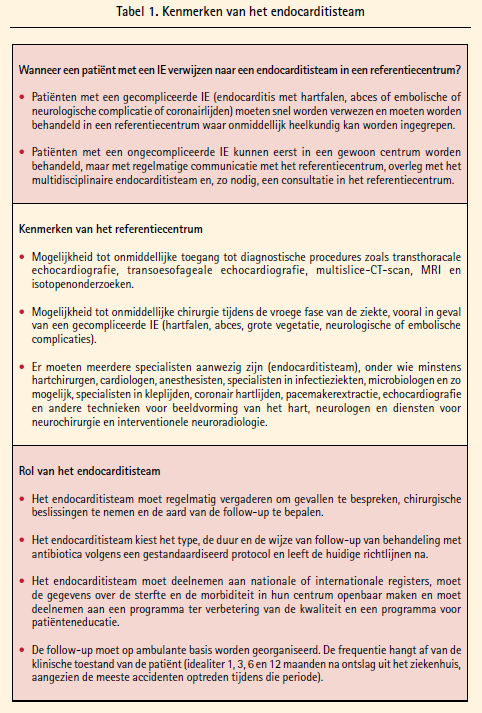
Tijdelijke doorverwijzing van het lokale centrum naar het referentiecentrum voor gecompliceerde IE-gevallen en een regelmatige communicatie met het referentiecentrum voor de niet-gecompliceerde gevallen is van cruciaal belang. In een Belgische context zal dit georganiseerd moeten worden binnen het netwerk.
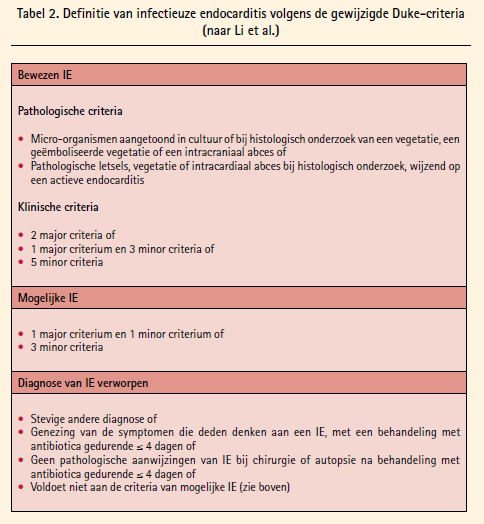
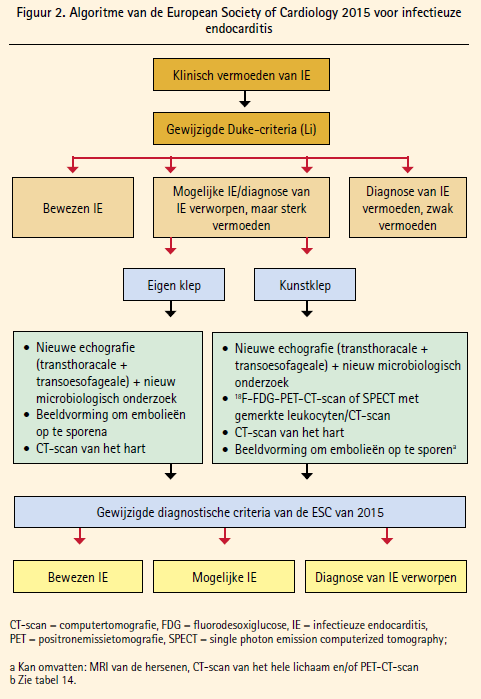
Op diagnostisch vlak hebben nieuwe beeldvormingstechnieken de richtlijnen veranderd. Zowel MRI, dat cerebrale embolen kan aantonen, als PET-CT, dat de infectiehaard aantoont, heeft een plaats ingenomen in de diagnose van IE. Echocardiografie blijft een sleutelrol spelen, maar voornamelijk in IE op klepprothesen en op devices (PM, CRT, Defibrillatoren, LVAD …) heeft PET-CT zijn intrede gemaakt. Belangrijk om te weten is dat ook PET-CT geen accuraatheid heeft van 100 % en vals-positieve en vals-negatieve resultaten kan geven en dat de gebreken van deze techniek herkend en aangeleerd moeten worden. Veranderingen in de diagnose van IE worden weergegeven in de tabellen 2 en 3 en figuur 2.

Aortaklepstenose
De voordrachten over de behandeling van aortaklepstenose resumeren we hieronder.
1. De Partner 1-trials hebben aangetoond dat TAVI een minstens evenwaardig alternatief is voor chirurgische aortaklepvervanging bij de patiënten met een hoog operatief risico. Zij toonden ook aan dat TAVI superieur is aan medische therapie bij de inoperabele patiënten. Aangezien hierop al werd ingegaan bij eerdere edities van het Tijdschrift voor Cardiologie zullen we dit in dit artikel niet doen.
2. De FU van de patiënten geïncludeerd in de TAVI-trials heeft aangetoond dat deze resultaten zich bevestigen na 2, 3 en nu ook 5 jaar. In de laatste publicatie, met FU na 5 jaar werden de volgende resultaten vermeld: na 5 jaar was het risico op dood 67,8 % in de TAVR-groep (transkatheter) en 62,4 % in de SAVR-groep (chirurgie) (hazard ratio 1,04, 95 % CI 0,86-1,24; p = 0,76). Matige of ernstige aortaklepregurgitatie werd gevonden bij 14 % van de TAVR-groep en bij 1 % in de SAVR-groep (p < 0,0001), en deze regurgitatie was wel significant gerelateerd aan een verhoogde mortaliteit na 5 jaar in de TAVR-groep (72,4 % voor matige of ernstige regurgitatie vs 56,6 % voor milde of lichtere regurgitatie; p = 0,003). Deze resultaten zijn dus erg bemoedigend voor TAVI wanneer we een FU van 5 jaar beschouwen. Er moet aandacht geschonken worden aan het feit dat een paravalvulair lek bij TAVI een belangrijk probleem is en dat dit in de toekomst opgelost moet worden. Het goede nieuws is dat nieuwe percutane prothesen die herpositioneerbaar zijn en/of een speciale ringontwikkeling hebben gekregen nu al een belangrijk deel van de oplossing bieden. Ook al blijft het grote verschil met chirurgie dat er geen debulking van de verkalkingen van de stenotische aortaklep gebeurt bij een percutane behandeling, uiteindelijk zullen nieuwe designs van nieuwe prothesen een belangrijk antwoord bieden op deze tekortkoming van de eerste modellen van percutane aortakleppen.
3. De superioriteit van TAVI ten opzichte van de chirurgische klepvervanging geldt voornamelijk voor de transarteriële en niet voor de apicale TAVI-procedure. Al van bij de eerste grote trials bleek dat de voorkeur voor elke TAVI-implantatie moet gaan naar de transfemorale toegangsweg. Zelfs als er rekening wordt gehouden met een propensity score-compensatie voor eenzelfde operatief risico blijft er een groot voordeel bestaan voor de transfemorale weg. Ook al zijn de meesten ervan overtuigd dat er niet volledig gecompenseerd kan worden om perfect vergelijkbare groepen te verkrijgen, daar waar de resultaten van de transfemorale weg erg moedgevend zijn, blijft de mortaliteit voor de transapicale weg hoog. Daarom moet deze techniek dan ook gebruikt worden voor een heel specifieke groep, waarbij de transfemorale weg onmogelijk is, chirurgie geen optie is en de levensverwachting van de patiënt met AS voldoende groot is.4
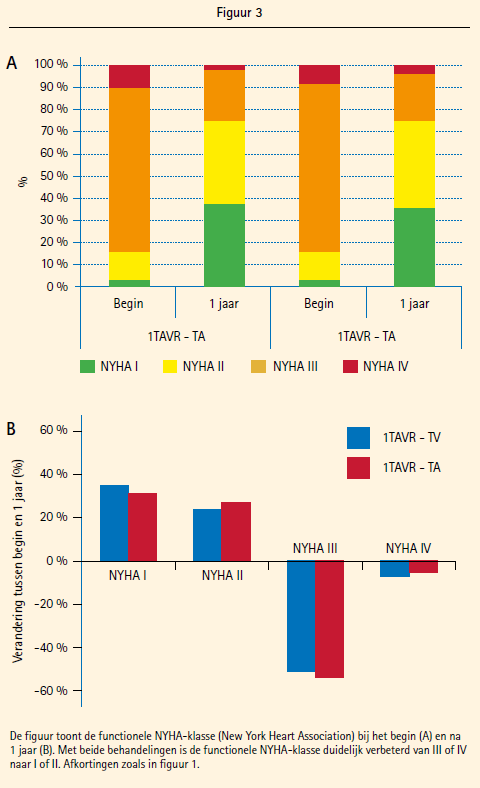
4. Real-life registers zoals GARY (Duitsland) maar ook meta-analyses van andere Europese registers bevestigen de veiligheid van de TAVI-procedure en tonen aan dat TAVI de levenskwaliteit van de patiënten verbetert.5 Zo was er een gunstige evolutie van de NYHA-classificatie (TAVR-TV= TAVI via vasculaire weg en TAVR-TA= TAVI via transapicale weg) (figuur 3).
Ook andere parameters voor levenskwaliteit verbeterden na TAVI.
5. De Partner 2-trial toonde aan dat TAVI evenwaardig is aan chirurgische aortaklepvervanging bij de intermediairrisicogroep en ook daar was de transfemorale weg superieur wat betreft totale mortaliteit en invaliderende beroerte. Overlijden en invaliderende beroerte werden even vaak gezien in de TAVIgroep als in de chirurgiegroep (p = 0,001 voor non inferiority). De event rate bedroeg na 2 jaar 19,3 % in de TAVIgroep en 21,1 % in de chirurgiegroep (hazard ratio in de TAVR-groep, 0,89; 95% CI, 0,73-1,09; p = 0,25). Opnieuw bleek de transfemorale TAVI-groep het zelfs beter te doen dan de chirurgiegroep (hazard ratio, 0,79; 95% CI, 0,62 - 1,00; p = 0,05), terwijl de twee transthoracale benaderingen, transapicale TAVI en chirurgie, dezelfde resultaten gaven. TAVI gaf grotere klepoppervlakten en minder nierfalen en ernstige bloeding en minder nieuwe voorkamerfibrillatie. Chirurgie van haar kant leidde tot minder vasculaire complicaties en minder paravalvulaire lekkage.
6. De NOTION-trial toonde aan dat de resultaten na 1 jaar van totale mortaliteit, beroerte en acuut myocardinfarct evenwaardig waren voor TAVI en chirurgische aortaklepvervanging in een laagrisicopopulatie met aortaklepstenose.6 De belangrijkste opmerking bij deze resultaten is de erg korte FU van 1 jaar, wat bij een laag risico en dus ook jongere populatie een erg belangrijke tekortkoming is van deze studie. De onderzoekers vonden ook meer nood tot pacemakerimplantaties in de TAVI-groep, wat naast paravalvulair lek ook een regelmatig weerkerend probleem van TAVI is. Meer ervaring en herpositioneerbare klepprothesen kunnen de resultaten in de toekomst zeker verbeteren.
7. Real-life data van het GARY-register tonen dat de mortaliteit na 1 jaar van TAVI hoger was dan na chirurgische aortaklepvervanging. Aangezien de groepen echter sterk van elkaar verschilden en allicht niet volledig vergelijkbaar waren, ook niet na een propensity-scoresysteem toegepast te hebben, besloot het FDA voorlopig zijn goedkeuring voor de intermediairrisicogroep niet te herzien.
8. Langetermijndata, na 5 jaar, zijn echter nog niet voorhanden voor TAVI-trials en dus blijft voorzichtigheid belangrijk als we de indicaties zouden verschuiven naar de lagererisicogroep en dus jongere leeftijdsgroep. Verschillende elementen geven aan dat de grenzen van TAVI verder verlegd zullen worden naar de jongere patiënten en de lagerrisicopatiënten: interesse van cardiologen en cardiochirurgen (in deze laatste groep is het opvallend om critici te horen, want zij voeren meestal zelf geen katheterprocedures uit, terwijl enthousiaste verdedigers van TAVI in functie van het type patiënt een chirurgische benadering of een percutane procedure aanbieden), interesse van de industrie en een grote groep van patiënten die moet behandeld worden (nog meer in de komende jaren door de vergrijzing). Toch moeten we hier de nodige voorzichtigheid aan de dag te leggen omdat de duurzaamheid van deze percutane prothesen slechts gekend is tot 5 jaar en omdat we weten dat cardiochirurgie voor deze groep patiënten uitstekende resultaten kan voorleggen!
9. Samen met de ontwikkeling van TAVI moeten we echter ook de enorme vooruitgang van de chirurgische technieken niet vergeten: betere stented biologische prothesen, alsook de ontwikkeling van stentless, sutureless en rapid-expandable bioprothesen kunnen bij de meer fragiele populatie een alternatief betekenen voor TAVI, zeker indien gecombineerd met een minder invasieve acces dan de klassieke sternotomie. Maar ook van deze nieuwe kleppen is de langetermijnwerking niet bewezen. Ook al zijn er geen gerandomiseerde studies tussen TAVI en sutureless of rapid-expandable hartkleppen, een vergelijkende studie (matching en propensity score matching studies) pleitte in het voordeel van de chirurgische aanpak: geen verschil in peri-operatoire periode maar betere overleving na 1 en 2 jaar voor chirurgie.7
10. Recente CT-bevindingen van de TAVI en chirurgische bioprothesen tonen dat subklinische trombosevorming vrij frequent aanwezig is en door anticoagulatie vermeden kan worden. Reden tot paniek is er hier zeker niet, gezien het meestal subklinische verloop en de goede respons op anticoagulatie als er een hemodynamische weerslag optreedt. CT moet hier niet vooropgezet worden voor de FU van deze patiënten gezien zijn pure morfologische informatie terwijl echocardiografie meer hemodynamische en klinisch relevante informatie biedt. Nieuwe trials die verschillende antistollings- en antiaggregatiebehandelingen onderzoeken bij deze patiënten zijn zeker vereist. Bij TAVI wordt thans meestal dubbeleplaatjesantiaggregatie voorgesteld na implantatie. Het combineren van anticoagulatie met antiaggregatie bij patiënten met voorkamerfibrillatie en TAVI, leidde niet tot minder beroertes en wel tot meer bloedingen, zodat het systematisch combineren hiervan geen optie is. Zowel ESC- als AHA-richtlijnen geven aan anticoagulatie bij bioprothesen slechts een aanbeveling IIb. Mogelijk zal er in de toekomst voor meer patiënten met bioprothetisch materiaal anticoagulatie voorgeschreven worden en mogelijk zullen we ons ook hier laten leiden door een soort CHADS-Vasc-score.
Besluit
De aangroeiende groep van patiënten met kleplijden en de groep patiënten met IE die een blijvende hoge mortaliteit vertonen vereisen een 'dedicated' aanpak: hartklepkliniek en endocarditisteam.
TAVI blijft aan populariteit winnen. Daar waar er consensus bestaat omtrent het gebruik van TAVI voor de hoogrisicopatiënt met een AS, behoren ook in vele landen de intermediairrisicopatiënten meer en meer tot de doelgroep. Vasculaire toegang, risico op beroerte en paravalvulair lek moeten enerzijds onze blijvende aandacht krijgen en moeten opgelost worden door nieuwe technologische ontwikkelingen.
Anderzijds moeten we er ons van bewust zijn dat er ook nieuwe chirurgische alternatieven bestaan en dat voor TAVI en de nieuwe chirurgische bioprothesen de langetermijnresultaten (10 jaar en meer) nog niet beschikbaar zijn.
Referenties
- Lancellotti, P., Rosenhek, R. Pibarot, P., Iung, B., Otto, C.M., Tornos, P. et al. ESC Working Group on Valvular Heart Disease Position Paper—heart valve clinics: organization, structure, and experiences. Eur Heart J, 2013, 34, 1597-1606.
- Habib, G., Lancellotti, P., Antunes, M., Bongiorni, M., Casalta, J.P., Del Zotti, F. et al. 2015 ESC Guidelines for the management of infective endocarditis. Eur Heart J, 2015, 36, 3075-3123.
- Mack, M.J., Leon, M.B., Smith, C.R., Miller, D.C., Moses, J.R.W., Tuzcu, E. et al. 5-year outcomes of transcatheter aortic valve replacement or surgical aortic valve replacement for high surgical risk patients with aortic stenosis (PARTNER 1): a randomised controlled trial. Lancet, 2015, 385, 2477-2484.
- Biancari, F., Rosato, S., D'Errigo, P., Ranucci, M., Onorati, F. Barbanti, M. et al. Immediate and Intermediate Outcome After Transapical Versus Transfemoral Transcatheter Aortic Valve Replacement. Am J Cardiol, 2016, 117, 245e-251.
- Lange, R., Beckmann, A., Neumann, T., Krane, M., Deutsch, M.A., Landwehr, S. et al. Quality of Life After Transcatheter Aortic Valve Replacement Prospective Data From GARY (German Aortic Valve Registry). J Am Coll Cardiol Intv, 2016, 9, 2541-2554.
- Hørsted Thyregod, H.G, Steinbrüchel, D.A., Ihlemann, N., Nissen, H., Kjeldsen, B.J., Petursson, P. et al. Transcatheter Versus Surgical Aortic Valve Replacement in Patients With Severe Aortic Valve Stenosis. 1-Year Results From the All-Comers NOTION Randomized Clinical Trial. J Am Coll Cardiol, 2015, 65, 2184-2194.
- Wang, N., Tsai, Y.C., Niles, N., Tchantchaleishvili, V., Di Eusanio, M., Yan, T.D., Phan, K. Transcatheter aortic valve implantation (TAVI) versus sutureless aortic valve replacement (SUAVR) for aortic stenosis: a systematic review and meta-analysis of matched studies. J Thorac Dis, 2016, 8 (11), 3283-3293.
- Schirmer, S.H., Mahfoud, F., Fries, P., Scheller, B. Thrombosis of TAVI prosthesis—cause for concern or innocent bystander? A comment and review of currently available data. Clin Res Cardiol, 2016, DOI 10.1007/s00392-016-1061-2.
Niets van de website mag gebruikt worden voor reproductie, aanpassing, verspreiding, verkoop, publicatie of commerciële doeleinden zonder voorafgaande schriftelijke toestemming van de uitgever. Het is ook verboden om deze informatie elektronisch op te slaan of te gebruiken voor onwettige doeleinden.