In de European Heart Journal1 verschenen de '2019 Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk', uitgebracht door een werkgroep van de European Society of Cardiology (ESC) en de European Atheroslerosis Society (EAS). Een 'pocket' versie is eveneens beschikbaar en de aanbevelingen kunnen ook op een app geraadpleegd worden (www.escardio.org/guidelines).
Deze 'update' omvat meerdere aanpassingen vergeleken met de versie die in 2016 verscheen2; ze berusten op recente wetenschappelijke bevindingen omtrent preventie van atherosclerotische cardiovasculaire ziekten (ASCVZ).
Resultaten van observationele studies, van mendeliaanse randomisatiestudies en van gerandomiseerde gecontroleerde klinische trials (RCTs) laten toe te besluiten dat de concentratie van lagedensiteitslipoproteïnepartikels (LDL) in het bloed oorzakelijk verband houdt met het risico op ASCVZ en dat het mogelijk is ASCVZ te voorkomen door het gehalte van LDL-cholesterol (LDL-C) te verlagen. De winst die zo geboekt wordt, situeert zich over de gehele verdeling van het LDL-C-gehalte. Met andere woorden: er blijkt geen grens te bestaan waaronder een verlaging van het LDL-C-gehalte niet verder gepaard gaat met preventie van ASCVZ. Resultaten van RCTs die evenwel slechts enkele jaren bestrijken, laten ook toe te besluiten dat het bereiken van erg lage LDL-C-gehaltes veilig is.
Gelet op deze en andere bevindingen was het nodig de aanbevelingen van 20162 aan te passen om in te gaan op de uitdaging die samengevat kon worden als 'too little, too late'.
1 Preventieve aanpak in functie van het totale cardiovasculaire risico van het individu
De 2019 guidelines bevestigen dat de keuze van de preventiestrategie bij een gegeven persoon afhankelijk moet zijn van het totale risico op de ontwikkeling van ASCVZ. Dit risico is verhoogd of sterk verhoogd bij de meeste patiënten met diabetes mellitus (DM), bij patiënten met een sterk verhoogd LDL-C-gehalte (> 190 mg/dL) of met familiale hypercholesterolemie (FH), met chronische nierinsufficiëntie en zeker bij patiënten met bekende ASCVZ.
Bij asymptomatische, ogenschijnlijk gezonde personen > 40 jaar oud, wordt aanbevolen het totale cardiovasculaire (CV) risico in te schatten aan de hand van bestaande modellen waarbij in Europa het SCORE-model (Systematic COronary Risk Estimation) de voorkeur krijgt.
In de 2019 guidelines zijn nieuwe SCORE- kaarten weergegeven waarbij rekening gehouden werd met het feit dat risicofactoren zoals roken, systolische bloeddruk en totaalcholesterolgehalte niet op alle leeftijden hetzelfde verband vertonen met ASCVZ; in de vorige versies van de SCORE-kaarten was dat wel verondersteld en dat bracht een overschatting van het totale CV-risico op oudere leeftijd met zich mee. De nieuwe kaarten omvatten nu ook gegevens voor de leeftijdsgroep 70+.
Bij het inschatten van het totale CV-risico wordt ook het HDL-cholesterolgehalte (HDL-C) in rekening gebracht en bij sommige subgroepen zal ook gekeken worden naar het niet-HDL-cholesterolgehalte (niet-HDL-C) en/of naar het apo B-gehalte. Dat zal bijvoorbeeld het geval zijn bij personen met hoge triglyceriden (TG), met het metaboolsyndroom, met DM, met een body mass index (BMI) > 30 kg/m2 of met een zeer laag LDL-C.
Er wordt ook aanbevolen het Lp(a)-gehalte bij volwassenen eenmalig te meten om personen op te sporen met sterk verhoogde waarden (> 180 mg/dL), wat gepaard gaat met een verhoogd risico op ASCVZ vergelijkbaar met wat waargenomen wordt bij personen met heterozygote FH.
Om het totale CV-risico van een asymptomatisch persoon in te schatten is het SCORE-model een eerste stap. Er wordt aanbevolen nadien ook rekening te houden met ' risk modifiers' als daar bijvoorbeeld zijn: lage sociale klasse, obesitas, gebrek aan lichaamsbeweging, psychosociale stress, familiale voorgeschiedenis van premature ASCVZ, chronische immuungemedieerde inflammatoire aandoeningen, majeure psychiatrische ziekten …
Bij personen die op basis van het SCORE-model tot de categorie 'matig-verhoogd' totaal CV-risico behoren, wordt ook aanbevolen subklinische atherosclerose op te sporen door bijvoorbeeld met computertomografie (CT) de Coronary Artery Calcium (CAC)-score te berekenen of door significante plaques in de carotiden op te sporen aan de hand van ultrasonografie. Dat laat toe om naargelang het resultaat het totale CV-risico in één of andere richting aan te passen, wat zijn weerslag zal hebben op de keuze van de preventiestrategie. Op basis van dat alles worden categorieën van totaal CV-risico samengesteld, gaande van laag, over matig verhoogd, naar hoog en ten slotte sterk verhoogd risico (tabel 1).

2 Preventiestrategieën en streefwaarden
Afhankelijk van het totale CV-risico en van het onbehandeld LDL-C-gehalte worden strategieën voorgesteld waarbij aanpassingen van leefgewoonten steeds de basis vormen en het toevoegen van vetverlagende medicamenten overwogen kan worden of meteen geïndiceerd is. Dat alles kadert in een brede preventiestrategie waarbij ook aandacht wordt besteed aan andere CV-risicofactoren.
De streefwaarden voor LDL-C, niet-HDL-C en apo B in de verschillende categorieën van totaal CV-risico, voorgesteld in tabel 2, werden aangepast op basis van een kritische synthese van de beschikbare evidentie in studies over de effecten van wijzigingen van het lipideprofiel op het CV-risico.
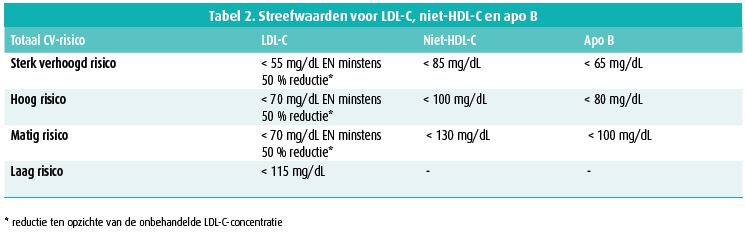
Bij patiënten met ASCVZ die binnen de twee jaar na een eerste CV-voorval (van welke aard ook) hervallen ondanks een behandeling met een maximaal getolereerde statine kan zelfs overwogen worden te streven naar een LDL-C van < 40 mg/dL.
De streefwaarden voor niet-HDL-C en apo B zijn minder sterk onderbouwd omdat ze in de RCTs minder aan bod zijn gekomen. Er worden geen streefwaarden gegeven voor HDL-C en voor TG hoewel een laag HDL-C mee het totale CV-risico bepaalt en een verhoogd TG-gehalte ook gepaard gaat met meer CV-risico. Er is evenwel onzekerheid over het effect van een wijziging ervan op het CV-risico.
3 Hoe bereikt men deze streefwaarden?
Het lipideprofiel van een persoon kan gunstig gewijzigd worden met aanpassingen van het voedingspatroon. Dat wordt in de 2019 guidelines uitvoerig toegelicht en heeft in de eerste plaats te maken met het vermijden van transvetzuren, met het vervangen van verzadigd vet door mono- en polyonverzadigd vet en met een beperking van de inname van voedingcholesterol.
Zo zal een toename van de inname van verzadigd vet met 1 energiepercent gemiddeld een LDL-C-verhoging veroorzaken van 0,8-1,6 mg/dL3. Een toename van de inname van transvetzuren met 2 energieprocent was geassocieerd met een toename van coronaire hartziekten met 25 %4.
Wijzigingen in de inname van voedingsstoffen moeten evenwel vertaald worden in voedingsmiddelen en dat is afhankelijk van de eetcultuur en de eetgewoonten van de gemeenschap; voor België kan daarvoor verwezen worden naar recente aanbevelingen van de Hoge Gezondheidsraad5.
Bij personen met een hoog of sterk verhoogd totaal CV-risico zijn voedingsaanpassingen nodig maar vaak onvoldoende om de streefwaarden te bereiken. In overleg met de patiënt moet dan beslist worden over het al of niet inschakelen van een behandeling met medicamenten. Statines vormen daarbij de eerste keuze; maar de keuze van het type statine en de dosis hangt af van het verschil tussen de uitgangswaarde en de vooropgestelde streefwaarde van LDL-C en dat laatste is afhankelijk van het totale CV-risico. Wil men bijvoorbeeld een reductie van minstens 50 % bereiken en een LDL-C < 70 mg/dL, dan zal de keuze van de medicamenteuze behandeling afhankelijk zijn van wat gemiddeld te verwachten is: 'matige-intensiteit'-statines kunnen gemiddeld gezien een reductie van LDL-C met -30 % bewerkstelligen; met 'hoge-intensiteits'-statines bereikt men -50 %, met de combinatie van hoge-intensiteitsstatines en ezetimibe -65 %, met PCSK9-inhibitoren -60 %, met de combinatie van hoge-intensiteitsstatines en PCSK9-inhibitoren -75 % en met de combinatie van hoge-intensiteitsstatines + ezetimibe + PCSK9-inhibitoren -85 %. Maar dat zijn gemiddelde projecties. Er bestaat een belangrijke interindividuele variatie in de respons van een individu op een gegeven dosis van een gegeven statine. Het is dus essentieel dat 4-6 weken na het opstarten van medicatie een controle gebeurt naar efficaciteit en veiligheid waarbij aanpassingen zonodig doorgevoerd kunnen worden.
Bij het opstarten en opvolgen van een medicamenteuze behandeling zal ook aandacht besteed worden aan de klinische toestand van de patiënt en aan potentiële interacties met andere medicatie. Het is bekend dat statines spierklachten en spierafwijkingen kunnen veroorzaken (statin-associated muscle symptoms of SAMS). De kans daarop is groter wanneer statines samen genomen worden met andere medicatie dat een gelijkaardig metabolisatieproces ondergaat en interageert zoals bepaalde anti-infectieuze medicamenten, en in het CV-domein verapamil, diltiazem, amlodipine en amiodarone, maar ook bijvoorbeeld pompelmoessap. De kans op SAMS is groter bij ouderen, vrouwen, personen met een laag BMI, personen van Aziatische afkomst, comorbiditeit (bv. acute infectie, hypothyreose, chronische nierinsufficiëntie, hiv, diabetes mellitus en vitamine D-deficiëntie), een voorgeschiedenis van spierpijnen, genetische voorbeschiktheid, overmatig alcoholgebruik of zware fysieke inspanningen. Niet alle spierpijnen bij patiënten die statines nemen zijn evenwel statinegeassocieerd. In RCTs is de incidentie van SAMS in de groepen op statines nihil of nauwelijks groter dan in de placebogroepen6; in observationele studies gewaagt men van een frequentie tussen de 10 en 15 %7.
Eerder werden door consensuspanels van de EAS overzichten gemaakt van bijwerkingen van statines en van hoe daarmee om te gaan8, 9. Een algoritme over hoe SAMS te beoordelen en behandelen vindt men in de 2019 guidelines in figuur 6 van het supplement1.
4 Behandeling van dyslipidemieën in diverse subgroepen
4.1 Familiale dyslipidemieën
Er zijn verschillende dyslipidemieën die genetisch bepaald zijn maar bijzondere aandacht wordt gevraagd voor FH, dat gepaard gaat met een sterk verhoogd risico op de ontwikkeling van ASCVZ op jonge leeftijd.
Er wordt aanbevolen daar speciaal aan te denken bij patiënten die vroegtijdig ASCVZ ontwikkelen; screening naar FH is ook aanbevolen bij personen met familiale antecedenten van premature CVZ (voor de leeftijd van 55 jaar voor mannen en < 60 jaar voor vrouwen) en bij personen met een sterk verhoogd LDL-C (> 190 mg/dL). De Dutch lipid clinic network diagnostic criteria (DLCN)1, 10 kunnen daarvoor nuttig gebruikt worden. Eens een geval geïdentificeerd is, is het nodig de familie te screenen (cascadescreening). Een persoon met FH behoort automatisch tot de categorie van hoog of sterk verhoogd totaal CV-risico waarbij overeenkomstig de LDL-C-streefwaarden van tel zijn (tabellen 1 en 2).
4.2 Vrouwen
De behandeling van dyslipidemieën is bij vrouwen niet anders dan bij mannen maar vetverlagende medicamenten, op uitzondering van harsen die nu evenwel minder gebruikt worden, zijn niet aangewezen wanneer een zwangerschap is voorzien, tijdens de zwangerschap en tijdens de borstvoedingsperiode.
4.3 Ouderen
Bij oudere patiënten met ASCVZ worden dyslipidemieën behandeld zoals bij jongere patiënten.
Voor primaire preventie zal de beslissing om statines op te starten afhangen van het totale CV-risico en van comorbiditeiten. Er zal bijzondere aandacht besteed worden aan de nierfunctie en aan mogelijke interacties met andere medicatie. Daarom zal men de streefwaarde van LDL-C meer stapsgewijs proberen te bereiken.
4.4 Diabetes mellitus
De behandeling van dyslipidemieën bij patiënten met DM is afhankelijk van de categorie van totaal CV-risico waartoe ze behoren (tabel 1). De grote meerderheid heeft een hoog of sterk verhoogd totaal CV-risico zodat naast voedingsaanpassingen ook medicatie nodig is om de LDL-C-streefwaarden te bereiken. Statines zijn de eerste keuze en naargelang het resultaat kunnen die opgedreven worden tot de maximaal getolereerde dosis, al of niet in combinatie met ezetimibe.
Guidelines ter preventie van ASCVZ bij patiënten met DM zijn recent uitgebracht door de ESC11.
4.5 Cardiovasculaire comorbiditeit
- Bij patiënten die een acuut coronair syndroom doormaken en bij wie geen contra-indicatie voor statines bestaat, is het aangewezen meteen te starten met een hoge-intensiteitsstatine ongeacht het LDL-C-gehalte waarvan men start. Na 4-6 weken beoordeelt men het resultaat; werd ≥ 50%-reductie en LDL-C < 55 mg/dL bereikt? Wordt de medicatie goed verdragen? Zo nodig wordt een combinatietherapie overwogen.
- Bij patiënten bij wie de streefwaarden niet bereikt worden met een maximaal getolereerde dosis van een hoge-intensiteitsstatine in combinatie met ezetimibe kan overwogen worden een PCSK9-inhibitor toe te voegen.
- Bij patiënten bij wie een PTCA is voorzien, is het te overwegen ze voorafgaand 'op te laden' met een hoge-intensiteitsstatine.
- Hartfalen en een aortaklepstenose zijn op zich geen indicaties voor een behandeling met vetverlagende medicamenten; statines kunnen nodig zijn als daar andere indicaties voor bestaan.
- Patiënten die een ischemische beroerte of een TIA hebben doorgemaakt of bij wie perifeer arterieel lijden werd vastgesteld hebben een sterk verhoogd totaal CV-risico waarbij gestreefd zal worden naar een LDL-C-reductie van minstens 50 % en een LDL-C-gehalte < 55 mg/dL.
4.6 Andere comorbiditeit
- Patiënten met chronische nierinsufficiëntie behoren tot de 'hoog of sterk verhoogd'-risicocategorieën van totaal CV-risico. Om de LDL-C-streefwaarden te bereiken zijn vaak statines of de combinatie van statine met ezetimibe nodig bij patiënten die niet dialyseafhankelijk zijn. Patiënten die reeds behandeld werden met een statine of een combinatie vooraleer dialyse opgestart werd, kunnen deze behandeling aanhouden, zeker wanneer ze ook een ASCVZ vertonen. Bij patiënten zonder ASCVZ die dialyseafhankelijk zijn, worden geen statines opgestart.
- Patiënten die een transplantatie hebben ondergaan, kunnen voordeel halen uit een behandeling met statines. Men start in een lage dosis en schenkt bijzondere aandacht aan mogelijke interacties met andere medicatie in het bijzonder met ciclosporine.
- Patiënten met ernstige psychiatrische ziekten hebben een verhoogd risico op ASCVZ. De behandeling van dyslipidemieën is bij hen niet anders dan bij andere personen; meer aandacht is nodig voor een goede compliance met medicatie en voor aanpassingen van leefgewoonten.
- Patiënten met chronische immuungemedieerde inflammatoire aandoeningen hebben een verhoogd risico op ASCVZ. Deze aandoeningen zijn op zich echter geen indicatie voor vetverlagende medicaties.
Tot slot
Deze nieuwe guidelines bevatten ook hoofdstukken over inflammatie, over de kosteneffectiviteit van een behandeling van dyslipidemieën, aanbevelingen over monitoring van lipiden en enzymes, strategieën om leefgewoonten aan te passen en de compliance met medicatie te optimaliseren en over wat nog ontbreekt aan kennis over het onderwerp.
In een elektronisch supplement wordt nog aanvullend informatie verstrekt; de aanbevelingen berusten op 608 referenties.
Ik wens u veel leesgenot maar vraag vooral uw aandacht voor de implementatie van deze aanbevelingen in de klinische praktijk.
Referenties
- Mach, F., Baigent, C., Catapano, A. et al. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J, 2019, doi: 10.1093/eurheartj/ehz455.
- Catapano, A.L., Graham, I., De Backer, G. et al. 2016 ESC/EAS Guidelines for the management of dyslipidaemias. Eur Heart J, 2016, 37, 2999-3058.
- Mensink, R.P., Zock, P.L., Kester, A.D., Katan, M.B. Effects of dietary fatty acids and carbohydrates on the ratio of serum total to HDL cholesterol and on serum lipids and apolipoproteins: a meta-analysis of 60 controlled trials. Am J Clin Nutr, 2003, 77, 1146- 1155.
- Mozaffarian, D., Aro, A., Willett, W.C. Health effects of trans-fatty acids: experimental and observational evidence. Eur J Clin Nutr, 2009, 63, S5-S21.
- HGR-Hoge Gezondheidsraad. Voedingsaanbevelingen voor de Belgische volwassen bevolking met een focus op voedingsmiddelen-2019. Advies van de Hoge Gezondheidsraad nr 9284.
- Finegold, J.A., Manisty, C.H., Goldacre, B. et al. What proportion of symptomatic side effects in patients taking statins are genuinely caused by the drug? Systematic review of randomized placebo-controlled trials to aid individual patient choice. Eur J Prev Cardiol, 2014, 21, 464- 474.
- Bruckert, E., Hayem, G., Dejager, S. et al. Mild to moderate muscular symptoms with high-dosage statin therapy in hyperlipidemic patients-the PRIMO study. Cardiovasc Drugs Ther, 2005, 19, 403-414.
- Stroes, E.S., Thompson, P.D., Corsini, A. et al. European Atherosclerosis Society Consensus Panel. Statin-associated muscle symptoms: impact on statin therapy-European Atherosclerosis Society Consensus Panel Statement on Assessment, Aetiology and Management. Eur Heart J, 2015, 36, 1012-1022.
- Mach, F., Ray, K.K., Wiklund, O. et al. European Atherosclerosis Society Consensus Panel. Adverse effects of statin therapy: perception vs. the evidence - focus on glucose homeostasis, cognitive, renal and hepatic function, haemorrhagic stroke and cataract. Eur Heart J, 2018, 39, 2526-2539.
- Defesche, J.C., Lansberg, P.J., Umans- Eckenhausen, M.A., Kastelein, J.J. Advanced method for the identification of patients with inherited hypercholesterolemia. Semin Vasc Med, 2004, 4, 59-65.
- Cosentino, F., Grant, P.J., Aboyans, V. et al. 2019 ESC Guidelines on diabetes, pre-diabetes and cardiovascular diseases. Eur Heart J, 2019; doi: 10.1093/eurheartj/ehz486.
Niets van de website mag gebruikt worden voor reproductie, aanpassing, verspreiding, verkoop, publicatie of commerciële doeleinden zonder voorafgaande schriftelijke toestemming van de uitgever. Het is ook verboden om deze informatie elektronisch op te slaan of te gebruiken voor onwettige doeleinden.