Inleiding
De eerste mineralocorticoïdreceptor (MR) -antagonist (MRA) spironolacton werd beschikbaar op de markt in 1959. Pas in 2002 werd eplerenon door de FDA goedgekeurd voor gebruik in arteriële hypertensie, en nog later voor de behandeling van hartfalen. Beide molecules zijn zogeheten steroïdale MRA's met een breed spectrum van toepassingsmogelijkheden (hartfalen, oedeem, cirrose, hyperaldosteronisme, arteriële hypertensie). De bedoeling van dit artikel is om wat dieper in te gaan op de rol van MRA's en in het bijzonder van eplerenon in ons therapeutisch arsenaal voor de hartfalenpatiënt.
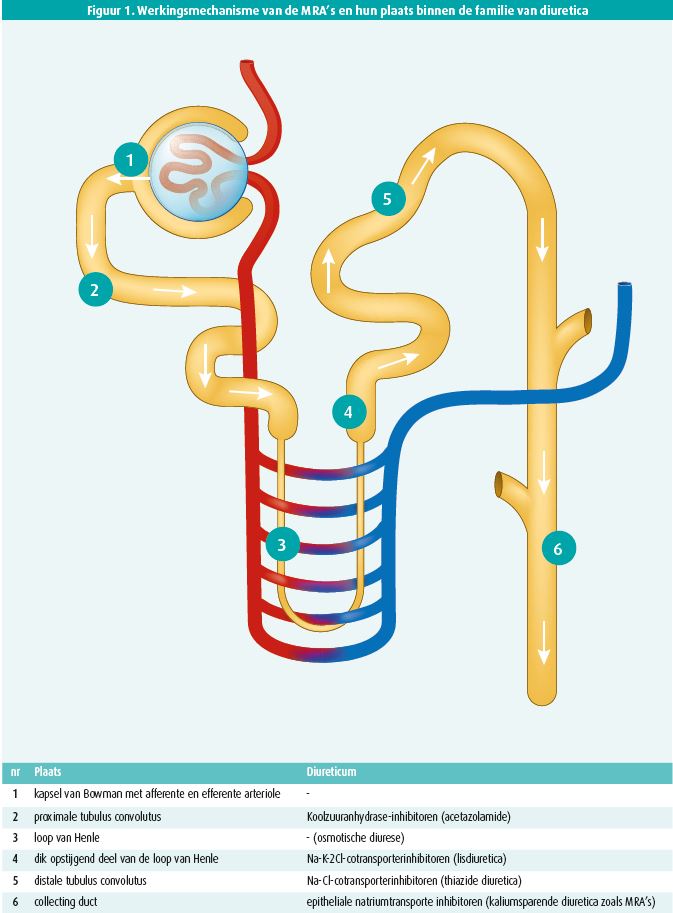
MRA's werden aanvankelijk ontwikkeld vanwege de centrale rol van aldosteron in de bloeddruk- en volumehomeostase. Aldosteron kan beschouwd worden als dé regulator van de natriumreabsorptie en de kaliumexcretie t.h.v. de nier (figuur 1). Nadien werd ook duidelijk dat hypersecretie van aldosteron niet alleen nefast is vanwege de water- en zoutretinerende effecten maar ook door nadelige effecten op de hersenen, de nieren, het hart en bloedvaten ten dele op basis van een pro-inflammatoire en fibroserende werking.
In een hele reeks trials werd de werkzaamheid aangetoond van angiotensineconverterendenzymremmers (ACEI's) en angiotensinereceptorblokkers (ARB's) in de behandeling van hypertensie en hartfalen met gereduceerde linkerkamerejectiefractie (HFrEF). Uit de literatuur blijkt evenwel dat na 12 tot 42 maanden behandeling met ACEI's of ARB's bij 40 tot 53 % van de proefpersonen de aldosteronconcentratie opnieuw oploopt tot boven de uitgangswaarde, de zogenaamde 'aldosterone breakthrough'1. Dat zou kunnen verklaren waarom MRA's een grote invloed hebben op de overleving bij patiënten met HFrEF die al voorbehandeld zijn met ACEI's of ARB's.
MRA's in HFrEF
Dankzij enkele 'landmark trials' hebben MRA's, zowel spironolacton als eplerenon, ondertussen hun meerwaarde bewezen in de behandeling van HFrEF met NYHA-klasse III-IV (RALES-trial2) en NYHA-klasse II (EMPHASIS-trial3). Ook in de post-myocardinfarctsetting (wanneer de LVEF lager is dan 40 % en er klinische tekens zijn van hartfalen) (EPHESUS-trial4) werden de voordelen van MRA's aangetoond. Toch zijn de hartfalenrichtlijnen van de ESC5 wat dubbelzinnig over de plaats van MRA's in de behandelingsboom van HFrEF: voor, samen met of na de implementatie van ACEI's (of ARB's) en bètablokkers (BB)? Enerzijds lezen we 'Voeg een MRA (spironolacton of eplerenon) toe indien er symptomen blijven bestaan ná correctie van volumeoverbelasting én na optitreren van ACEI's of ARB's en BB's'; m.a.w. MRA's zouden slechts aangewend moeten worden wanneer na volumecorrectie en na optitreren van ACEI's (of ARB's) en BB's, de HfrEF-patiënt symptomatisch blijft. Deze hiërarchie vloeit voort uit de historiek van het gerandomiseerde onderzoek waarop de richtlijnen zijn gebaseerd. Anderzijds lezen we op de webpagina met praktische tips over het gebruik van diuretica6 een veel meer logische aanpak: 'Wanneer men diuretica gebruikt, moet dat altijd in combinatie zijn met een ACEI (of een ARB), een BB en een MRA bij patiënten met HFrEF (tenzij een van deze medicatieklasses niet wordt getolereerd of gecontra-indiceerd is) totdat de tekens van congestie zijn verdwenen'. Het is immers zeer moeilijk om bij een NYHA III-IV-patiënt met congestieverschijnselen hypokaliëmie door gebruik van diuretica te vermijden zonder gebruik van MRA's. Goed afgewogen lis- of thiazidediuretica enerzijds en MRA's anderzijds houden elkaar op dit vlak vrij goed in evenwicht en zijn daarom niet alleen de logica zelve, maar zelfs een essentieel hulpmiddel om de congestie onder controle te brengen - en te houden.
Congestieteken: zoeken, vinden, behandelen!
Het onder controle brengen van congestie aan de hand van klachten en fysisch onderzoek blijft nog steeds onze eerste doelstelling bij de HfrEF-patiënt, niet alleen voor zijn/haar comfort maar ook om nadien de titrage van de BB's enz. succesvol te kunnen doorvoeren én uit prognostisch oogpunt. Inderdaad is het opsporen van fysische tekens van congestie (derde toon, verhoogde CVD, oedeem en longcrepitaties) ook vanuit prognostisch oogpunt zeer belangrijk7. Wij hebben om al deze redenen al vroeger gepleit voor meer 'upfront' gebruik van MRA bij HfrEF8, i.e. van bij de start van de behandeling. Starten van MRA's later in het herstelproces, na het optitreren van BB's, is bovendien niet helemaal consequent met de literatuur, aangezien in de RALES-trial slechts 10 % van de studiepopulatie met een BB behandeld werd. In de EMPHASIS-trial (12 jaar later) was dat inmiddels opgeklommen tot 86 %. Toch had ook daar de MRA nog een significant additioneel gunstig effect.
RISICO's van het gebruik van MRA's
De voornaamste risico's aan het gebruik van MRA's zijn hypotensie, afname van de nierfunctie en hyperkaliëmie. Seksuele disfunctie zoals impotentie bij de man en menometrorragie bij de vrouw en gynaecomastie zijn minder vitaal, behalve dan wanneer deze neveneffecten ertoe leiden dat de therapie wordt onderbroken. Eplerenon is bij gynaecomastie een volwaardig alternatief voor spironolacton.
Enkele jaren na de publicatie van RALES verscheen een alarmerende studie waarin werd gewezen op het risico van hyperkaliëmie en als gevolg daarvan ziekenhuisopname en zelfs overlijden wanneer de selectie en opvolging van de patiënten te wensen overlaat9. Waarom er zulke grote verschillen zijn in het voorkomen van hyperkaliëmie tussen RALES en 'real life ' heeft velerlei oorzaken10. Naast het gebruik bij oudere patiënten, met een hogere graad van nierinsufficiëntie dan in de studiepopulatie van RALES, en de toename in het gebruik van BB's, is vermoedelijk de grootste reden het niet goed opvolgen van de patiënt. Het is immers te kort door de bocht te stellen dat voor MRA's gewoon de 'targetdosis ' ingesteld moet worden of nagestreefd, zoals voor andere hartfalenmedicatie het geval is. Integendeel, de dosis van een MRA moet zeer nauwgezet worden getitreerd en aangepast aan iedere individuele patiënt en diens evolutie, en vergt dus regelmatige opvolging van klinische parameters én laboratoriumgegevens. Het speelveld van de arts wordt daarbij afgebakend door klinische parameters (klachten, tekens van congestie of de volemie, tensies) enerzijds en kaliëmie, natriëmie en nierfunctie anderzijds. Bij gebruik van vooraf vastgestelde en vaste dosissen is immers het risico op hyperkaliëmie onaanvaardbaar hoog zoals werd vastgesteld in de RALES Pilot-studie (een 'dose finding' studie), waarin verschillende vaste dosissen spironolacton werden vergeleken11. Het risico op belangrijke hyperkaliëmie (> 5,5 mEq/L) nam toe van 5 % bij een dagdosis van 12,5 mg tot 25 % bij een dagdosis van 75 mg. De dosis moet dus zo nodig regelmatig bijgestuurd worden in functie van de evolutie van elke individuele patiënt. Er rust dus een grote verantwoordelijkheid op de schouders van de verantwoordelijke arts, nl. ervoor instaan dat deze parameters betrouwbaar worden opgevolgd en geïntegreerd in het beleid. Enerzijds stelt zich het probleem van de kaliëmie: het is geen geheim dat de kaliëmiedosages door hemolyse in de huisartsenpraktijk vaak onbetrouwbaar zijnvanwege logistieke beperkingen. Bij de minste twijfel moet een controle worden uitgevoerd met afname in het ziekenhuislaboratorium. Anderzijds is er de problematiek van de onvoldoende aandacht (en/of expertise) zowel bij huisartsen, als bij cardiologen voor het fysisch onderzoek en het beoordelen van de volemie aan de hand van congestietekens zoals oedeem, verhoogde CVD, crepitaties … Het klinisch onderzoek is onterecht verdrongen door technisch onderzoek (echo-doppler) en laboparameters zoals BNP/NT-pro-BNP, die als een aanvulling en niet als een surrogaat beschouwd moeten worden. Zowel een te hoge dosering van de MRA als het lichtzinnig staken of verlagen van de dosis kunnen ernstige gevolgen hebben. Het is twijfelachtig dat de behandeling enkel aan de huisarts overgelaten kan worden10. Meer en meer wordt duidelijk dat hartfalenbeleid door - of minstens in intensieve collaboratie met - hartfalenspecialisten gevoerd moet worden, net zoals de kankertherapie door de medische oncologen wordt gecoördineerd en de behandeling van chronische nierinsufficiëntie door de nefroloog. Het staat echter buiten kijf dat samenwerking, gedeelde verantwoordelijkheid en goede communicatie tussen zorgverleners de hartfalenpatiënt zeker ten goede komen.
MRA's in HFpEF
In de TOPCAT-trial werd de invloed van spironolacton op de prognose van patiënten met hartfalen met bewaarde LVEF (HFpEF) onderzocht. De trial was neutraal12 voor het primair eindpunt (samengesteld eindpunt van cardiovasculaire sterfte, plotse dood en opname voor hartfalen). Enkel het aantal hospitalisaties voor hartfalen was in de met spironolacton behandelde groep significant lager dan in de placebogroep. Het primair eindpunt was niet significant, vermoedelijk door inclusie van een te groot aantal patiënten (uit Oost-Europa) met een dubieuze diagnose van hartfalen. In een subanalyse van de patiënten uit Noord- en Zuid-Amerika, was het primair eindpunt wél significant beter bij de met spironolacton behandelde groep. Los daarvan bestaat er bij HFpEF ook na de TOPCAT-trial, hoe dan ook een indicatie voor MRA's. Bij HFpEF is het corrigeren van congestie even zo goed een hoofdbekommernis omdat congestie in belangrijke mate de levenskwaliteit en de morbiditeit van de HfpE-patiënt bepaalt. Levenskwaliteit is voor veel patiënten met HFpEF vaak predominant, meer dan de prognose. Deze mensen worden - vaker dan HfrEF-patiënten - met tal van comorbiditeiten geconfronteerd die evenzeer de levensverwachting bepalen. Correcte dosering van diuretica is daarbij de hoeksteen en ook hier houden op vlak van kaliëmie lis- en thiazidediuretica enerzijds en MRA's anderzijds mekaar in evenwicht13. Uit een recente meta-analyse van RALES, EMPHASIS en TOPCAT bleek overigens dat in de oudere populatie (> 75 jaar) het gebruik van MRA de morbiditeit en mortaliteit significant deed afnemen over het gehele spectrum van ejectiefractie14, dus ook bij de HfpEF-patiënt, hoewel het effect daar minder groot was dan bij HFrEF. Nog belangrijker zijn de resultaten van een recent gepubliceerde subanalyse van de TOPCAT-trial; het gaat hier over een omvangrijke groep patiënten, van wie gegevens betreffende klinisch onderzoek (CVD, oedeem en longcrepitaties) bekend waren bij inclusie en opvolging15. Uit dat onderzoek bleek dat het klinisch onderzoek bij de HfpEF-patiënt enorm belangrijk is. Hoe meer tekens van congestie bij fysisch onderzoek, hoe slechter de prognose. Voor ieder extra teken van congestie (verhoogde CVD, longcrepitaties of oedeem) nam het risico op cardiovasculaire mortaliteit, opname voor hartfalen en totale mortaliteit met niet minder dan 30 tot 80 % toe! Belangrijker dan de congestie bij de inclusie bleek de opvolging en correctie van de congestie in de loop van de studie. Het belang van het klinisch onderzoek in deze populatie contrasteert overigens met het feit dat BNP/NT-pro- BNP bij aanvang geen invloed hadden op de prognose in deze HfpEF-populatie. Spironolacton verbeterde de levenskwaliteit én de prognose significant. Deze studie zet het fysisch onderzoek bij HFpEF weer helemaal in het middelpunt van het HF-beleid: tekens van congestie correleren niet alleen met de levenskwaliteit maar hebben ook een sterke invloed op de prognose. Spironolacton biedt daarbij een significante meerwaarde. Dat werpt ook een totaal ander licht op de na te streven dosering van MRA's. Als tekens van congestie prognostisch belangrijk zijn en het wegwerken ervan een belangrijke, zo niet de belangrijkste maatregel, in deze populatie met weinig of geen evidencebased alternatief, dan moeten we niet naar vooraf vastgelegde targetdosissen streven van MRA's, maar naar de minimaal effectieve dosis die ons toelaat om in koor met andere factoren die de volumestatus bepalen (zout- en vochtbeperking, lis- en thiazidediuretica, ziektemodulerende medicatie) de congestie te elimineren en dat binnen de grenzen gesteld door nierfunctie en elektrolyten.
MRA's in hypertensie
Er werden twee Cochrane-reviews gewijd aan MRA's voor hypertensie: in 2010 voor spironolacton16 en in 2017 voor eplerenon17. Voor spironolacton bleek de conclusie merkwaardig genoeg dat er onvoldoende bewijs was dat spironolacton in de eerstelijnsbehandeling van hypertensie klinisch relevante outcomeparameters in gunstige zin beïnvloedt. Misschien houdt dat verband met het feit dat het hier oude literatuur betreft, voor de periode van de algemene verspreiding van RCT's. Ook voor eplerenon blijkt er geen bewijs te zijn voor een impact op klinische belangrijke outcomevariabelen in de eerstelijnsbehandeling van hypertensie. MRA's zijn wel de meest efficiënte antihypertensiva bij primair aldosteronisme18. Spironolacton en eplerenon bleken evenwaardig te zijn voor de behandeling van primair hyperaldosteronisme19. MRA's hebben vooral hun plaats verworven in de behandeling van therapieresistente hypertensie en worden in de richtlijnen van de ESC voor hypertensie in dat verband heel duidelijk aanbevolen20 op basis van twee RCT's21, 22.
Werkingsmechanisme en verschillen tussen MRA: spironolacton en eplerenon
Spironolacton antagoneert niet alleen de MR met een zeer grote affiniteit, maar het is relatief weinig specifiek voor de MR en blokkeert ook de progesteronreceptor (PR) en de androgeenreceptor (AR) waardoor het bij de vrouw menstruatieproblemen en bij de man gynaecomastie kan veroorzaken. Eplerenon daarentegen heeft een zeer grote specificiteit maar een veel lagere affiniteit voor de MR dan spironolacton. Het heeft een veel kortere werkingsduur waardoor het in principe tweemaal daags gedoseerd zou moeten worden, hoewel dat in de grote gerandomiseerde trials niet het geval was. Het voordeel van eplerenon is dat het de AR niet antagoneert en dat daardoor veel minder vaak gynaecomastie optreedt. Beide hebben wel een stel andere bijwerkingen gemeen: hyperkaliëmie, nierinsufficiëntie, hypotensie ... Klassieke contra-indicaties (exclusiecriteria in de RCT's) zijn dan ook nierinsufficiëntie met een GFR < 30 ml/min/m2 of een creatinine van > 2,5 mg/dL, en/ of hyperkaliëmie in de voorgeschiedenis. Deze contra-indicaties zijn relatief, ook is het gebruik mogelijk mits aangepaste dosering en zeer strikte opvolging van de laboratoriumparameters.
Als beide geneesmiddelen op gelijkaardige manier de MR antagoneren, zijn ze dan inwisselbaar? M.a.w. kan men spironolacton bij patiënten met gynaecomastie gewoon vervangen door eplerenon? Beide MRA zijn nooit op grote schaal direct met mekaar vergeleken, noch bij hypertensie, noch bij hartfalen. Alles wijst er wel op dat - afgezien van de bijwerkingen door het al dan niet antagoneren van de AR en de PR - het effect op outcomeparameters bij HfrEF-patiënten vergelijkbaar is. In een meta-analyse van 14 RCT's op een totaal van 12 213 HfrEF-patiënten bleken zowel spironolacton als eplerenon vergelijkbare effecten te hebben op de totale mortaliteit en de cardiovasculaire mortaliteit en de hospitalisatie voor HF te verminderen waarbij er een trend was in het voordeel van spironolacton maar dat was niet significant23. Ook op vlak van bijwerkingen zoals nierinsufficiëntie en hyperkaliëmie waren de producten vergelijkbaar, enkel het voorkomen van gynaecomastie was beduidend minder bij eplerenon.
MRA's in België: een staaltje Kafka
Daarnaast speelt ook de kostprijs en de door de wetgever al dan niet toegestane indicatie en modaliteiten van terugbetaling een rol. Inderdaad is spironolacton heel goedkoop in België (0,14 EUR per tablet van 25 mg). Eplerenon is ongeveer vijfmaal duurder (0,69 EUR per tablet van 25 mg). Bovendien wordt het vlotte gebruik van eplerenon bemoeilijkt door de terugbetaling aan strikte voorwaarden te koppelen en in de dagelijkse praktijk is dat niet zo eenvoudig (BCFI):
- Enkel voor 'mannelijke patiënten': hoewel in EPHESUS 30 % en in EMPHASIS 22 % vrouwen werden geïncludeerd en er geen enkele reden was om aan te nemen dat eplerenon minder werkzaam zou zijn bij vrouwen in vergelijking met mannen;
- Die 'voorafgaandelijk behandeld werden met spironolacton en onder deze therapie als onaanvaardbare nevenwerking een belangrijke gynaecomastie ontwikkeld hebben';
- En lijden aan 'hartfalen met een LVEF < 30 % ' of 'hartfalen met een LVEF < 40 % en een recent myocardinfarct';
- 'Op basis van een omstandig verslag'.
Uit de wetenschappelijke gegevens die aan de basis liggen van het gebruik van MRA's, of het nu spironolacton betreft of eplerenon zoals hoger beschreven, blijkt nochtans dat de ESC in haar richtlijnen gewoon MRA's vermeldt en geen onderscheid maakt tussen beide voor wat de indicatiestelling betreft. Overigens wordt HFrEF gedefinieerd als hartfalen bij een LVEF van minder dan 40 % (en dus niet < 30 %). Uit gerandomiseerd onderzoek blijkt zonder meer dat MRA's bij HFrEF een onmisbare schakel zijn in het therapeutisch arsenaal omdat zij een belangrijk prognostisch impact hebben op patiënten in NYHA-klasse II, III en IV met of zonder recent infarct.
Uit subanalyses van de TOPCAT-trial blijkt ook dat de patiënten die werkelijk HFpEF hebben het ook prognostisch beter doen wanneer ze met spironolacton worden behandeld12, 24, en dat de prognose significant beter is bij HfpEF-patiënten, wanneer MRA oordeelkundig worden aangewend om de congestie te bestrijden15. MRA's zijn ook opgenomen in alle internationale richtlijnen voor de behandeling van therapieresistente hypertensie waarbij de LVEF niets ter zake doet.
We moeten dus concluderen dat de verschillende terugbetalingsmodaliteiten in ons land voor de twee gecommercialiseerde MRA's arbitrair zijn en niet wetenschappelijk onderbouwd. Vergeleken met spironolacton lijkt eplerenon inderdaad veel duurder. Spironolacton heeft slechts weinig commercieel belang en wegens de vrijemarktwerking verschuiven de voorraden naar de commercieel interessantste locatie in die mate dat stockbreuken vooral in kleine landen met lage verkoopsprijs legio zijn. Voor een product waarvan de dosering zeer nauwgezet aangepast moet worden aan de individuele nood van de patiënt houdt dit grote risico's in. Is eplerenon te duur? Is de restrictie die de overheid oplegt in het gebruik van eplerenon te verantwoorden uit economische overwegingen? Twee studies hebben de kosteneffectiviteit van eplerenon bij NYHA II HfrEF-patiënten (in het VK25 en in Australië26) aangetoond aan een kostprijs per tablet die vele malen hoger is dan de verkoopsprijs vandaag in ons land. Het is dus moeilijk te verantwoorden dat er restricties blijven bestaan op het gebruik van eplerenon dat een vergelijkbaar toepassingsgebied heeft als spironolacton.
Besluit
Er zijn in ons land twee MRA's beschikbaar: spironolacton en eplerenon. MRA's zijn een hoeksteen voor correctie van congestie zowel bij HFrEF als bij HFpEF en in de behandeling van primair aldosteronisme en therapieresistente hypertensie. MRA's hebben bij HFrEF een zeer grote impact op de prognose. Wij pleiten voor een vroege en systematische implementatie in een gewogen combinatie met lis- of thiazidediuretica van bij de start van de behandeling van HFrEF, voor de optitrage van de BB's. Hoewel bij HFpEF de prognostische meerwaarde om tal van redenen minder sterk is, wijst recent onderzoek er toch op dat MRA ook een meerwaarde bieden bij de controle van de congestieveschijnselen bij HfpEF-patiënten en daardoor onrechtstreeks ook een belangrijk impact hebben op de prognose. De opvolging van de met MRA behandelde HfrEF- en HfpEF-patiënten vergt een grote expertise en discipline van arts en patiënt: betrouwbaar opvolgen van klinische parameters (zoals congestie) en laboratoriumparameters. Spironolacton en eplerenon hebben een vergelijkbaar toepassingsgebied en de restrictie in de terugbetaling van eplerenon zoals we die vandaag in ons land aantreffen is moeilijk op wetenschappelijk verantwoorde basis te rechtvaardigen.
Referenties
- Bomback, A.S., Klemmer, P.J. The incidence and implications of aldosterone breakthrough. Nat Clin Pract Nephrol, 2007, 3 (9), 486-492.
- Pitt, B., Zannad, F., Remme, W.J., et al. The effect of spironolactone on morbidity and mortality in patients with severe heart failure. Randomized Aldactone Evaluation Study Investigators. N Engl J Med, 1999, 341 (10), 709-717.
- Zannad, F., McMurray, J.J., Krum, H., et al. Eplerenone in patients with systolic heart failure and mild symptoms. N Engl J Med, 2011, 364 (1), 11-21.
- Pitt, B., Remme, W., Zannad, F., et al. Eplerenone, a selective aldosterone blocker, in patients with left ventricular dysfunction after myocardial infarction. N Engl J Med, 2003, 348 (14), 1309-1321.
- Ponikowski, P., Voors, A.A., Anker, S.D., et al. 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure: The Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC) Developed with the special contribution of the Heart Failure Association (HFA) of the ESC. Eur Heart J, 2016, 37 (27), 2129-2200.
- Ponikowski, P., Voors, A.A., Anker, S.D., et al. 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure: The Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC) Developed with the special contribution of the Heart Failure Association (HFA) of the ESC. '2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure.' Web. 14 Jan. 2020. https://www.escardio.org/static_file/Escardio/ Guidelines/ehw128_Addenda.pdf.
- Wong, M., Staszewsky, L., Carretta, E., et al. Signs and symptoms in chronic heart failure: relevance of clinical trial results to point of care-data from Val-HeFT. Eur J Heart Fail, 2006, 8 (5), 502-508.
- Heggermont, W.A., Goethals, M., Dierckx, R., Verstreken, S., Bartunek, J., Vanderheyden, M. Should MRAs be at the front row in heart failure? A plea for the early use of mineralocorticoid receptor antagonists in medical therapy for heart failure based on clinical experience. Heart Fail Rev, 2016, 21 (6), 699-701.
- Juurlink, D.N., Mamdani, M.M., Lee, D.S., et al. Rates of hyperkalemia after publication of the Randomized Aldactone Evaluation Study. N Engl J Med, 2004, 351 (6), 543-551.
- McMurray, J.J., O 'Meara, E. Treatment of heart failure with spironolactone--trial and tribulations. N Engl J Med, 2004, 351 (6), 526-528.
- Effectiveness of spironolactone added to an angiotensin-converting enzyme inhibitor and a loop diuretic for severe chronic congestive heart failure (the Randomized Aldactone Evaluation Study [RALES]). Am J Cardiol, 1996, 78 (8), 902-907.
- Pitt, B., Pfeffer, M.A., Assmann, S.F., et al. Spironolactone for heart failure with preserved ejection fraction. N Engl J Med, 2014, 370 (15), 1383-1392.
- Yancy, C.W., Jessup, M., Bozkurt, B., et al. 2017 ACC/AHA/HFSA Focused Update of the 2013 ACCF/AHA Guideline for the Management of Heart Failure: A Report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines and the Heart Failure Society of America. Circulation, 2017, 136 (6), e137-e161.
- Ferreira, J.P., Rossello, X., Eschalier, R., et al. MRAs in Elderly HF Patients: Individual Patient-Data Meta-Analysis of RALES, EMPAHSIS-HF, and TOPCAT. JACC Heart Fail, 2019, 7 (12), 1012-1021.
- Selvaraj, S., Claggett, B., Shah, S.J., et al. Utility of the Cardiovascular Physical Examination and Impact of Spironolactone in Heart Failure With Preserved Ejection Fraction. Circ Heart Fail, 2019, 12 (7), e006125.
- Batterink, J., Stabler, S.N., Tejani, A.M., Fowkes, C.T. Spironolactone for hypertension. The Cochrane database of systematic reviews, 2010, 8, CD008169.
- Tam, T.S., Wu, M.H., Masson SC, et al. Eplerenone for hypertension. The Cochrane database of systematic reviews, 2017, 2, CD008996.
- Colussi, G., Catena, C., Sechi, L.A. Spironolactone, eplerenone and the new aldosterone blockers in endocrine and primary hypertension. J Hypertens, 2013, 31 (1), 3-15.
- Karashima, S., Yoneda, T., Kometani, M., et al. Comparison of eplerenone and spironolactone for the treatment of primary aldosteronism. Hypertens Res, 2016, 39 (3), 133-137.
- Williams, B., Mancia, G., Spiering, W., et al. 2018 ESC/ESH Guidelines for the management of arterial hypertension: The Task Force for the management of arterial hypertension of the European Society of Cardiology and the European Society of Hypertension: The Task Force for the management of arterial hypertension of the European Society of Cardiology and the European Society of Hypertension. J Hypertens, 2018, 36 (10), 1953-2041.
- Oxlund, C.S., Henriksen, J.E., Tarnow, L., Schousboe, K., Gram, J., Jacobsen, I.A. Low dose spironolactone reduces blood pressure in patients with resistant hypertension and type 2 diabetes mellitus: a double blind randomized clinical trial. J Hypertens, 2013, 31 (10), 2094-2102.
- Williams, B., MacDonald, T.M., Morant, S.V., et al. Endocrine and haemodynamic changes in resistant hypertension, and blood pressure responses to spironolactone or amiloride: the PATHWAY-2 mechanisms substudies. Lancet Diabetes Endocrinol, 2018, 6 (6), 464-475.
- Frankenstein, L., Seide, S., Tager, T., et al. Relative Efficacy of Spironolactone, Eplerenone, and cAnRenone in patients with Chronic Heart failure (RESEARCH): a systematic review and network meta-analysis of randomized controlled trials. Heart Fail Rev, 2019, [Epub ahead of print].
- McMurray, J.J., O 'Connor, C. Lessons from the TOPCAT trial. N Engl J Med, 2014, 370 (15), 1453-1454.
- Lee, D., Wilson, K., Akehurst, R., et al. Cost-effectiveness of eplerenone in patients with systolic heart failure and mild symptoms. Heart, 2014, 100 (21), 1681-1687.
- Ademi, Z., Pasupathi, K., Krum, H., Liew, D. Cost effectiveness of eplerenone in patients with chronic heart failure. Am J Cardiovasc Drugs, 2014, 14 (3), 209-216.
Niets van de website mag gebruikt worden voor reproductie, aanpassing, verspreiding, verkoop, publicatie of commerciële doeleinden zonder voorafgaande schriftelijke toestemming van de uitgever. Het is ook verboden om deze informatie elektronisch op te slaan of te gebruiken voor onwettige doeleinden.