Symposiumverslag van het HFA
Het jaarlijkse Europese hartfalencongres van de ESC vond dit jaar plaats in Praag en was een succes. Internationale experten bespraken verschillende interessante topics en er was veel interactie met het talrijke publiek. Dit verslag vat een sessie samen over innovaties binnen het veld van de cardiomyopathieën. Een actueel topic, zeker gezien de nieuwe Europese richtlijnen. De sprekers waren James Januzzi (Boston, VS), Iacopo Olivotto (Firenze, Italië), Arsen Ristic (Belgrado, Servië), Stephane Heymans (Maastricht, Nederland) en Damien Logeart (Parijs, Frankrijk).
Nieuwe benaderingen voor diabetische cardiomyopathie
James Januzzi - Boston, VS
Hoewel deze entiteit voor velen nieuw is, is ze toch belangrijk gezien de stijgende prevalentie en vooruitgang op vlak van therapie. De voordracht werd toegespitst op drie vragen: wat is diabetische cardiomyopathie en hoe prevalent is het? Hoe wordt de diagnose gesteld? En tot slot: welke behandelingen zijn mogelijk?
Wanneer men spreekt over het cardiovasculaire risico bij patiënten met diabetes mellitus, denkt men voornamelijk aan atherosclerose en coronairlijden. Wanneer men echter de cardiovasculaire outcomestudies van de antidiabetica bekijkt, spant hartfalen de kroon. Een grote multinationale studie bij > 750 000 patiënten met diabetes mellitus zonder voorgaand cardiovasculair of renaal lijden toonde aan dat na een mediane opvolgduur van 4,5 jaar ongeveer een kwart van de patiënten hartfalen had ontwikkeld (tegenover 11 % acuut myocardinfarct) en dat het voorkomen van hartfalen in deze populatie onafhankelijk geassocieerd was met een verhoogd mortaliteitsrisico.1 Diabetische cardiomyopathie (CMP) is een van de redenen waarom hartfalen zo prevalent is in deze bevolkingsgroep. De aandoening kan voorkomen bij zowel type 1- als type 2-diabetes mellitus. Centraal in de pathofysiologie staan hyperglykemie en insulineresistentie. Hierdoor treden diverse metabole veranderingen op, waaronder een toegenomen oxidatie van vetzuren met lipotoxiciteit tot gevolg, inflammatie en opstapeling van zogenoemde advanced glycation end products (eiwitten die onherstelbaar beschadigd zijn doordat er suikergroepen aan verankerd zijn) met myocardiale remodellering en veranderde calciumhuishouding in de myocardcellen tot gevolg. Hierdoor ontstaan apoptose, fibrose en myocardhypertrofie. Initieel zal dit leiden tot een diastolische disfunctie als gevolg van toegenomen ventriculaire stijfheid, maar na verloop van tijd treedt verdere progressie op naar systolische disfunctie.2 De prevalentie bij patiënten met diabetes mellitus verschilt tussen studies, maar ligt tussen de 17 en 24 %.3-5 Gekende risicofactoren voor de ontwikkeling van dit ziektebeeld zijn leeftijd, duur van diabetes, verminderde renale klaring (< 60 ml/min) en de aanwezigheid van andere micro- en macrovasculaire diabetische complicaties. Wat betreft het stellen van de diagnose is het belangrijk te weten dat veel patiënten pauci- tot asymptomatisch zijn, zeker in de beginfase. Tijdens een inspanningsproef is er vaak wel een duidelijk verminderde inspanningscapaciteit en bovendien is ook disfunctie merkbaar op de beeldvorming. Meestal zijn linkerventrikelhypertrofie, linkeratriumdilatatie, een verhoogde linkeratriumdruk (op basis van een verhoogde E/e'-ratio) en ook een verminderde globale longitudinale strain aanwezig. Een combinatie van voorgaande echocardiografische parameters toonde in onderzoek een incrementeel risico op het ontwikkelen van een hartfalenevent bij asymptomatische patiënten met diabetes mellitus met normale ejectiefractie en zonder evidentie voor coronairlijden.6 Daarnaast zijn cardiale biomerkers (natriuretische peptiden en troponines) vaak gestegen wanneer er geen andere oorzaak van hartfalen (zoals bijvoorbeeld coronairlijden) is. Gezien het endemische karakter van diabetes mellitus en de hoge prevalentie van diabetische CMP heeft de American Diabetes Association recent een consensusdocument gepubliceerd over deze ziekte-entiteit.7 Patiënten met diabetes worden hierbij ingedeeld in drie risicoklassen (A: met bijkomende risicofactoren voor HF; B: met structurele afwijkingen op echo; C: met symptomen van HF - figuur 1). De richtlijnen raden aan om bij patiënten uit risicoklasse A en B minstens eenmaal per jaar cardiale biomerkers te bepalen en beeldvorming uit te voeren als deze verhoogd zijn om zo vroegtijdig HFpEF/HFrEF te diagnosticeren.7
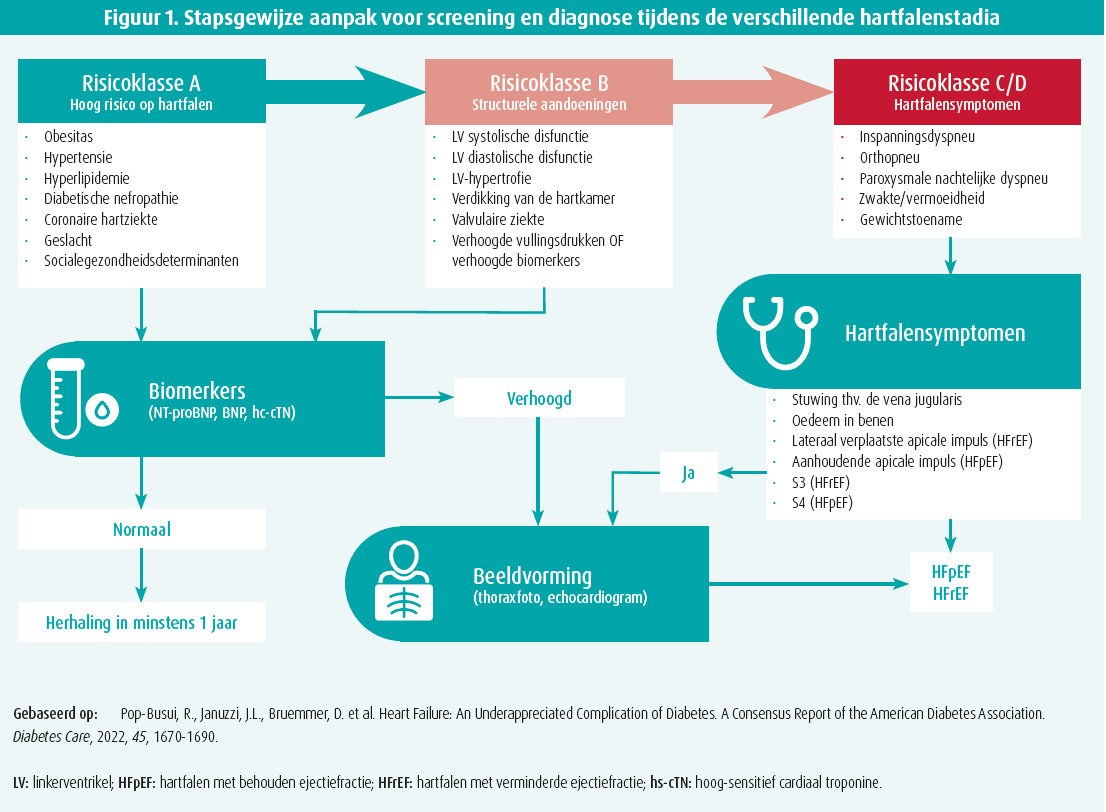
In de discussie die na de presentaties volgde, kwam de vraag of deze entiteit wezenlijk verschilt van HFpEF. De spreker antwoordde dat diabetische CMP een van de mogelijke oorzaken van HFpEF in deze patiëntenpopulatie is, en dat een specifieke diagnose belangrijk is omdat er de laatste jaren vooruitgang is geboekt op vlak van gerichte therapie. Deze aanpak bestaat globaal uit drie pijlers: de aanpak van andere risicofactoren (zoals obesitas, arteriële hypertensie en hypercholesterolemie), het nastreven van correcte glykemische controle met onder andere SGLT2-inhibitoren en GLP-agonisten (DPP4-inhibitoren en thiazolidinedionderivaten zijn te vermijden) en ten slotte gerichte therapie. Wanneer het op gerichte therapie voor diabetische CMP aankomt, zitten er heel wat opties in de pijplijn: gentherapie, neureguline-1, anti-inflammatoire therapie, mitotropen en aldosereductase-inhibitoren. De spreker ging voornamelijk dieper in op de laatste twee. Ninerafaxstat (een mitotroop) heeft als doel de mitochondriale functie te verbeteren waardoor de myocardiale energiedeficiëntie (ATP-deficiëntie) verminderd wordt, en ook een reductie van cardiale steatose (en dus lipotoxiciteit) en een verbetering van diastolische functie wordt bekomen. Dit alles werd bevestigd in de resultaten van een recente fase 2A-trial (IMPROVE-DiCE-trial).8 Aldosereductase- inhibitoren werden vroeger reeds ontwikkeld om de microvasculaire complicaties van diabetes mellitus tegen te gaan. Hun werking berust op de inhibitie van de polyole pathway. Bij patiënten met hyperglykemie zorgt deze pathway namelijk voor omvorming van intracellulaire glucose naar fructose en sorbitol waarbij natuurlijke antioxidanten (bv. glutathion) worden verbruikt en de cel kwetsbaar wordt voor oxidatieve stress.9 De eerste generatie van deze medicijnen bleek echter veel off-targetcomplicaties te veroorzaken en werd van de markt gehaald. Nu worden nieuwe molecules onderzocht, waaronder de molecule 'AT-001', die potenter zijn en minder complicaties veroorzaken. AT-001 bleek in kleinschalig onderzoek aanleiding te geven tot duidelijk lagere sorbitolconcentraties en ook een daling in NT-proBNP.10 Ondertussen is een gerandomiseerde, placebogecontroleerde studie (ARISE-HF) lopende om de veiligheid en effectiviteit van deze molecule na te gaan in een populatie patiënten met diabetische CMP. De eerste resultaten worden volgend jaar verwacht.
Hypertrofe cardiomyopathie: medicamenteuze therapie of interventie
Iacopo Olivotto - Firenze, Italië
De spreker startte zijn voordracht met een korte opsomming van de huidige richtlijnen omtrent de behandeling van hypertrofe obstructieve cardiomyopathie: medicamenteus (bètablokkade, verapamil, disopyramide) en de invasieve opties (chirurgische myomectomie en alcoholische septumablatie). Het zijn allemaal krachtige behandelingen met bewezen effect op symptomatologie, maar er zijn ook inherente tekortkomingen. Zo is het geen panacee voor alle patiënten in alle situaties en blijven er aan de invasieve opties risico's verbonden (bv. 5-7 % nood aan pacemakerplaatsing, voornamelijk na alcoholseptumablatie), zijn de uitkomsten heel operatorafhankelijk en is vaak een heringreep noodzakelijk (voornamelijk bij de septumablaties). Bovendien wordt de onderliggende pathofysiologie, en dus ook de ziekteprogressie, niet aangepakt. Om hierop in te spelen is de laatste jaren het concept van myosinemodulatie door zogenoemde targeted small molecules opgekomen. Deze worden peroraal ingenomen en binden zeer selectief aan cardiale myosine met in muismodellen normalisatie van de contractiliteit, betere compliantie, minder hypertrofie, minder fibrose en minder energieconsumptie tot gevolg. Bij mensen zijn de data beperkter. De EXPLORER-HCM, een fase 3, gerandomiseerde, dubbelblinde, placebogecontroleerde trial, toonde reeds dat een behandeling met mavacamten aanleiding gaf tot een verbeterde inspanningscapaciteit, minder linkerventrikeluitstroombaan (LVOT)-obstructie en beterschap in de NYHA-klasse bij patiënten met hypertrofe obstructieve cardiomyopathie.11 Een gelijkaardige fase 3-studie (SEQUOIA-HCM) met een ander preparaat, aficamten, loopt nog en de resultaten worden binnenkort verwacht. Data over de lange termijn zijn momenteel nog niet beschikbaar.
Tijdens de verdere uiteenzetting ging de spreker dieper in op de plaats voor deze nieuwe behandeling in het landschap van hypertrofe cardiomyopathie. Hij plaatst de behandeling tussen de eerstelijns medische behandeling (bètablokkade, verapamil, disopyramide) en interventionele ingrepen. De vraag stelt zich dan of de noodzaak tot invasief ingrijpen in de toekomst sterk zal verminderen door deze bijkomende medicamenteuze behandeling. Hierover is reeds onderzoek gebeurd.12 In deze RCT werden 112 patiënten met hypertrofe obstructieve cardiomyopathie met LVOT-gradiënt > 50 mmHg die in aanmerking kwamen voor septale reductietherapie gerandomiseerd tot een behandeling met mavacamten of placebo en zestien weken opgevolgd. Als primair eindpunt werd de proportie van patiënten genomen die alsnog in aanmerking kwamen of waren verwezen voor septale reductietherapie ondanks de behandeling. Men zag dat dit het geval was bij 76,8 % van de patiënten onder behandeling met placebo vs. 17,9 % van de patiënten die een behandeling met mavacamten hadden ontvangen. Ook secundaire eindpunten (NYHA-klasse, LVOT-gradiënt, levenskwaliteit en cardiale biomerkers) spraken in het voordeel van mavacemten.12 Langetermijneffecten zijn ook hier nog niet beschikbaar. De spreker merkte verder op dat er na publicatie van deze resultaten verschillende redactionelen zijn verschenen waarin verder werd gedebatteerd over het blijvende belang van chirurgie. Hij concludeert dat chirurgisch ingrijpen in deze patiëntpopulatie beschikbaar moet blijven, maar dat een meerderheid van de patiënten een ingreep zal kunnen vermijden door medische therapie. Wel is er nog meer data nodig, ook op de lange termijn, om de plaats van orale myosine-inhibitoren in de behandeling van HCM verder te consolideren en ook hun kosteneffectiviteit tegenover de andere therapeutische opties na te gaan.
De rol van biopsie
Arsen Ristic - Belgrado, Servië
De volgende sessie was een beknopte uiteenzetting over de rol van endomyocardbiopsie bij mensen met cardiomyopathie. Tijdens de lezing werd voornamelijk verwezen naar een consensusdocument van de Europese, Amerikaanse en Japanse hartfalenorganisaties over het gebruik van endomyocardbiopsie.13 De spreker benadrukte dat het uitvoeren van een biopt zeker zijn plaats heeft in de diagnostiek van cardiomyopathie omdat diverse pathognomonische bevindingen mogelijk zijn: myocarditis, maligniteit, loefflersyndroom, ijzerstapeling, amyloïd, etc. Wel moet men beseffen dat de diagnostische opbrengst zeer operatorafhankelijk is, dit voor zowel de uitvoerende (interventie)cardioloog als de patholoog die het specimen onderzoekt. Men moet bovendien goed op de hoogte zijn van de absolute contra-indicaties voor het uitvoeren van de procedure, en de potentiële complicaties kennen en kunnen behandelen. De spreker pleitte dan ook voor centralisatie van deze procedure in ervaren centra, zowel voor het uitvoerende deel van de procedure als voor het pathologische nazicht van het specimen. Op die manier betreft het volgens de spreker een laagrisicoprocedure met in veel gevallen een diagnostische meerwaarde die niet vervangen kan worden door beeldvorming, zoals nucleaire magnetische resonantie (NMR).
De rol van genetica
Stephane Heymans - Maastricht, Nederland
Vaak worden patiënten naar de dienst Genetica verwezen vanwege een onverklaard hartfalen en/of een gereanimeerde plotse dood en is er op beeldvorming sprake van hypertrofe, gedilateerde of aritmogene cardiomyopathie. Op de dienst Genetica wordt vervolgens uitgebreide counseling uitgevoerd, alsook integratie van anamnese, kliniek, beeldvorming en uiteindelijk ook genetische testen. Wat dit laatste betreft werd in 1990 een eerste pathogene genetische variant ontdekt in het myosine heavy chain gene14, maar zijn de mogelijkheden ondertussen fors verbreed met onder andere whole genome sequencing waarbij het volledige genoom kan worden getest in één test. Het is echter belangrijk te weten dat de aanwezigheid van een genvariant onvoldoende is om een diagnose te stellen. De aanwezigheid van een pathogeen genotype zal namelijk niet steeds tot hetzelfde fenotype leiden. Het bepaalt wel de gevoeligheid van een individu om een fenotype te ontwikkelen, maar leeftijd, epigenetica en omgevingsfactoren (bv. virussen, auto-immuniteit, chemo, alcohol, comorbiditeiten, etc.) spelen hierbij ook een belangrijke rol (gen-omgevingsinteractie). Men weet bijvoorbeeld dat bijkomende blootstelling aan omgevingsfactoren het finale fenotype en de prognose van patiënten met gedilateerde cardiomyopathie (DCM) in belangrijke mate bepaalt.15 Daarom is een multidisciplinair cardiomyopathieprogramma noodzakelijk waarin klinische, biochemische, pathologische, immunologische, beeldvormingsgerelateerde en genetische kenmerken worden samengelegd.
Vervolgens werd er dieper ingegaan op de monogenetische varianten. Tot 70 % van de patiënten met een hypertrofische cardiomyopathie (HCM) heeft dergelijke variant, het meest frequent in de sarcomeergenen (zoals MYH7, MYBPC3, TNNT2 en TNNI3). Bij DCM is er een genetische predispositie bij ongeveer 35 % van de patiënten met een positieve familiale voorgeschiedenis en bij ongeveer 15 % van de patiënten zonder positieve familiale voorgeschiedenis, waarbij zeven genen verantwoordelijk zijn voor 95 % van de gevallen. Bij aritmogene CMP zijn voornamelijk varianten in de genen die coderen voor desmosomale eiwitten verantwoordelijk en wordt tot bij 70 % een pathogene variant vastgesteld. Globaal moet wel worden gesteld dat de verschillende fenotypes van cardiomyopathie (HCM, DCM en aritmogene CMP) vaak overlap vertonen in de onderliggende genetische variaties.
Verder werd nog de focus gelegd op titine, het grootste menselijke eiwit. Zogenoemde truncerende varianten (TTNtv) in de A-band van dit eiwit zijn verantwoordelijk voor een derde van alle genetisch voorbeschikte gevallen van DCM. Ondertussen weet men ook dat dergelijke varianten eveneens prevalenter zijn bij patiënten met een 'verworven' cardiomyopathie (bv. alcoholische CMP, peripartum CMP, chemo-geïnduceerde CMP en zelfs bij acute myocarditis). Dit doet denken aan een second hit hypothese, waarbij patiënten met een variant gevoeliger zijn voor de ontwikkeling van een klinisch ziektebeeld (zoals chemo-geïnduceerde CMP) bij blootstelling aan een oorzakelijk agens. De aanwezigheid van een TTNtv is dus meer en meer van klinisch belang.
How to put the pieces of the puzzle together
Damien Logeart - Parijs, Frankrijk
Tot slot vatte Damien Logeart de voorgaande informatie samen en besprak hij een stappenplan om tot een geïntegreerde aanpak te komen bij patiënten met cardiomyopathie waarbij het belang van een uitgebreide persoonlijke en familiale anamnese en het uitsluiten van fenokopieën nogmaals werd benadrukt aangezien voor deze groepen specifieke behandelingen beschikbaar zijn. Zo werd nogmaals benadrukt dat het belangrijk is om bij een vermoeden van HCM onder andere amyloïdose, ziekte van Fabry, aortaklepstenose, hypertensieve CMP en een atletenhart uit te sluiten en bij DCM ernstige hypertensie, valvulair en ischemisch hartlijden uit te sluiten, evenals andere oorzaken zoals toxiciteit, nutriëntdeficiëntie, tachycardie, etc.
Referenties
- Birkeland, K.I., Bodegard, J., Eriksson, J.W. et al. Heart failure and chronic kidney disease manifestation and mortality risk associations in type 2 diabetes: A large multinational cohort study. Diabetes Obes Metab, 2020, 22 (9), 1607-1618.
- Jia, G., Hill, M.A., Sowers, J.R. Diabetic Cardiomyopathy: An Update of Mechanisms Contributing to This Clinical Entity. Circ Res, 2018, 122 (4), 624-638.
- Segar, M.W., Khan, M.S., Patel, K.V. et al. Prevalence and Prognostic Implications of Diabetes With Cardiomyopathy in Community-Dwelling Adults. J Am Coll Cardiol, 2021, 78 (16), 1587-1598.
- Pham, I., Cosson, E., Nguyen, M.T. et al. Evidence for a Specific Diabetic Cardiomyopathy: An Observational Retrospective Echocardiographic Study in 656 Asymptomatic Type 2 Diabetic Patients. Int J Endocrinol, 2015, 2015, 743503.
- Dandamudi, S., Slusser, J., Mahoney, D.W. et al. The prevalence of diabetic cardiomyopathy: a population-based study in Olmsted County, Minnesota. J Card Fail, 2014, 20 (5), 304-309.
- Wang, Y., Yang, H., Huynh, Q. et al. Diagnosis of Nonischemic Stage B Heart Failure in Type 2 Diabetes Mellitus: Optimal Parameters for Prediction of Heart Failure. JACC Cardiovasc Imaging, 2018, 11 (10), 1390-1400.
- Pop-Busui, R., Januzzi, J.L., Bruemmer, D. et al. Heart Failure: An Underappreciated Complication of Diabetes. A Consensus Report of the American Diabetes Association. Diabetes Care, 2022, 45 (7), 1670-1690.
- Hundertmark, M., Siu, A.G., Matthews, V. et al. A phase 2a trial investigating ninerafaxstat - a novel cardiac mitotrope for the treatment of diabetic cardiomyopathy (IMPROVE-DiCE). Eur Heart J, 43, Epub ahead of print 2022. DOI: 10.1093/eurheartj/ ehac544.246.
- Brownlee, M. The pathobiology of diabetic complications: a unifying mechanism. Diabetes, 2005, 54 (6), 1615-1625.
- Perfetti, R., Shendelman, S. Abstract 13475: Clinical Assessment of AT-001, an Aldose Reductase Inhibitor in Development for Diabetic Cardiomyopathy: A 28-Day Proof of Concept Study. Circulation, 2019, 140, A13475-A13475.
- Olivotto, I., Oreziak, A., Barriales-Villa, R. et al. Mavacamten for treatment of symptomatic obstructive hypertrophic cardiomyopathy (EXPLORER-HCM): a randomised, double-blind, placebocontrolled, phase 3 trial. The Lancet, 2020, 396 (10253), 759-769.
- Desai, M.Y., Owens, A., Geske, J.B. et al. Myosin Inhibition in Patients With Obstructive Hypertrophic Cardiomyopathy Referred for Septal Reduction Therapy. J Am Coll Cardiol, 2022, 80 (2), 95-108.
- Seferović, P.M., Tsutsui, H., McNamara, D.M. et al. Heart Failure Association of the ESC, Heart Failure Society of America and Japanese Heart Failure Society Position statement on endomyocardial biopsy. Eur J Heart Fail, 2021, 23 (6), 854-871.
- Geisterfer-Lowrance, A.A., Kass, S., Tanigawa, G. et al. A molecular basis for familial hypertrophic cardiomyopathy: a beta cardiac myosin heavy chain gene missense mutation. Cell, 1990, 62 (5), 999-1006.
- Hazebroek, M.R., Moors, S., Dennert, R. et al. Prognostic Relevance of Gene-Environment Interactions in Patients With Dilated Cardiomyopathy: Applying the MOGE(S) Classification. J Am Coll Cardiol, 2015, 66 (12), 1313-1323.
Niets van de website mag gebruikt worden voor reproductie, aanpassing, verspreiding, verkoop, publicatie of commerciële doeleinden zonder voorafgaande schriftelijke toestemming van de uitgever. Het is ook verboden om deze informatie elektronisch op te slaan of te gebruiken voor onwettige doeleinden.