De indicatie voor anticoagulantia bij voorkamerfibrillatie (VKF) is goed gekend en goed bestudeerd, maar het wordt al heel wat minder duidelijk als VKF niet klinisch (door middel van een ecg), maar via ambulante langdurige ritmemonitoring wordt vastgesteld. Deze studie geeft ons een eerste inzicht in de aanpak van deze frequente aandoening.
Op het ESC-congres eind augustus dit jaar werden de resultaten van de langverwachte NOAH-AFNET 6-studie1 gepresenteerd die de praktijk van vele cardiologen zeker zal veranderen.
Achtergrond
Beroerte en VKF blijven een intrigerend onderwerp. Er is reeds tientallen jaren een hevig debat gaande over de rol van VKF bij beroerte en vermoedelijk is VKF eerder een risicomarker dan een risicofactor voor het ontstaan van een beroerte.2 Atriale cardio(myo)pathie is de relatief nieuwe term die gebruikt wordt om de fysiopathologie van onder andere een embolische beroerte van onbekende oorsprong (embolic stroke of undetermined source - ESUS) te verklaren.
Atriale cardio(myo)pathie is een aandoening waarbij atriale dilatatie, fibrose en endotheliale disfunctie ontstaat en die op zich ook gerelateerd is aan het ontstaan van VKF.3
Orale anticoagulantia zijn de hoeksteen van de behandeling bij VKF (met een of meerdere risicofactoren) en heel vaak worden ze pas opgestart als er al een beroerte heeft plaatsgevonden. Daarom is er veel aandacht naar ambulante screeningsprogramma's om VKF vroegtijdig op te sporen. Vaak worden dan kortere, subklinische episodes van VKF vastgesteld. Een belangrijke vraag blijft vanaf welke aritmielast (burden) men orale anticoa gulantia moet opstarten.4-6 Daarnaast hebben we ook bij patiënten met pacemakers en defibrillatoren regelmatig een continue monitoring van het atriale ritme. Wanneer hierbij dan episodes van atriale snelle ritmes (atrial high rate episodes - AHRE) worden vastgesteld, wordt de opstart van orale anticoagulantia frequent overwogen, voornamelijk bij patiënten met een hoger risico op beroerte en bij AHRE's die langer duren dan 24 uur.7 Deze, meestal asymptomatische, patiënten lopen echter niet hetzelfde risico op een beroerte als patiënten waarbij op klinische basis VKF wordt vastgesteld (door middel van een ecg of klassieke holtermonitoring).
Er was dus tot nu toe een belangrijk tekort aan wetenschappelijke evidentie op dit terrein en daar brengt deze studie nu verandering in.
Methodes
De NOAH-AFNET 6-studie is een dubbelblinde, gerandomiseerde studie waarbij patiënten werden geïncludeerd die bij het uitlezen van hun ritmemonitoring (pacemaker, defibrillator, resynchronisatietoestel of geïmplanteerde looprecorder) een of meerdere AHRE's toonde. Deze AHRE moet zich ten minste twee maanden na implantatie van het toestel voordoen, moet even lang of langer duren dan 6 minuten en moet een atriaal ritme hebben van minimum 170 slagen per minuut. De geïncludeerde patiënten zijn ouder dan of gelijk aan 65 jaar, hebben nooit eerder de klinische diagnose van VKF gekregen en hebben minstens één risicofactor voor het ontstaan van een beroerte (volgens de criteria van de CHA2DS2-VASc-score).
Geschikte patiënten werden vervolgens 1:1 gerandomiseerd naar de inname van edoxaban (een directe factor Xa-inhibitor) of placebo. Edoxaban werd voorgeschreven volgens de huidige richtlijnen bij de behandeling van patiënten met VKF, namelijk 60 mg eenmaal daags, of 30 mg eenmaal daags (in functie van gewicht, nierfunctie en interagerende medicatie). Bij de placebogroep werd een dubbel-dummy placebotablet voorgeschreven met ofwel geen actief bestanddeel, ofwel acetylsalicylzuur aan een dosis van 100 mg per dag. Dat laatste werd bepaald aan de hand van de gekende indicaties voor het gebruik van acetylsalicylzuur, namelijk perifeer- of coronairlijden of voorgeschiedenis van een hartinfarct of beroerte.
Het primaire eindpunt van werkzaamheid was het eerste optreden van een samengesteld eindpunt, met name cardiovasculaire dood, beroerte of systemische embolie. Het primaire eindpunt van veiligheid was eveneens een samengesteld eindpunt, met name dood van elke origine, of ernstige bloeding. De belangrijkste secundaire uitkomsten waren de individuele componenten van de primaire eindpunten, het samengestelde eindpunt van beroerte of systemische embolie, en meerdere zachtere uitkomsten zoals patiënttevredenheid, symptomen, cognitieve functie en functionele status.
Resultaten
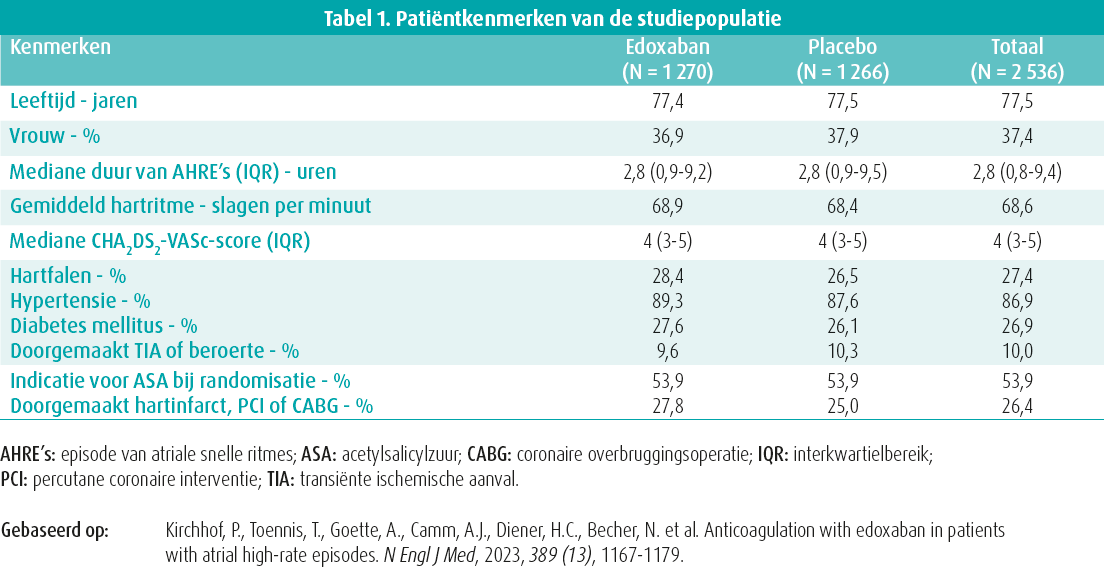
Tussen 2016 en 2022 werden in 18 Europese landen 2 536 patiënten gerandomiseerd. De klinische en demografische patiëntkenmerken zijn weergegeven in tabel 1 en zijn vergelijkbaar in beide groepen. De studie werd vroegtijdig beëindigd na een mediane opvolging van 21 maanden, vanwege bezorgdheid over de veiligheid en de werkzaamheid van edoxaban. Klinische VKF ontwikkelde zich bij 8,7 % per patiënt per jaar in de edoxabangroep en 8,8 % per patiënt per jaar in de placebogroep.
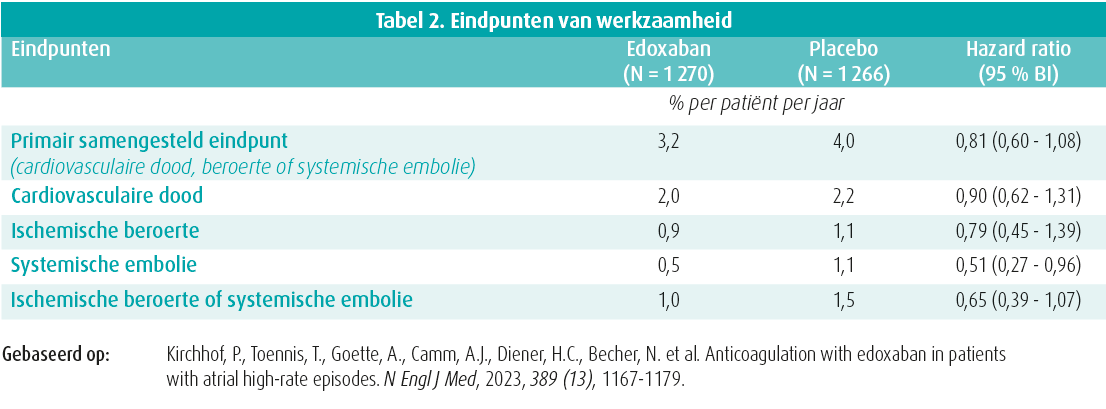
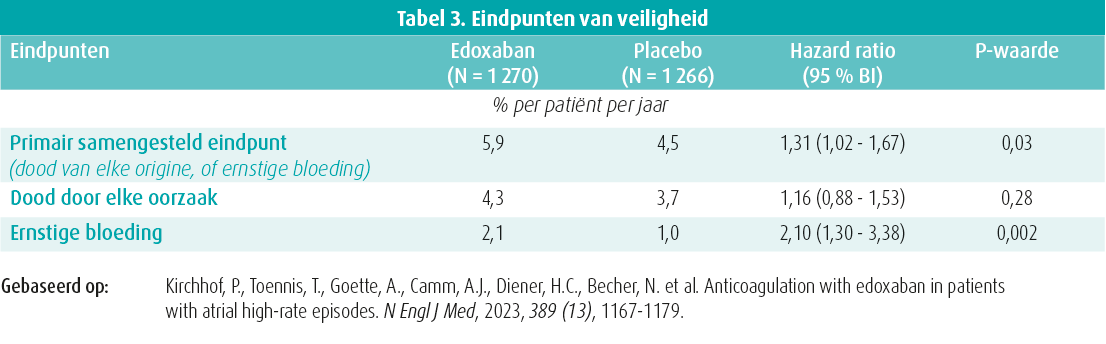
Het primaire eindpunt van werkzaamheid en veiligheid zijn weergegeven in respectievelijk tabel 2 en 3. Zowel bij de primaire als de secundaire eindpunten van werkzaamheid zijn er geen significante verschillen tussen de edoxaban- en de placebogroep. Bij de eindpunten van veiligheid daarentegen zijn er significant meer bloedingen in de edoxabangroep. De overige secundaire uitkomsten waren vergelijkbaar tussen beide groepen.
Bespreking
Bij de onderzochte groep patiënten met AHRE heeft edoxaban dus geen voordeel naar het primaire eindpunt toe, maar is er daarentegen bezorgdheid over het groter aantal bloedingen. De incidentie van de vooropgestelde eindpunten in deze studie was over het algemeen binnen de verwachtingen. Er valt echter op te merken dat, ondanks de hogere leeftijd en de aanwezige risicofactoren, het aantal beroertes in deze studie duidelijk lager is dan in andere reeksen met een klinische diagnose van VKF.8-11 Dit verschil is vermoedelijk te wijten aan een verminderde aritmielast bij AHRE.
We weten al dat een lagere aritmielast gepaard gaat met een lager risico op beroerte. Zo hebben patiënten met paroxysmale VKF minder risico dan patiënten met persistente of permanente VKF.12 Ook hebben VKF-patiënten met een succesvolle ritmecontrole minder kans op een beroerte.13 Daarnaast werd ook in een eerder gepubliceerde gerandomiseerde studie bij patiënten met risicofactoren waarbij VKF werd vastgesteld door middel van geïmplanteerde looprecorders (ILR) een lagere incidentie van beroerte vastgesteld (met evenmin baat bij anticoagulantia).14 Al deze resultaten ondersteunen de bevindingen van de huidige studie, waarbij we bij patiënten met AHRE's maar zonder klinische evidentie voor VKF beter geen orale anticoagulantia voorschrijven.
De belangrijkste beperking van deze studie is de vroegtijdige onderbreking, waardoor de studie onvoldoende kracht had om een beperkt voordeel van edoxaban op het voorkomen van beroerte te detecteren of te weerleggen.
Eerder onverwacht worden deze resultaten echter niet ondersteund door de ARTESIA-studie.15 Deze studie werd begin november gepubliceerd in hetzelfde tijdschrift en heeft een vergelijkbare opstelling maar met apixaban in plaats van edoxaban. We zullen verdere analyse en studies moeten afwachten vooraleer meer definitieve conclusies te kunnen trekken.
Besluit
Patiënten met een AHRE van 65 jaar of ouder, met een of meerdere risicofactoren voor beroerte, zonder klinisch VKF (gedetecteerd door middel van een ecg), hebben geen baat bij het opstarten van edoxaban, maar hebben daarentegen een hoger risico op ernstige bloeding.
Referenties
- Kirchhof, P., Toennis, T., Goette, A., Camm, A.J., Diener, H.C., Becher, N. et al. Anticoagulation with edoxaban in patients with atrial high-rate episodes. N Engl J Med, 2023, 389 (13), 1167-1179.
- Bunch, T.J., May, H.T. Atrial fibrillation: a risk factor or risk marker? Eur Heart J, 2016, 37 (38), 2890-2892.
- Stalikas, N., Doundoulakis, I., Karagiannidis, E., Kartas, A. Gavriilaki, M., George Sofidis, G. et al. Prevalence of markers of atrial cardiomyopathy in embolic stroke of undetermined source: A systematic review. Eur J Int Med, 2022, 99, 38-44.
- Tiver, K.D., Quah, J., Lahiri, A., Ganesan, A.N., McGavigan, A.D. Atrial fibrillation burden: an update the need for a CHA2DS2VASc-AF-Burden score. Europace, 2021, 23 (5), 665-673.
- Healey, J.S., Connolly, S.J., Gold, M.R., Israel, C.W., Van Gelder, I.C., Capucci, A. et al. Subclinical atrial fibrillation and the risk of stroke. N Eng J Med, 2012, 366 (2), 120-129.
- Van Gelder, I.C., Healey, J.S., Crijns, H.J., Wang, J., Hohnloser, S.H., Gold, M.R. et al. Duration of device-detected subclinical atrial fibrillation and occurrence of stroke in ASSERT. Eur Heart J, 2017, 38 (17), 1339-1344.
- Perino, A.C., Fan, J., Askari, M., Heidenreich, P.A., Keung, E., Raitt, M.H. et al. Practice variation in anticoagulation prescription and outcomes after device-detected atrial fibrillation: insights from the veterans health administration. Circulation, 2019, 139 (22), 2502-2512.
- Friberg, L., Rosenqvist, M., Lip, G.Y. Evaluation of risk stratification schemes for ischaemic stroke and bleeding in 182,678 patients with atrial fibrillation: the Swedish atrial fibrillation cohort study. Eur Heart J, 2012, 33 (12), 1500-1510.
- Connolly, S.J., Eikelboom, J., Joyner, C., Diener, H.C., Hart, R., Golitsyn, S. et al. Apixaban in patients with atrial fibrillation. N Engl J Med, 2011, 364 (9), 806-817.
- Okumura, K., Akao, M., Yoshida, T., Kawata, M., Okazaki, O., Akashi, S. et al. Low-dose edoxaban in very elderly patients with atrial fibrillation. N Eng J Med, 2020, 383 (18), 1735-1745.
- Mant, J., Hobbs, F.R., Fletcher, K., Roalfe, A., Fitzmaurice, D., Lip, G.Y. et al. Warfarin versus aspirin for stroke prevention in an elderly community population with atrial fibrillation: a randomised controlled trial. The Lancet, 2007, 370 (9586), 493-503.
- Vanassche, T., Lauw, M.N., Eikelboom, J.W., Healey, J.S., Hart, R.G., Alings, M. et al. Risk of ischaemic stroke according to pattern of atrial fibrillation: analysis of 6563 aspirin-treated patients in ACTIVEA and AVERROES. Eur Heart J, 2015, 36 (5), 281-287.
- Kirchhof, P., Camm, A.J., Goette, A., Brandes, A., Eckardt, L., Elvan, A. et al. Early rhythm-control therapy in patients with atrial fibrillation. N Engl J Med, 2020, 383 (14), 1305-1316.
- Svendsen, J.H., Diederichsen, S.Z., Højberg, S., Krieger, D.W., Graff, C., Kronborg, C. et al. Implantable loop recorder detection of atrial fibrillation to prevent stroke (the LOOP study): a randomised controlled trial. The Lancet, 2021, 398 (10310), 1507-1516.
- Healey, J.S., Lopes, R.D., Granger, C.B., Alings, M., Rivard, L., McIntyre, W.F. et al. Apixaban for stroke prevention in subclinical atrial fibrillation. N Engl J Med, 2023.
Niets van de website mag gebruikt worden voor reproductie, aanpassing, verspreiding, verkoop, publicatie of commerciële doeleinden zonder voorafgaande schriftelijke toestemming van de uitgever. Het is ook verboden om deze informatie elektronisch op te slaan of te gebruiken voor onwettige doeleinden.