BSC-congresverslag - sessie 25
Tijdens deze sessie werd een update gegeven over hoe cardiale beeldvorming kan helpen in de diagnose, behandeling en opvolging van patiënten met cardiale amyloïdose. Cardiale amyloïdose is een vorm van een infiltratieve cardiomyopathie die ontstaat door extracellulaire accumulatie van verkeerd gevouwen proteïnes in het myocard, bestaande lichteketenimmunoglobulines (AL-amyloïdose) of verkeerd gevouwen transthyretine-eiwit (ATTR-amyloïdose).1 ATTR-amyloïdose wordt de laatste jaren meer en meer geïdentificeerd met een geschatte prevalentie van bijna 1:1000.2 De opstapeling van transthyretineeiwit neemt progressief toe met de leeftijd. Patiënten met een genetisch normale (wildtype) ATTR-amyloïdose (ATTRwt), werden vroeger benoemd als 'seniele' ATTR-amyloïdose. De exacte pathofysiologie hiervan is nog onbekend.3 Er bestaat ook een erfelijke variant (ATTRv) die minder prevalent is.
Rol van echocardiografie
Echocardiography in amyloidosis: solving enigma's in cardiac hypertrophy
Philippe Debonnaire - AZ Sint Jan, Brugge
In de eerste lezing bespreekt Philippe Debonnaire de actuele rol van echocardiografie bij cardiale amyloïdose. Naast klinische rode vlaggen, zoals spinaalkanaalstenose en bilateraal carpaletunnelsyndroom, zijn er ook een aantal echocardiografische kenmerken die ons kunnen doen denken aan cardiale amyloidose. De opstapeling van amyloïdfibrillen in het myocard kan zich manifesteren als een verdikking van het linkerventrikel (≥ 12 mm).1 Concentrische maar ook asymmetrische linkerventrikelhypertrofie, milde pericardiale effusie, biatriale dilatatie, een restrictief vullingspatroon en kleplijden (low-flow low-gradiënt aortaklepstenose) zijn onder andere de kenmerken van cardiale amyloïdose die kunnen worden opgespoord via echocardiografie.4, 5 Verder kan er ook een patroon van granulaire spikkeling worden gezien op echocardiografie, hoewel dit eerder een aspecifieke bevinding is.1 Soms zijn er echografisch slechts subtiele afwijkingen te zien. Een sensitieve marker voor cardiale amyloïdose is de afwijking van longitudinale strain van het linker- en rechterventrikel. Structurele afwijkingen op echocardiografie zijn afhankelijk van de hoeveelheid geaccumuleerde amyloïdfibrillen (amyloïdbelasting). Eerst worden functionele afwijkingen gezien, bijvoorbeeld in longitudinalestrainpatroon of bij hoge vullingsdrukken op basis van E/e'. Enkel bij belangrijke amyloïdbelasting gaan andere parameters zoals ejectiefractie en TAPSE afwijkend zijn6, 7 (figuur 1). Een ander typisch kenmerk voor cardiale amyloïdose is het patroon van 'apical sparing' bij de GLS-analyse, wat wijst op een relatief bewaarde longitudinale functie van de apex ten opzichte van de basale en midsegmenten. Een recente studie toonde aan dat apical sparing evenwel niet 100 % specifiek is voor cardiale amyloïdose.1
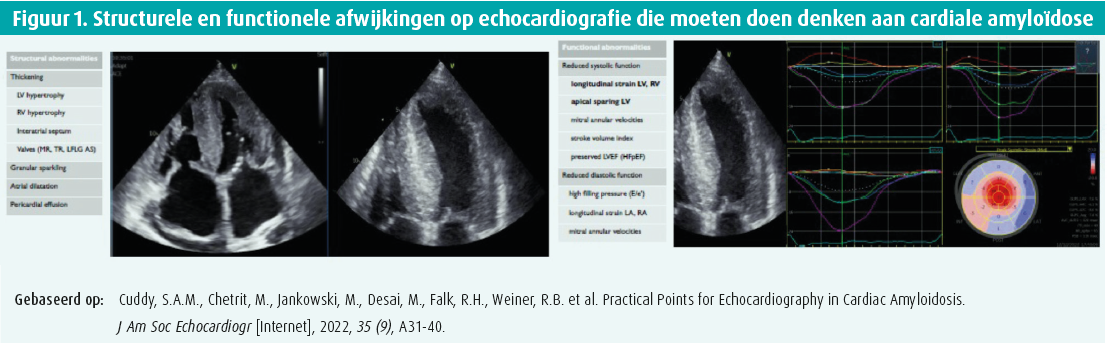
Echocardiografie kan ook worden gebruikt om ziekteprogressie en respons op behandeling in te schatten. De prognose van cardiale amyloïdose is gekoppeld aan de graad van amyloïddepositie en dit weerspiegelt zich ook in de waarde van verschillende biomerkers (zoals NT-proBNP, troponine T/I, en eGFR) alsook bepaalde echografische parameters, zoals longitudinale strain van het linker- en rechterventrikel en het linkeratrium. Ook valvulaire ziekten zoals ernstige aorta klepstenose en progressieve mitralisklepinsufficiëntie zijn prognostische markers voor cardiale amyloïdose.4, 8 In een aantal kleinere studies, werd een verbetering van globale longitudinale strain gecorreleerd aan een reductie van amyloïdbelasting bij patiënten die werden behandeld met tafamidis/patisiran.9, 10 Voorlopig zijn deze echocardiografische parameters onvoldoende gevalideerd voor de therapeutische evaluatie.
Rol van nucleaire beeldvorming
Nuclear imaging: do's and don'ts in amyloidosis diagnosis and follow-up
Oliver Gheysens - Nucleaire Geneeskunde, UCL
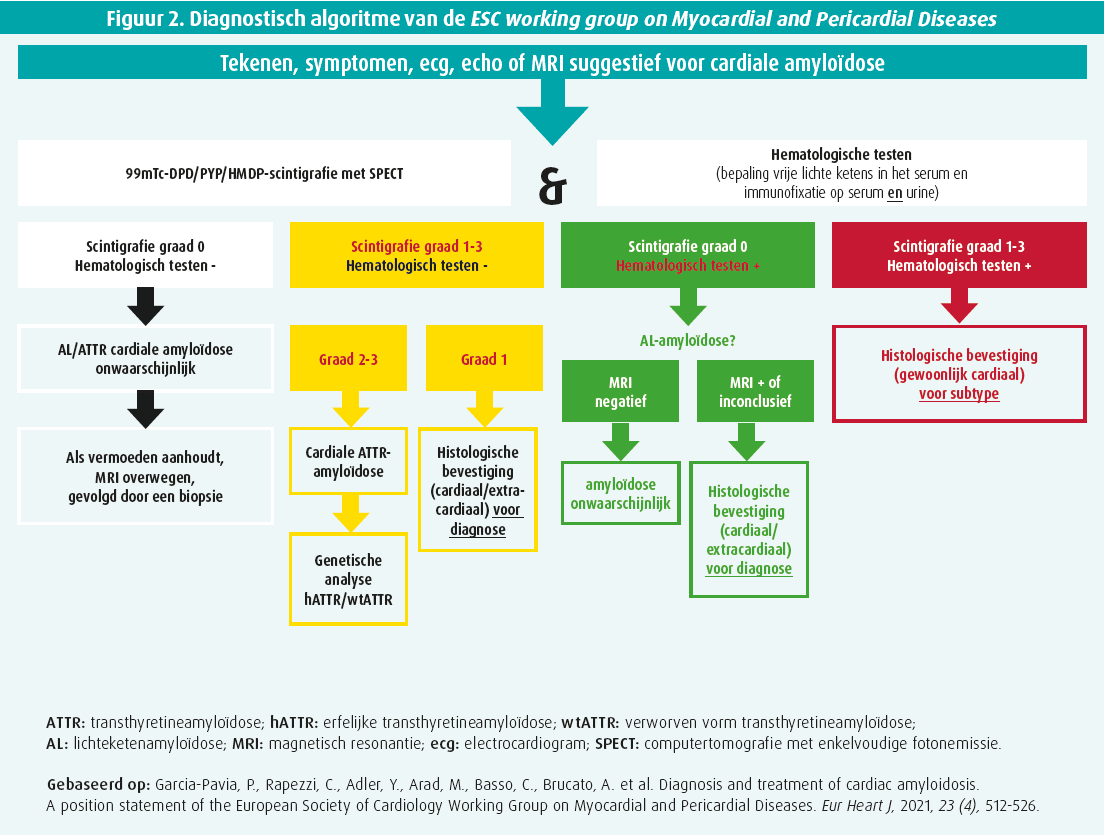
Echocardiografie en cardiale MRI kunnen ons structurele afwijkingen tonen die passen bij de diagnose van cardiale amyloïdose maar kunnen niet differentiëren tussen ATTR- en AL-amyloïdose. Volgens het diagnostische algoritme van de ESC working group on Myocardial and Pericardial Diseases moet er bij een vermoeden van cardiale amyloïdose verdere diagnostiek worden uitgevoerd voor de diagnose en differentiatie van het onderliggende subtype van cardiale amyloïdose11 (figuur 2). AL-amyloïdose kan worden aangetoond of uitgesloten door het bepalen van monoklonaliteit op serum-proteïne-elektroforese en serum-urine-immunofixatie. Daarnaast moet een cardiale scintigrafie (99m Technetiumdifosfonopropranodicarbon zuur [DPD], -pyrofosfaat [PYP] of -hydroxymethyleendifosfonaat [HMDP]) met SPECT/CT (computertomografie met enkelvoudige fotonemissie in combinatie met CT) worden uitgevoerd. Hierbij wordt de mate van uptake van contrast tracers in het myocard gebruikt voor het opstellen van de peruginigraad.11 Peruginigraad 2 of 3 uptake op cardiale scintigrafie heeft een hoge specificiteit voor ATTR-CA (positief voorspellende waarde van 98,5 %).12, 13 De diagnose van ATTR-CM kan enkel worden aangetoond als AL-amyloïdose is uitgesloten. Peruginigraad 1 uptake is specifiek voor amyloïdose maar hierbij is verdere diagnostiek noodzakelijk met eventueel biopsie, alsook in sommige gevallen bij grade 0 uptake (bv. bij AL-amyloïdose, bepaalde erfelijke ATTR-CM, vroegtijdige ATTR-CM).13 Invasieve diagnostiek zoals biopsie heeft evenwel een hoger complicatierisico. Dankzij het gebruik van cardiale scintigrafie wordt de diagnose van ATTR dus meer frequent gesteld en ook op een vroeger stadium van de ziekte.14 In de toekomst zullen kwantitatieve SPECT/CT en amyloïd-PET (met specifieke amyloïdtracers: 11c-PIB, 18F-labeled tracers, 124 I-evuzamitide) kunnen worden gebruikt om op een kwantitatieve manier veranderingen in uptake van myocard te meten en dit te correleren aan ziekteprogressie of respons op behandeling van ATTR-CA.15-17
Rol van cardiale MRI
Cardiac MRI: first-line or second-line use in amyloidosis?
Thomas Treibel - University College of London, Institute of Cardiovascular Science, Verenigd Koninkrijk
Naast echografie is cardiale MRI een van de belangrijke diagnostische tools voor cardiale amyloïdose. We kunnen naast linkerventrikelafmetingen en -functie ook littekenweefsel onderscheiden op MRI via late gadolinium enhancement. De amyloïdbelasting kunnen we inschatten op basis van extracellulaire volumemeting (ECV) via pre-post contrast T1-mapping.18
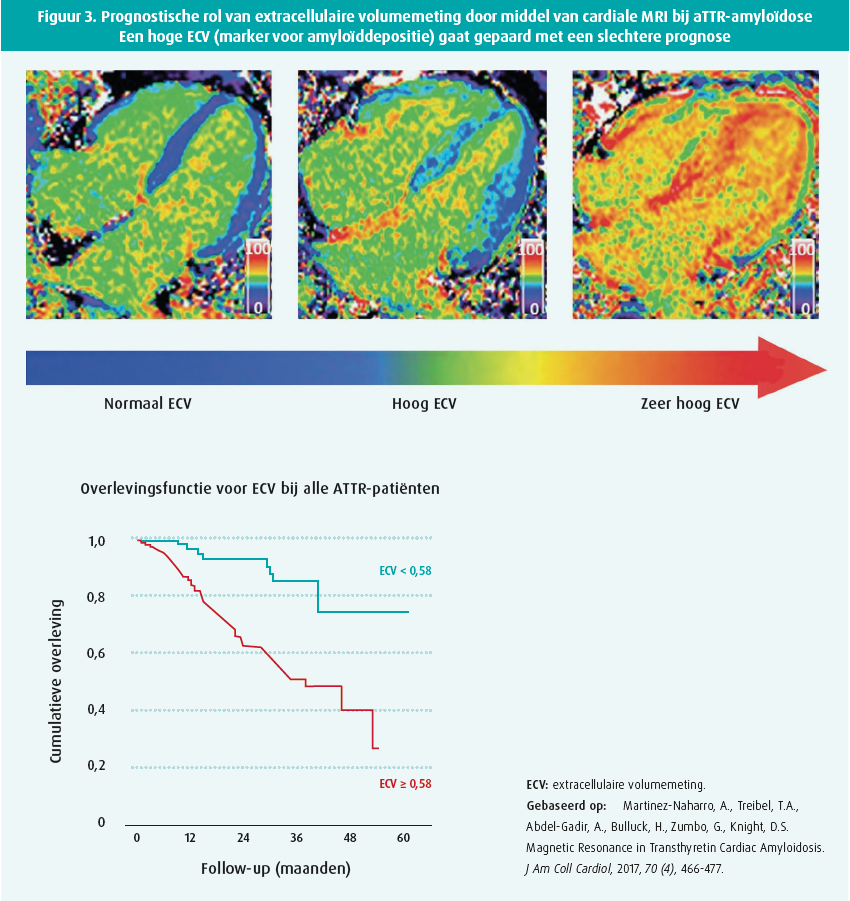
MRI kan ook een rol spelen in het inschatten van prognose en respons van behandeling bij cardiale amyloïdose. De uitgebreidheid van late gadolinium enhancement en kwantificatie van extracellulair volume spelen een rol bij de inschatting van de prognose, zowel bij ATTR- als AL-amyloïdose (figuur 3).5, 19, 20 MRI kan evenwel geen onderscheid maken tussen beide subvormen. Er zijn een aantal kleinere studies verschenen die de respons op therapie konden aantonen via MRI bv. met reductie van ECV na chemotherapie bij AL-amyloïdose of na behandeling met patisiran+diflunisal bij ATTR-amyloïdose.5, 19 Dankzij MRI kunnen we ook de respons van behandeling in andere orgaansystemen (zoals milt en lever) beter inschatten, bijvoorbeeld bij patiënten met AL-amyloïdose.21
Eerste studies tonen dat een ecg-triggered CT op termijn ook wordt gebruikt voor het inschatten van de amyloïdbelasting als alternatief voor de MRI. Dit kan nuttig zijn bij patienten die geen MRI kunnen ondergaan of waarbij reeds een CT is geïndiceerd voor een andere aandoening (bv. pre-TAVI, pre-mitraclip).22,23
Besluit
Echocardiografie en MRI kunnen geen definitieve diagnose bevestigen maar kunnen ons een klinisch vermoeden geven om bijkomend onderzoek zoals cardiale scintigrafie met SPECT/CT en monoklonale testen uit te voeren om de differentiatie te maken tussen ATTR- en AL-amyloïdose. Gezien de evolutie in nieuwe behandelingen voor cardiale amyloïdose is het belangrijk om ziekteprogressie en respons van therapie te kunnen inschatten. Naast echografie zullen ook andere beeldvormingsmodaliteiten zoals scintigrafie, amyloïd-PET/CT, MRI en cardiale CT hierbij een rol spelen. Er moeten nog verdere studies gebeuren om deze waarden te valideren.
Referenties
- Cuddy, S.A.M., Chetrit, M., Jankowski, M., Desai, M., Falk, R.H., Weiner, R.B. et al. Practical Points for Echocardiography in Cardiac Amyloidosis. J Am Soc Echocardiogr [Internet], 2022, 35 (9), A31-40.
- Kittleson, M.M., Ruberg, F.L., Ambardekar, A.V., Brannagan, T.H., Cheng, R.K., Clarke, J.O. et al. 2023 ACC Expert Consensus Decision Pathway on Comprehensive Multidisciplinary Care for the Patient With Cardiac Amyloidosis: A Report of the American College of Cardiology Solution Set Oversight Committee. J Am Coll Cardiol, 2023, 81 (11), 1076-1126.
- Ruberg, F.L., Grogan, M., Hanna, M., Kelly, J.W., Maurer, M.S. Transthyretin Amyloid Cardiomyopathy: JACC State-of-the-Art Review. J Am Coll Cardiol, 2019, 73 (22), 2872-2891.
- Chacko, L., Martone, R., Bandera, F., Lane, T., Martinez-Naharro, A., Boldrini, M. et al. Echocardiographic phenotype and prognosis in transthyretin cardiac amyloidosis. Eur Heart J, 2020, 41 (14), 1439-1447a.
- Martinez-Naharro, A., Treibel, T.A., Abdel-Gadir, A., Bulluck, H., Zumbo, G., Knight, D.S. et al. Magnetic Resonance in Transthyretin Cardiac Amyloidosis. J Am Coll Cardiol, 2017, 70 (4), 466-477.
- Knight, D.S., Zumbo, G., Barcella, W., Steeden, J.A., Muthurangu, V., Martinez-Naharro, A. et al. Cardiac Structural and Functional Consequences of Amyloid Deposition by Cardiac Magnetic Resonance and Echocardiography and Their Prognostic Roles. JACC Cardiovasc Imaging, 2019, 12 (5), 823-833.
- Boldrini, M., Cappelli, F., Chacko, L., Restrepo-Cordoba, M.A., Lopez-Sainz, A., Giannoni, A. et al. Multiparametric Echocardiography Scores for the Diagnosis of Cardiac Amyloidosis. JACC Cardiovasc Imaging, 2020, 13 (4), 909-920.
- Antonelli, J., Neveu, A., Kosmala, W., L'Official, G., Curtis, E., Oger, E. et al. Evolution and prognostic value of left ventricular deformation and myocardial work parameters in transthyretin amyloid cardiomyopathy. Eur Heart J Cardiovasc Imaging [Internet], 2023, jead318.
- Giblin, G.T., Cuddy, S.A.M., Gonza, E., Sewell, A., Murphy, A., Dorbala, S. et al. Effect of tafamidis on global longitudinal strain and myocardial work in transthyretin cardiac amyloidosis. Eur Heart J Cardiovasc Imaging, 2022, 23 (8), 1029-1039.
- Solomon, S.D., Adams, D., Grogan, M., González-Duarte, A., Maurer, M.S. et al. Effects of Patisiran, an RNA Interference Therapeutic, on Cardiac Parameters in Patients With Hereditary Transthyretin-Mediated Amyloidosis. Circulation, 2019, 139 (4), 431-443.
- Garcia-Pavia, P., Rapezzi, C., Adler, Y., Arad, M., Basso, C., Brucato, A. et al. Diagnosis and treatment of cardiac amyloidosis: A position statement of the ESC Working Group on Myocardial and Pericardial Diseases. Eur Heart J, 2021, 42 (16), 1554-1568.
- Gillmore, J.D., Maurer, M.S., Falk, R.H., Merlini, G., Damy, T., Dispenzieri, A. et al. Heart Failure Nonbiopsy Diagnosis of Cardiac Transthyretin Amyloidosis. Circulation, 2016, 133 (24), 2404-2412.
- Rauf, M.U., Hawkins, P.N., Cappelli, F., Perfetto, F., Zampieri, M., Argiro, A. et al. Tc-99m labelled bone scintigraphy in suspected cardiac amyloidosis. Eur Heart J [Internet], 2023, 44 (24), 2187-2198.
- Ioannou, A., Patel, R.K., Razvi, Y., Porcari, A., Massa, P., Knight, D. et al. Impact of Earlier Diagnosis in Cardiac ATTR Amyloidosis Over the Course of 20 Years. Circulation, 2022, 146 (22), 1657-1670.
- Pemberton, H.G., Collij, L.E., Heeman, F., Bollack, A., Shekari, M. Quantification of amyloid PET for future clinical use: a state-of-the-art review. Eur J Nucl Med Mol Imaging [Internet], 2022, 3508-3528.
- Gheysens, O., Treglia, G., Masri, A., Hyafil, F., Dorbala, S., Gheysens, O. Treatment response assessment in transthyretin - related cardiac amyloidosis : an emerging clinical indication of bone - seeking radiopharmaceuticals? Eur J Nucl Med Mol Imaging [Internet], 2024, 51 (3), 691-694.
- Kessler, L., Costa, F., Kersting, D., Jentzen, W., Weber, M., Lu, P. et al. Quantitative 99m TcDPDSPECT / CT assessment of cardiac amyloidosis. J Nucl Cardiol, 2023, 30 (1), 101-111.
- Fontana, M., Pica, S., Reant, P., Abdelgadir, A., Treibel, T.A., Banypersad, S.M. et al. Prognostic Value of Late Gadolinium Enhancement Cardiovascular Magnetic Resonance in Cardiac Amyloidosis. Circulation, 2015, 132 (16), 16-18.
- Fontana, M., Martinez-Naharro, A., Chacko, L., Rowczenio, D., Gilbertson, J.A., Whelan, C.J. et al. Reduction in CMR Derived Extracellular Volume With Patisiran Indicates Cardiac Amyloid Regression. JACC Cardiovasc Imaging, 2021, 14 (1), 189-199.
- Banypersad, S.M., Fontana, M., Maestrini, V., Sado, D.M., Captur, G., Petrie, A. et al. T1 mapping and survival in systemic light-chain amyloidosis. Eur Heart J, 2015, 36 (4), 244-251.
- Wisniowski, B., Lachmann, H., Wechelakar, A., Whelan, C., Kellman, P. Multi-Imaging Characterization of Cardiac Phenotype in Different Types of Amyloidosis. Jacc Cardiovasc Imaging, 2023, 16 (4), 464-477.
- Gama, F., Rosmini, S., Bandula, S., Patel, K.P., Massa, P., Tobon-Gomez, C. et al. Extracellular Volume Fraction by Computed Tomography Predicts Long-Term Prognosis Among Patients With Cardiac Amyloidosis. JACC Cardiovasc Imaging [Internet], 2022, 15 (12), 2082-2094.
- Scully, P.R., Patel, K.P., Saberwal, B., Klotz, E., Augusto, J.B., Thornton, G.D. et al. Identifying Cardiac Amyloid in Aortic Stenosis: ECV Quantification by CT in TAVR Patients. JACC Cardiovasc Imaging [Internet], 2020, 13 (10), 2177-2189.
Niets van de website mag gebruikt worden voor reproductie, aanpassing, verspreiding, verkoop, publicatie of commerciële doeleinden zonder voorafgaande schriftelijke toestemming van de uitgever. Het is ook verboden om deze informatie elektronisch op te slaan of te gebruiken voor onwettige doeleinden.