Compte rendu du congrès du BeHRA
Dans le cadre du 16e Belgian Heart Rhythm Meeting, une session concernant le futur du pacing était proposée afin de parcourir les nouvelles modalités et possibilités concernant la stimulation cardiaque. Les thématiques abordées étaient la thérapie de resynchronisation par Francesco Leyva (Londres, RU), le pacing du tissu de conduction par Cynthia Brabaud (Liège, Belgique), le pacing sans sonde par Christophe Garweg (Louvain, Belgique), et enfin un résumé des dernières recommandations de l'European Society of Cardiology concernant la stimulation cardiaque édité en 2021.
Le premier orateur, Francesco Leyva (Londres, RU), rappelait d'emblée que l'un des objectif clés de la thérapie de resynchronisation est la conduction intraventriculaire la plus rapide possible à travers le myocarde sain. Ceci est représenté par la mesure électrique clinique la plus simple, à savoir la réduction de la durée du QRS, le but ultime étant d'obtenir le QRS le plus proche du QRS natif. Ensuite, l'orateur nous a fait part d'une comparaison entre le his bundle pacing (HBP) et la thérapie de resynchronisation (CRT) en termes de succès d'implantation. Dans l'étude RAFT, les taux de succès d'implantation des CRT étaient de 91 % au premier essai et 96,3 % après moins de 3 essais. Le problème le plus fréquent étant la migration de sondes imposant une nouvelle intervention. Afin d'éviter cet écueil, en particulier pour la sonde gauche, on peut proposer des fixations actives avec une nette réduction des migrations. Concernant le HBP, les taux de succès dans les centres avec une grande expertise sont moindres (environ 80 % avec certaines études dont certaines études ne comptent que peu de patients). Cela est dû à la difficulté liée au placement de la sonde au meilleur endroit possible pour la stimulation.
Le point suivant concernait la resynchronisation du patient insuffisant cardiaque avec bloc de branche gauche complet via HBP. Pour illustrer son propos, l'orateur cite l'étude publiée par W. Huang en 2022 qui rapporte 74 patients inclus avec une indication de resynchronisation (dont une majorité de cardiopathies non ischémiques). De cette cohorte, 75 % des patients ont bénéficié d'HBP avec succès (pacing sélectif, du tissu de conduction, dans 56 % des cas). Cependant, 20 % des patients sont devenus pacemaker dépendants (ce qui est potentiellement lié aux lésions induites par la procédure en elle-même) avec un point d'attention sur l'augmentation statistiquement significative et importante des seuils de stimulation à 12 mois.1
Actant ces différents problèmes lié au pacing hissien (dans le cadre de la resynchronisation ou non), une technique plus prometteuse est le pacing de la branche gauche (ou LBBaP).
En effet, les taux de succès d'implantation sont plus importants que le HBP (72 % vs. 94 % dans la littérature). Pour exemplifier ce propos, l'orateur a évoqué les premiers résultats d'essai pilote LBBP-RESYNC comptant 41 patients présentant une cardiopathie non-ischémique (CMNI) en rythme sinusal avec un bloc de branche gauche complet. Ces patients ont été randomisés en 1/1 dans un groupe CRT classique (taux de succès d'implantation de 80 %) ou un groupe CRT-LBBaP (taux de succès d'implantation de 90 %). En comparant ces deux groupes, une différence semble se dégager en termes de récupération de la fonction ventriculaire gauche (p = 0,039 en faveur du LBBaP) ainsi que sur la réduction du diamètre télédiastolique ventriculaire gauche, cela étant à confirmer par de nouvelles études.
Par contre, une limitation du LBBaP-CRT est le manque d'activation de la paroi latérale ventriculaire gauche d'où l'idée d'une approche combinant le LBBaP et une sonde gauche conventionnelle, appelée Left-Optimized Therapy - CRT ou LOT-CRT. Plusieurs études sur cette approche ont été publiées dont une évoquée lors du congrès.2 Ceci pourrait être une approche réservée aux patients les plus malades.
Le deuxième orateur, Cynthia Barbaud (Liège, Belgique), a présenté les nouvelles alternatives au pacing traditionnel et à la CRT, à savoir le pacing des voies de conduction (CSP), qui comprend le pacing hissien (HBP) et le pacing de la région de la branche gauche (LBBaP).
Il a été rappelé que les cardiomyopathies induites par le pacing conventionnel sont l'une des complications liées à la technique. La prévalence de cette dernière peut varier de 5 à 20 % des patients, surtout chez ceux avec une altération préexistante de fonction VG et un pourcentage important de pacing ventriculaire. Elle est associée à une mortalité accrue ainsi qu'à une augmentation du nombre d'hospitalisations pour insuffisance cardiaque.
Concernant le HBP, un des avantages évoqués à ce stade est illustré par une étude publiée par P. Vijayaraman en 20183 montrant que le pacing du his est statistiquement associé à moins de cardiopathies induites par le pacing ainsi qu'une réduction d'évènements cardiovasculaires (morts, hospitalisation pour insuffisance cardiaque ou upgrade vers un CRT) comparé au pacing ventriculaire droit (sur un suivi de 5 ans). C'est surtout le cas pour les patients nécessitant un pacing ventriculaire supérieur à 20 %.
Un autre avantage de cette technique est que, sachant que la majorité des blocs atrio-ventriculaires surviennent en intra-hissien, ces derniers peuvent être corrigés par HBP, soit par la majoration des seuils de stimulation ou en stimulant en aval du bloc afin de capturer des régions plus distales de faisceau. Cette propriété étant due à la dissociation longitudinale du faisceau de His, rappelle l'oratrice (figure 1).
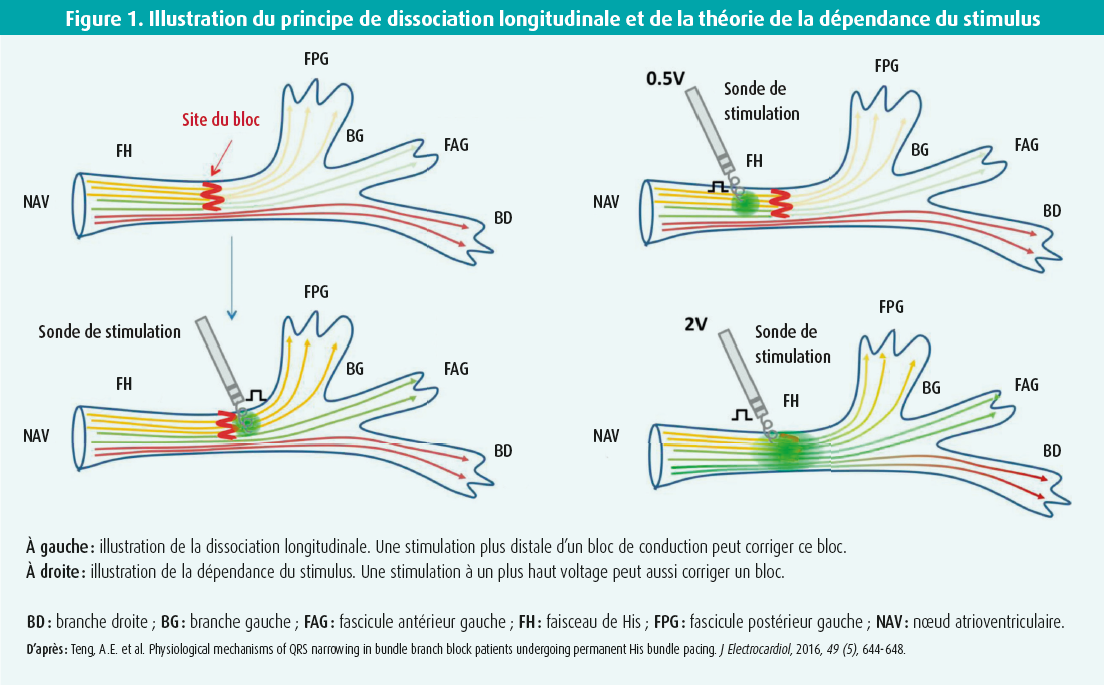
En outre, par comparaison avec la resynchronisation conventionnelle, la resynchronisation via HBP est, dans l'étude publiée en 2021 par M. Vinther1 et comptant 50 patients suivis durant 6 mois, plus efficace qu'un CRT conventionnelle sur la réduction de durée du QRS, la classe fonctionnelle NYHA, l'amélioration de FEVG et la réduction du diamètre télésystolique VG, cela devant être reproduit par des études plus robustes sur le plan statistique.
Malgré tout, cela explique, en partie, l'adaptation des guidelines de l'American Heart Association de 2018 qui recommande le HBP en classe IIA chez les patients en insuffisance cardiaque avec fonction systolique gauche altérée (HFrEF) en bloc AV, ou chez le patient nécessitant un pacing ventriculaire important.
Tous ces espoirs sont cependant pondérés par les limitations du HBP. Parmi ces limitations, l'oratrice cite le taux de succès d'implantation moindre, même s'il augmente avec l'expérience, les seuils de stimulation importants et se majorant progressivement durant le suivi, imposant un repositionnement de sonde (5 à 11 % des cas) avec des conséquences sur la longévité de la batterie du device, des EGM de plus faible amplitude pouvant gêner l'interrogation/le suivi du device.
Au vu de cela, une autre technique plus prometteuse est avancée, à savoir le LBBaP. Plusieurs avantages de cette technique en comparaison au HBP sont notés par l'oratrice : un taux de succès d'implantation de LBBaP plus important dans les études vérifiées dans la pratique courante par l'étude MELOS (Multicenter European Left bundle branch area pacing Outcome Study), une stabilité des seuils de stimulation plus importante et un meilleur sensing des évènements ventriculaires.
Comme pour toute technique, des échecs d'implantation sont constatés. Ceux-ci sont en majorité liés à l'impossibilité de traverser le septum interventriculaire (SIV) pour quelque raison que ce soit, la cause principale étant une éventuelle cicatrice d'infarctus. Notons que les complications toutes gravités confondues sont peu fréquentes dans la pratique courante (environ 6-8 %) comme nous enseigne l'étude MELOS. Parmis les complications les plus relevantes en pratique, nous notons les perforation ventriculaires gauches (comptant pour 3,7 % des complications totales) les migrations de sondes (1,5 %), les syndromes coronariens aigus (SCA) (0,4 %), …
Le troisième orateur, Christophe Garweg (Louvain, Belgique) a, quant à lui, retracé le développement du pacemaker sans sonde ainsi que les avancées de cette technique.
Malgré une expérience importante en matière de technique de stimulation et d'implantation, on estime entre 10 et 15 % les complications liées à l'implantation de devices voire 20 % dans le cas d'un suivi sur 5 ans. Les complications liées au matériel transveineux sont nombreuses et variées : les limitations liées à l'accès veineux, les problèmes de sondes (migration, régurgitations tricuspidiennes, syndrome de Twiddler …), les problèmes liés à la logette (hématomes et infections du site). C'est dans ce contexte que le pacing sans sonde s'est développé comme alternative.
Micra TPS VR : un point sur 10 ans d'évolution
Cela fait actuellement 10 ans d'évolution/ d'expérience clinique avec ce device. La première étude, datant de 2015-2016 et portant sur 726 candidats implantés dans des centres sélectionnés, montre un taux de succès d'implantation de 99,2 % et un taux de complications de 4 % à 12 mois (soit 48 % de complications en moins comparé à une implantation classique).5
Des nouvelles données publiées en 2018 sur une cohorte de 1 817 patients montrent des résultats similaires voire légèrement meilleurs.6
Les dernières données publiées à ce sujet datent de 20217 et comparent un leadless pacemaker (N = 6 219) à un pacemaker simple chambre VVI (N = 10 212) dont la population est issue des mêmes centres et ces 2 populations ont été comparées sur une durée de 2 ans. Plusieurs outcome ont été observés (avec un facteur de correction statistique pour tenter de limiter le manque de randomisation). Les complications à 30 jours étaient similaires dans les 2 groupes, les effusions cardiaques/ perforations étaient plus importantes dans le groupe leadless. À deux ans, le taux de complications globales dans le groupe leadless est moindre que dans le groupe transveineux (P < 0,0001). Autre donnée intéressante, le groupe leadless était associé avec un taux de réintervention moindre et un taux de complication moindre sans différence sur la mortalité de toutes causes ajustées à 2 ans. Concernant la mortalité non ajustée, elle était plus importante dans le groupe leadless, ceci pouvant s'expliquer par une population plus malade et présentant plus de comorbidités.
Un autre point intéressant sur ces 10 dernières années concerne les infections systémiques et les device leadless. Un essai et un registre (IDE trial [21 événements sur 16 patients, N = 720, follow-up de 17 mois] et PAR registry [3 événements sur 3 patients, N = 1801, follow-up de 6,8 mois]) montrent qu'il y a peu d'événements infectieux chez ces patients. Respectivement 2 décès sont associés à une endocardite de la valve aortique dans le premier papier et 100 % des événements recensés sont traités par antibiotiques sans décès dans le registre.
Micra VR : le futur
L'orateur a évoqué ici le Micra TPS AV, évolution du Micra TPS VR fonctionnant selon un mode VDD. Ce dernier fonctionne avec un logiciel permettant de reconstituer un sensing atrial mécanique. Sur la base d'un accéléromètre, le device reconnaît 4 temps appelés A1 (correspondant au début de la systole ventriculaire), A2 (correspondant à la fin de la systole ventriculaire), A3 (correspondant à l'onde E échocardiographique et donc au remplissage ventriculaire passif) et A4 (correspondant au remplissage ventriculaire actif, et donc à l'onde A à l'échographie Doppler). C'est ce dernier événement qui va être perçu et interprété par le device.
L'histoire de ce device a débuté parallèlement à celle du Micra VR, c'est-à-dire en 2015. Parmi l'historique de ce device, l'étude MARVEL 2 était une étude de faisabilité afin d'évaluer l'efficacité et la sureté d'un tel device au repos durant 30 minutes avec un tel logiciel. Cette étude confirmera l'efficacité et la sûreté du device malgré les limites liées à la petite taille de l'échantillon. Une autre donnée importante rapportée par l'étude MARVEL 2 est la bonne corrélation entre un synchronisme AV réel et le synchronisme perçu par le device (marqué par l'acronyme AM-VP lors de l'interrogation du device).
On présente alors les premiers résultats de l'étude ACCEL AV. Son but est d'étudier, en ambulatoire, le synchronisme AV lors du fonctionnement du Micra AV. Il s'agit d'une étude prospective non randomisée multicentrique (États-Unis et Hong Kong) incluant 152 patients implantés avec un Micra AV dont 54 présentaient au moment de l'inclusion un rythme sinusal et un bloc AV complet.
Ce qui a été recherché/ observé durant cette étude :
- Un bon synchronisme AV (ou AVS) au repos à 1 et 3 mois. Seuls 2 patients ont présenté une chute du AVS liée à une mauvaise stratégie de programmation ;
- Recherche de corrélation entre qualité de vie et AVS ; une corrélation entre le débit cardiaque évalué à l'échocardiographie et la qualité de vie a été observée de même qu'un passage du mode VVI au mode VDD permet une augmentation du débit cardiaque. Il est noté une augmentation de la qualité de vie du suivi mais, fait intéressant, le taux de synchronisme AV ne présente pas de corrélation avec la qualité de vie.
Leadless pacing à deux chambres : le mythe devient réalité
Dans ce volet, l'orateur a présenté le système AVEIR (atrial leadless pacemaker) et l'étude préclinique d'évaluation de la sécurité et du fonctionnement du device sur 10 espèces ovines sur une durée de 12 semaines. Le device comporte 2 boîtiers distincts : un ventriculaire et un autre qui est implanté dans l'auricule droit et communiquant par un système qui s'apparente au Bluetooth. Des améliorations liées aux matériaux utilisés dans la fabrication du device permettent d'obtenir une diminution de la fibrose de la zone de contact, ce qui assure un meilleur contact avec le tissu et une meilleure efficacité électrique, et se traduisant par une diminution des seuils de stimulation et une augmentation du sensing.
L'étude AVEIR est encore en cours (multicentrique prospective, un seul bras) et s'intéresse à la sûreté et à l'efficacité d'un tel protocole en mode DDD(R). Le premier humain dans le cadre de cette étude a été implanté en février 2022. Le premier patient belge a été implanté à Leuven en juillet 2022.
Le but du device sera d'obtenir un synchronisme parfait, battement par battement, entre l'oreillette droite et le ventricule droit.
Enfin, le dernier orateur était Michael Glikson (Jérusalem, Israël) est retourné vers les nouvelles guidelines de l'ESC de 2021 concernant le pacing. De nouveaux sujets ont été implémentés dans l'édition de 2021. L'orateur souligne certains d'entre eux (figure 2).
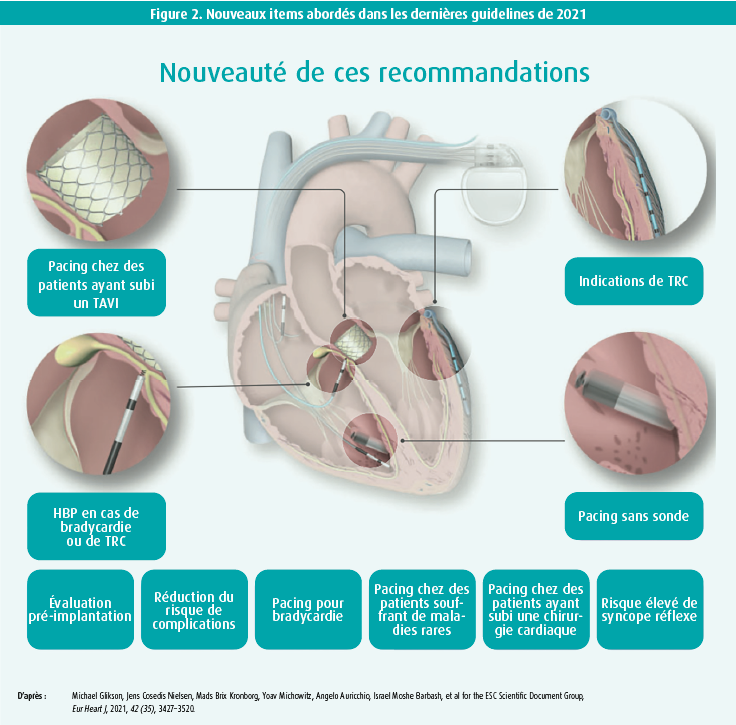
Evaluation du patient avant implantation (y compris l'imagerie et testing génétique)
Il est toujours recommandé en classe I de pratiquer des tests d'effort aux patients ayant ressenti des symptômes évocateurs de bradycardie lors d'un effort ou immédiatement après l'effort. Chez les patients avec un trouble de la conduction intraventriculaire ou un BAV de degré inconnu, l'épreuve d'effort peut être considérée en classe IIB pour démontrer un bloc intranodal. La recherche d'apnée du sommeil chez les patients présentant des bradycardies extrêmes ou BAV durant le sommeil est recommandée en classe 1.
L'imagerie cardiaque est recommandée chez les patients avec bradycardies symptomatiques afin de rechercher une maladie structurelle, de déterminer la FEVG et diagnostiquer de potentiels troubles conductifs (classe 1). L'imagerie multimodale devrait être considérée afin de caractériser le tissu myocardique en particulier dans les pathologies associées à des troubles de la conduction et pour lesquelles un pacing est indiqué (chez les patients de moins de 60 ans [classe 2A]).
Un testing génétique devrait être considéré chez les patients présentant des formes précoces de maladie touchant le tissu de conduction (classe 2A).
Le patient syncopal
Un nouvel algorithme décisionnel a été présenté à ce sujet. Si un patient victime de syncopes inexpliquées présente un bloc fasciculaire et une fonction systolique gauche (< 35 %), un ICD/CRT-D est indiqué. Si la fonction gauche est > à 35 % une évaluation plus approfondie du patient est nécessaire.
Si le patient est fragile ou âgé avec un haut risque de récidive, un pacemaker est indiqué ; dans le cas contraire, une étude électrophysiologique serait indiquée. Si celle-ci est positive, une thérapie appropriée est indiquée et si non, un enregistreur d'évènements implantable serait indiqué plutôt qu'un pacemaker.
Un résumé des indications de pacing chez le patient de plus de 40 ans présentant une syncope reflexe a aussi été exposé.
Si une pause sans systole spontanée a été observée , qu'elle soit symptomatique de plus de 3 secondes ou asymptomatique de plus de 6 secondes, un pacing est indiqué en classe 1. S'il n'y a pas de pauses spontanées, un test d'inclinaison (tilt-test) ou un test à l'adénosine sera proposé. Si ce test est positif, alors un le pacing est alors indiqué en classe 1. Si un bloc AV de plus de 10 secondes est induit au test à l'adénosine, le pacing est indiqué en classe 2B. En l'absence de syncope ou de test d'induction +, le pacing n'est pas indiqué (classe 3).
Les thérapies de resynchronisation chez le patient en rythme sinusal et en fibrillation atriale
En ce qui concerne les thérapies de resynchronisation, seuls quelques changements mineurs avec un alignement sur les dernières guidelines de la prise en charge de l'insuffisance cardiaque ont été réalisés. Le CRT dans le cadre de la FA avec insuffisance cardiaque n'est recommandé qu'en classe NYHA III-IV avec un QRS > à 130 ms qu'importe le pattern de bloc de branche. Chez le patient en bloc AV avec indication de pacing, le CRT est recommandé en cas de fonction gauche < à 40 % et un taux de VP > à 20 % (sans lien avec la fréquence cardiaque). En cas d'ablation du noeud AV, le CRT est recommandé si la fonction VG est < à 50 %. Cela est principalement dû au fait qu'il s'agit d'une iatrogénie volontaire.
Concernant les indications d'ablation du noeud AV chez les patients en FA consacrée ; si le rythme est contrôlé et que le patient est candidat à un CRT (fonction réduite à 35 %, QRS > à 130 ms et NYHA > III), alors l'indication est retenue dès lors qu'un taux de stimulation biventriculaire compris entre 95 et 100 % peut être obtenu. Si ce taux de stimulation n'est pas atteint, alors une ablation peut être proposée en classe 2A). Si le rythme n'est pas contrôlé, que la FA est considérée comme consacrée et que l'ablation du noeud est retenue ;
- Dès lors que la fonction est > à 50 %, un pacing ventriculaire droit est indiqué en classe 2A, un CRT/HBP en classe 2B) ;
- Si la fonction est < à 50 %, un CRT est indiqué en classe 1.
Dès lors que l'indication d'un CRT est posée, la décision entre CRT-P ou CRT- D peut être complexe. Il n'a pas été décidé de cut-off clair mais plutôt une clarification des grandes lignes directrices. Par exemple, la présence de fibrose myocardique sera un argument penchant vers le CRT-D et l'âge avancé vers le CRT-P. D'autres facteurs feront pencher la balance vers un CRT-P tels qu'une cardiopathie non-ischémique, une espérance de vie peu importante, d'importantes comorbidités, … (figure 3).

Autres modalités de pacing (HBP, LBBaP, leadless pacing)
Quant aux les autres modalités de pacing, le HBP-CRT est recommandé en classe 2A chez les patients pour lesquels une sonde gauche conventionnelle n'a pu être implantée. Cette option peut être considérée au même titre qu'une sonde épicardique. S'il y a décision d'un HBP, alors une sonde ventriculaire droite de backup sera considérée en classe 2A. Chez les patients pour lesquels une stratégie « pace and ablate » en cas d'arythmie supraventriculaire rapide a été retenue, le HBP peut être considéré en classe 2B.
Comme précisé ci-dessus, les leadless devices peuvent être considérés comme alternatives dans certains cas en classe 2A.
Il a été rappelé que l'implantation d'un pacemaker définitif en cas d'infarctus et de bloc AV est recommandée en classe 1 dès lors que le bloc AV persiste après 5 jours. Chez certains patients avec BAV suite à un infarctus antérieur ou insuffisance cardiaque aiguë, l'implantation dans des délais plus rapides d'un CRT peut être considérée en classe 2B.
En cas de bloc AV complet concomitamment à une chirurgie cardiaque, une période d'observation de minimum 5 jours afin d'évaluer le trouble est indiqué en classe 1. Évidemment si les chances de récupération sont jugées faibles ou en l'absence de rythme d'échappement, cette période sera raccourcie. L'indication de pacemaker en cas de chirurgie cardiaque et de dysfonction sinusale sera soumise à une période d'attente de 6 semaines en classe 2A.
L'implantation d'une sonde épicardique sera considérée en classe 2A chez les patients devant bénéficier d'une chirurgie valvulaire liée à une endocardite et en présence d'un BAV complet si une de ces conditions est observée : anomalie de la conduction préopératoire, infection à S. doré, abcès intracardiaque, implication de la tricuspide ou antécédent de chirurgie valvulaire.
Management des troubles conductifs per et post-TAVI
Pour conclure l'exposé, l'orateur a précisé quelques recommandations liées aux troubles de la conduction per et post-TAVI. En cas de survenue d'un bloc AV de haut degré ou d'un bloc alternant, l'implantation d'un pacemaker est indiquée en classe I. En cas de bloc droit préexistant, dès lors qu'un trouble de la conduction nouveau est observé, l'implantation d'un pacemaker doit être considérée en classe II a. En cas de survenue d'un bloc gauche avec un élargissement du QRS > 150 ms, d'un allongement de l'intervalle PR > 240 ms non progressif endéans 48 h, une étude électrophysiologique entre autres afin d'étudier le tissu conductif du patient ou un recontrôle de l'ECG à 7-30 jours en ambulatoire est indiquée en classe IIa.
Enfin, il est recommandé en classe II b dès lors qu'une anomalie de la conduction préexistante est connue et associée à un élargissement du QRS ou un allongement de l'intervalle PR > 20 ms per ou post-procédure (48 h) de réaliser un contrôle ambulatoire d'ECG à 7-30 jours ou de procéder à la réalisation d'une étude électrophysiologique afin de caractériser la conduction du patient, en particulier la mesure du délai HV.
Referenties
- Lustgarten, D.L., Crespo, E.M., Arknipova- Jenkins, I., Lobel, R., Winget, J., Koehler, J., Liberman, E. et al. His-bundle pacing versus biventricular pacing in cardiac resynchronization therapy patients: A crossover design comparison, Heart Rhythm, 2015, 12 (7), 1548-1557.
- Jastrzebski, M., Moskal, P., Huybrechts, W., Curila, K., Sreekumar, P., Rademakers, L.M., Ponnusamy, S.S. et al, Left bundle branchoptimized cardiac resynchronization therapy (LOT-CRT): Results from an international LBBAP collaborative study group, Heart Rhythm, 2022, 19 (1), 13-21.
- Vijayaraman, P. Chung, M.K., Dandamudi, G., Upadhyay, G.A., Krishnan, K., Crossley, G. et al. His Bundle Pacing. J Am Coll Cardiol, 2018, 72 (8), 927-947.
- Vinter, M., Risum, N., Svendsen J.H., Møgelvang, R., Philbert, B.T. et al. A Randomized Trial of His Pacing Versus Biventricular Pacing in Symptomatic HF Patients With Left Bundle Branch Block (His-Alternative). J Am Coll Cardiol, 2021, 7 (11), 1422-1432.
- Reynolds, D., Duray, G.Z., Omar, R., Soejima, K., Neuzil, P., Zhang, S., Narasimhan, C. et al. for the MICRA Transcatheter Pacing Study Group. A Leadless Intracardiac Transcatheter Pacing System February 11, 2016, N Engl J Med, 2016, 374 (6), 533-541.
- El-Chami, M.F., Al-Samadi, F., Clementy, N., Garweg, C., Martinez-Sande, J.L., Piccini, J.P. et al. Updated performance of the Micra transcatheter pacemaker in the real-world setting: A comparison to the investigational study and a transvenous historical control, Heart rhythm, 2018, 15 (12), 1800-1807.
- El-Chami, M.F., Bockstedt, L., Longarce, C., Higuera, L., Stromberg, K., Crossley, G., Kowal, R.C. et al., Leadless vs. transvenous single-chamber ventricular pacing in the Micra CED study: 2-year follow-up, Eur Heart J, 2022, 43 (12), 1207-1215.
Niets van de website mag gebruikt worden voor reproductie, aanpassing, verspreiding, verkoop, publicatie of commerciële doeleinden zonder voorafgaande schriftelijke toestemming van de uitgever. Het is ook verboden om deze informatie elektronisch op te slaan of te gebruiken voor onwettige doeleinden.