Pro-Con-sessie op het BIWAC-symposium van vrijdag 3 juni 2016
Op vrijdag 3 juni 2016 organiseerde de Belgische Interdisciplinaire Werkgroep voor Acute Cardiologie (BIWAC) voor de vijfde maal haar tweejaarlijkse symposium. In de ochtend was er een pro-contradebat over 'pretreatment with P2Y12 blocking agent in every ACS?'.
De term pretreatment verwijst naar het tijdig toedienen van een P2Y12-blokker voor coronarografie (CAG) zodat op het moment van de percutane coronaire interventie (PCI) er een maximale inhibitie is van de bloedplaatjesaggregatie. Pretreatment kan gebeuren in de ambulance (preziekenhuis), op de spoeddienst, in de coronaire eenheid (CCU) of in het cathlab vóór de invasieve procedure, maar niet onmiddellijk voor PCI.
Het lijkt evident dat oplading met een krachtige P2Y12-blokker voor CAG het risico op trombotische verwikkelingen tijdens een PCI zal verminderen. Dit is des te belangrijker bij patiënten met een acuut coronair syndroom (ACS) bij wie de bloedplaatjes al sterk geactiveerd zijn en bij wie er sprake is van instabiele, geruptureerde plaques met trombusvorming in de coronaire circulatie. Bovendien worden bloedplaatjes nog extra geactiveerd door intracoronaire manipulaties tijdens de PCI-procedure.
Maar er zijn ook nadelen aan de pretreatmentstrategie, zoals een hoger bloedingsrisico, vooral bij femorale PCI-procedures of in geval van urgente chirurgische revascularisatie (CABG), of de verlenging van hospitalisatieduur in geval van electieve CABG voor preoperatieve monitoring en wash-out van de P2Y12- blokker. Om dan nog niet te spreken over pretreatment bij patiënten met acute thoracale pijn bij wie verkeerdelijk de diagnose van ACS gesteld werd.
Welke wetenschappelijke argumenten zijn er om alle ACS-patiënten systematisch op te laden met een P2Y12-blokker vóór CAG? De farmacologische eigenschappen van de vier beschikbare P2Y12- blokkers worden samengevat in tabel 1.
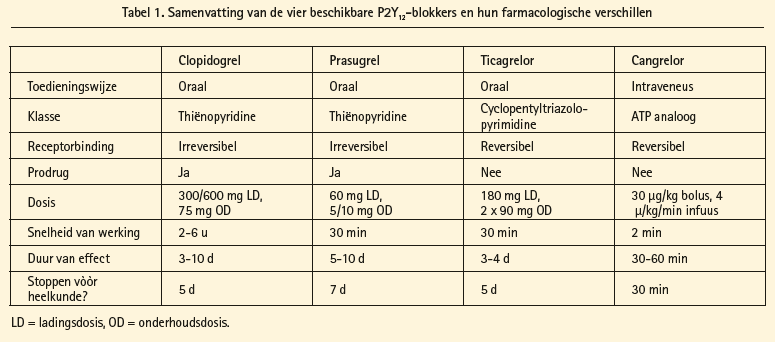
Clopidogrel
Clopidogrel is een prodrug dat in vivo bioactivatie moet ondergaan en dat een eerder trage werking heeft. Na een oplaaddosis van 600 mg duurt het nog minstens 2 uur voor een optimale inhibitie van de bloedplaatjesaggregatie. Dit interval kan niet ingekort worden door de oplaaddosis te verhogen van 600 mg naar 900 mg.1 Pretreatment lijkt op basis van het farmacologisch profiel van clopidogrel logisch en zinvol.
Verrassend is dan ook dat er geen verschil gezien wordt in overlijden en ischemische gebeurtenissen tussen pretreatment en 'in-lab' oplading met clopidogrel, na de CAG, in twee gerandomiseerde studies, PRAGUE-8 en ARMYDA-5.2, 3
Deze bevindingen worden bevestigd in de ACTION Study Group-meta-analyse met clopidogrel en prasugrel. Er is geen verschil in mortaliteit (odds ratio: 0,90; p = 0,24) maar wel een significante toename met 30-45 % van het aantal majeure bloedingen (odds ratio: 1,32; p < 0,0001) met een pretreatmentstrategie. 4, 5
Prasugrel
Prasugrel is, zoals clopidogrel, ook een thiënopyridine prodrug, maar dan met een snelle werking waardoor een optimale inhibitie van de bloedplaatjesaggregatie al binnen 30 minuten na de oplaaddosis verkregen wordt. Hierdoor is het voordeel van pretreatment minder duidelijk. Bovendien was er in het TRITON-TIMI 38-studieprotocol met prasugrel 60/10 mg versus clopidogrel 300/75 mg geen pretreatment voorzien. Patiënten met NSTEMI en ook 68 % van de STEMI-patiënten kregen de oplading met studiemedicijn pas na CAG, onmiddellijk vóór of zelfs na PCI.6, 7 Vandaar dat er een aparte gerandomiseerde studie met prasugrel werd opgezet om het belang van pretreatment na te gaan. In de ACCOAST-trial werden 4 033 patiënten met NSTEMI gerandomiseerd tussen 30 mg prasugrel voor CAG (pretreatmentgroep) of placebo (controlegroep). In geval van PCI, volgens het protocol binnen 2 tot 48 uur, met een mediaan van 4,3 uur, werd nog eens 30 mg prasugrel gegeven in de pretreatmentgroep of 60 mg prasugrel in de controlegroep. De studie moest vroegtijdig stopgezet worden vanwege een verdubbeling van het aantal majeure bloedingen in de pretreatmentgroep (van 1,4 % naar 2,6 %, odds ratio 1,90; p = 0,006) zonder dat er een verschil was in het primair samengesteld eindpunt van cardiovasculaire mortaliteit, myocardinfarct, CVA, urgente revascularisatie of 'bail-out' toediening van een glycoproteïne IIbIIIa-blokker (odds ratio 1,02; p = 0,81). De incidentie van majeure en levensbedreigende bloedingen, niet gerelateerd aan coronaire heelkunde, steeg met een factor 3 en 6, respectievelijk.8
In een farmacodynamische substudie van de ACCOAST-trial ziet men dat de bloedplaatjesinhibitie op het moment van PCI groter is in de pretreatmentgroep, wat de hogere bloedingsincidentie zou kunnen verklaren. De meeste PCI-procedures gebeurden immers via een femoraal acces. Maar twee uur later was er al geen verschil meer in bloedplaatjesinhibitie tussen beide groepen. Dit maakt het moeilijk om nog een verschil in trombotische complicaties aan te tonen.
Door ACCOAST en andere data is pretreatment met prasugrel bij NSTE-ACS-patiënten definitief verbannen. Voorlopig blijft het een open vraag of deze stelling ook kan uitgebreid worden naar de andere, nieuwe P2Y12-blokkers, ticagrelor en cangrelor, en naar STEMI-patiënten.
Een head-to-headvergelijking tussen prasugrel en ticagrelor, pretreatment versus 'in-lab'-oplading zowel bij NSTE-ACS als bij STEMI wordt momenteel onderzocht in de ISAR-REACT 5-studie, waarvan de rekrutering startte in september 2013.9 Een uitdagende hypothese, nl. de superioriteit van pretreatment met ticagrelor tegenover 'in-lab treatment' met prasugrel wordt onderzocht bij 4 000 invasief behandelde ACS-patiënten.
Ticagrelor
Ticagrelor is een orale en krachtige P2Y12-blokker. In vergelijking met clopidogrel en prasugrel is het een compleet andere molecule. Het is een directe en reversibele blokker van de P2Y12-receptor die voor zijn werking niet gemetaboliseerd moet worden. Nochtans is ook het belangrijkste metaboliet van ticagrelor farmacologisch actief. Zoals prasugrel, is ticagrelor ook een snel werkend product met een piekeffect vanaf 30 minuten na oplading van 180 mg.
In de PLATO-trial wordt ticagrelor vergeleken met clopidogrel bij 18 624 'all-commers' ACS-patiënten. Ticagrelor vermindert het risico op ischemische gebeurtenissen (gecombineerd primair eindpunt van cardiovasculair overlijden, myocardinfarct en CVA; hazard ratio: 0,84; p < 0,001) zonder toename van de majeure bloedingscomplicaties (hazard ratio: 1,03; p = 0,57). Er was wel een toename van de majeure bloedingen, niet gerelateerd aan CABG, in de ticagrelorgroep (hazard ratio: 1,25; p = 0,03).10
PLATO was geen studie die pretreatment vergeleek met 'in-lab treatment'. Alle patiënten kregen het studiemedicijn vóór de invasieve procedure. 81 % van de populatie onderging een CAG, 64 % een PCI en 10 % CABG.
De meeste patiënten in de PLATO-studie kregen een eigentijdse, snel invasieve aanpak. In de ticagrelorgroep was de mediane duur vanaf de toediening van het studiemedicijn tot PCI 15 min bij STEMI en 3u 54 min bij NSTEMI. Op basis van de PLATO-studieresultaten, is ticagrelor de voorkeursbehandeling voor alle patiënten met ACS, ongeacht de behandelingsstrategie, zelfs wanneer de patiënten al voorbehandeld werden met clopidogrel (klasse I, LOE B).
De waarde van pretreatment met ticagrelor werd onderzocht in de ATLANTIC-studie die prehospitaal pretreatment met ticagrelor vergeleek met 'in-lab treatment' bij 1 862 patiënten met STEMI, gepland voor primaire PCI.11 De studie was niet gepowered om superioriteit van pretreatment aan te tonen op klinische eindpunten. Vandaar dat er twee surrogaateindpunten gekozen werden, nl. afwezigheid van ≥ 70 % resolutie van ST-segmentelevatie op ecg en TIMI-flow < 3 in het infarctbloedvat juist voor PCI. Er kon geen verschil aangetoond worden tussen de pretreatment- en de 'in-lab treatment'-strategie, waarschijnlijk omdat het tijdsverschil tussen de toediening van ticagrelor in beide groepen zeer klein was, nl. een mediaan van 31 minuten. Bovendien blijkt er een significante interactie (Pint = 0,005) met het gebruik van morfine, waardoor de absorptie van ticagrelor in de pretreatmentgroep vertraagd werd. Dit wordt bevestigd in de IMPRESSION-trial, een dubbelblinde protocol van morfine vs. placebo bij STEMI-patiënten opgeladen met ticagrelor. Hierin zag men dat de opname van oraal toegediende ticagrelor met 36 % daalde bij gelijktijdig gebruik van morfine.12
Ten slotte was er in ATLANTIC een numeriek verschil in het aantal definitieve stenttromboses in het voordeel van pretreatment (2 in de pretreatment- vs. 11 in de 'in-lab treatment'-groep). Maar merkwaardig genoeg ging dit niet gepaard met minder overlijdens. Integendeel, de mortaliteit was numeriek groter in de pretreatmentgroep (30 in de pretreatmentgroep vs. 19 in 'in-lab treatment'-groep). Ook de som van het aantal definitieve en waarschijnlijke stenttromboses was niet verschillend in beide groepen (21 in pretreatment vs. 20 in in-lab treatment).
Hoewel pretreatment met ticagrelor veilig is en niet meer bloedingen geeft, is er bij STEMI-patiënten geen voordeel ten opzichte van de 'in-lab'-oplading tijdens PCI. Bovendien bleek 10 % van de patiënten in ATLANTIC geen revascularisatie gekregen te hebben omdat de prehospitaaldiagnose van STEMI onjuist was en het eigenlijk om een acuut thoracaal aortasyndroom ging, een aandoening waarbij de oplading met een P2Y12- blokker ernstige nadelen heeft.
Cangrelor
Cangrelor is de eerste intraveneuze P2Y12-blokker met een reversibele werking en een zeer kort halfleven van < 5 minuten. Het behoort tot de klasse van de ATP-analogen en heeft een snel en krachtig direct inhiberend effect op de P2Y12-receptor.
Cangrelor werd onderzocht in drie grote fase 3-studies, CHAMPION-PCI, CHAMPION-Platform en CHAMPION-PHOENIX. Hoewel de trials afzonderlijk grotendeels neutraal waren, blijkt uit een gepoolde meta-analyse (n = 24 910 patiënten) dat cangrelor de aan PCI gerelateerde trombotische complicaties vermindert, zowel bij electieve patiënten als bij ACS-patiënten, maar ten koste van een toename van (mineure) bloedingen.13 Het gebrek aan een effect in de individuele trials zou kunnen verklaard worden door de korte of zelfs afwezige transitie van cangrelor naar clopidogrel in de cangrelorarm van de trials, wanneer bovendien de relatief trage werking van clopidogrel en de competitie voor binding aan de P2Y12-receptor van beide geneesmiddelen in acht genomen worden.
Cangrelor werd tot op heden nog niet onderzocht in een pretreatmentstrategie maar zou hier een voordeel kunnen hebben ten opzichte van orale P2Y12-blokkers aangezien het binnen 5 minuten na stopzetting is uitgewerkt en hierdoor dringende heelkunde bij bv. een aortadissectie toelaat. Het kan ook gegeven worden aan bewusteloze patiënten die niet kunnen slikken of bij wie vanwege cardiogene shock of toediening van morfine de intestinale absorptie van geneesmiddelen verminderd is. Interessant om te weten is dat cangrelor de binding van clopidogrel en van prasugrel aan de P2Y12-receptor blokkeert, maar niet die van ticagrelor.
Het belangrijkste nadeel van cangrelor is de kostprijs van 350 EUR per vial. Eén vial is nodig voor een behandeling van 2 uur bij een patiënt < 100 kg.
Implicaties voor NSTE-ACS- en STEMI-guidelines
Aangezien alle gerandomiseerde trials over pretreatment negatief zijn, is routineuze pretreatment met een P2Y12-blokker bij NSTE-ACS- en STEMI-patiënten niet aangewezen.
De huidige 2015 ESC guidelines voor NSTE-ACS zijn al in die zin aangepast en doen geen aanbevelingen meer over de timing van toediening van clopidogrel en ticagrelor. Pretreatment met prasugrel wordt afgeraden. Prasugrel kan alleen gestart worden als de coronaire anatomie bekend is en in geval van PCI.
De ESC guidelines voor STEMI hebben de gegevens van meer recente studies zoals ATLANTIC nog niet geïmplementeerd en adviseren nog om de P2Y12-blokker te starten 'bij het eerste medische contact' of 'zo snel als mogelijk na de diagnose van STEMI' zonder te specificeren of dit in de ambulance, op de spoeddienst of in het cathlab moet zijn. Routineuze prehospitaal pretreatment met een P2Y12-blokker bij STEMI-patiënten kan nog moeilijk aanbevolen worden, zeker wanneer de diagnose onzeker is of de patiënt bewusteloos of in shock is. Een strategie waarbij een krachtige P2Y12-blokker, prasugrel of ticagrelor, gestart wordt in het ziekenhuis, op de spoeddienst of in het cathlab, eens de diagnose van STEMI bevestigd is en de patiënt een primaire PCI krijgt, lijkt momenteel de beste aanpak.14
Referenties
- von Beckerath, N. et al. Absorption, metabolization, and antiplatelet effects of 300, 600 and 900mg loadinhg doses of clopidogrel: results of the ISARCHOICE trial. Circulation, 2005, 112, 2946-2950.
- Widimsky, P. et al. Clopidogrel pre-treatment in stable angina: for all patients > 6h before elective coronary angiography or only for angiographically selected patients a few minutes before PCI? A randomized multicentre trial PRAGUE-8. Eur Heart J, 2008, 29, 1495-1503.
- Di Sciascio, G. et al. Effectiviness of in-laboratory high-dose clopidogrel loading versus routine preload in patients undergoing percutaneous coronary intervention: results of the ARMYDA-5 PRELOAD trial. J Am Coll Cardiol, 2010, 56, 550-557.
- Bellemain-Appaix, A. et al. for the ACTION group. Association of Clopidogrel Pretreatment with mortality, cardiovascular events and major bleeding among patients undergoing percutaneous coronary intervention. A systematic review and meta-analysis. JAMA, 2012, 308 (23), 2507-2517.
- Bellemain-Appaix, A. et al. for the ACTION group. Reappraisal of thienopyridine pretreatment in patients with non-ST elevation acute coronary syndrome: a systematic review and meta-analysis. BMJ, 2014, 349, g6269.
- Wiviott, S.D. et al. For the TRITON-TIMI 38 Investigators. Prasugrel versus Clopidogrel in patients with acute coronary syndromes. N Engl J Med, 2007, 357, 2001-2015.
- Montalescot, G. et al. Prasugrel compared with clopidogrel in patients undergoing percutaneous coronary intervention for ST-elevation myocardial infarction (TRITON-TIMI 38): double-blind, randomised controlled trial. Lancet, 2009, 373, 723-731.
- Montalescot, G. et al. for the ACCOAST Investigators. Pretreatment with prasugrel in non-ST-segment elevation acute coronary syndromes. N Engl J Med, 2013, 369, 999-1010.
- Schulz, S. et al. Randomized comparison of Ticagrelor versus Prasugrel in patients with acute coronary syndrome and planned invasive strategy-Design and rationale of the ISAR-REACT 5 trial. J Cardiovasc Trans Res, 2014, 7, 91-100.
- Wallentin, L. et al for the PLATO investigators. Ticagrelor versus clopidogrel in patients with acute coronary syndromes. N Engl J Med, 2009, 361, 1045-1057.
- Montalescot, G. et al. for the ATLANTIC Investigators. Prehospital ticagrelor in ST-segment elevation myocardial infarction. N Engl J Med, 2014, 371, 1016- 1027.
- Kubica, J. et al. Morphine delays and attenuates ticagrelor exposure and action in patients with myocardial infarction: the randomzed, double-blind, placebo-controlled IMPRESSION trial. Eur Heart J, 2016, 37, 245-252.
- Steg, P.G. et al. Effect of cangrelor on periprocedural outcomes in percutaneous coronary interventions: a pooled analysis of patient-level data. Lancet, 2013, 382, 1981-1992.
- Sibbing D, et al. Pretreatment with P2Y12 inhibitors in ACS patients: who, when, why, and which agent? Eur Heart J, 2015, 37 (16), 1284-1295.
Niets van de website mag gebruikt worden voor reproductie, aanpassing, verspreiding, verkoop, publicatie of commerciële doeleinden zonder voorafgaande schriftelijke toestemming van de uitgever. Het is ook verboden om deze informatie elektronisch op te slaan of te gebruiken voor onwettige doeleinden.