Inleiding
Sinds de eerste inplanting van een aortaklep in april 2002 door professor Alain Cribier in Rouen is het 'operatieve risico' een centraal gegeven in de discussie.
De werkzaamheid van TAVI (Transcatheter Aortic Valve Implantation) werd eerst aangetoond bij inoperabele patiënten (PARTNER 1B-studie, 2010): de overleving na 1 jaar was beter dan met een medische behandeling (sterfte respectievelijk 30,7 en 50,7 %, p < 0,001) en dat werd bevestigd na een follow-up van 2, 3 en 5 jaar1-4.
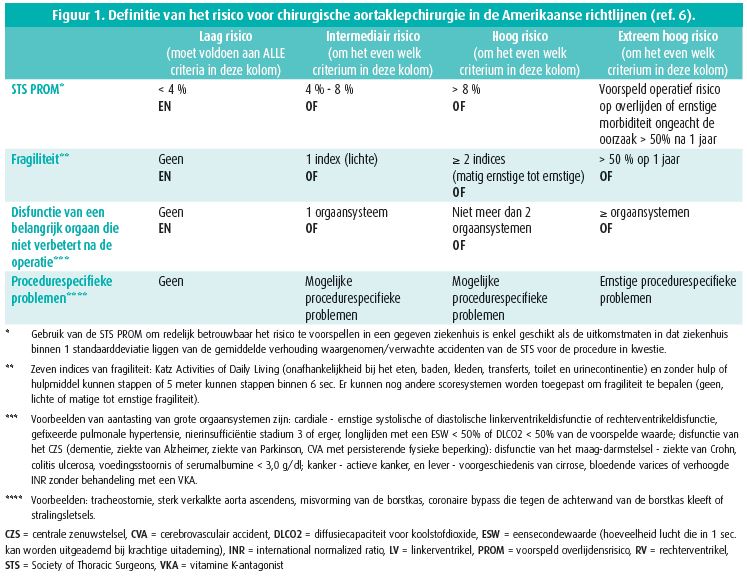
Er werd een nieuwe definitie van het operatieve risico gegeven in de Amerikaanse richtlijnen van 2014 (figuur 1) en daarna in de Europese richtlijnen (combinatie van STS-PROM, criteria van geriatrische fragiliteit en andere anatomische punten) 5, 6.
Twee non-inferioriteitsstudies hebben aangetoond dat de sterfte na 1 jaar, het primaire eindpunt, niet hoger was na TAVI (PARTNER 1A: 24,4 vs. 26,8 %) of zelfs lager was na TAVI (CoreValve US Pivotal Trial: 14,2 vs. 19,1 %) dan na klassieke aortaklepchirurgie bij patiënten met een hoog operatief risico. Die resultaten werden bevestigd bij een langere follow-up tot 5 jaar7-12.
Gezien die uitstekende resultaten werd TAVI ook geëvalueerd bij patiënten met een intermediair risico. In de studies PARTNER 2 en SURTAVI waren de sterfte en de incidentie van cerebrovasculair accident bij patiënten met een intermediair risico niet hoger na TAVI dan na chirurgie13, 14.
Tussen 2010, datum waarop de eerste gerandomiseerde studie werd gepubliceerd, en 2017, datum waarin de resultaten bij patiënten met een intermediair operatief risico werden gepubliceerd, heeft de TAVI-techniek een exponentiële ontwikkeling gekend: verschillende modellen van kleppen (ballon of zelfexpansie) en katheters om de klep af te leveren hebben een oplossing geboden voor de meeste technische problemen die zich in het begin hebben voorgedaan. Het aantal vaatcomplicaties is drastisch gedaald doordat de katheters die in de aorta worden ingebracht, smaller zijn geworden (van 24 French in 2002 tot 14 French met de laatste generaties). De nieuwe kunstkleppen bevatten een extern 'kraagje', wat een oplossing biedt voor het probleem van paravalvulaire lekken. Met een CT-scan van de aortaklep kan je vooraf de grootte, het type en de positionering van de prothese bepalen, waardoor er minder risico is op mismatch, ruptuur van de annulus en occlusie van een kransslagader. Die technische verbeteringen en de grotere ervaring van de interventionele teams verklaren de uitstekende resultaten die werden behaald in gerandomiseerde studies waarin TAVI werd vergeleken met klassieke chirurgische plaatsing van een nieuwe aortaklep. Het was dan ook logisch die techniek uit te testen bij patiënten met een laag operatief risico. Scandinavische vorsers hebben dat al tussen 2009 en 2013 gedaan in de Notion-studie. Die studie werd uitgevoerd bij een klein aantal patiënten, maar heeft opvallend positieve resultaten gegeven: geen verschil in het primaire eindpunt, een samengesteld eindpunt van overlijden, cerebrovasculair accident en myocardinfarct, na 1 en na 5 jaar15, 16. Die resultaten werden bevestigd door grotere studies: PARTNER 3 en Evolut Low Risk, die beide werden gepresenteerd op het laatste congres van het American College of Cardiology en die in maart werden gepubliceerd in the New England Journal of Medicine17, 18.
PARTNER 3 trial
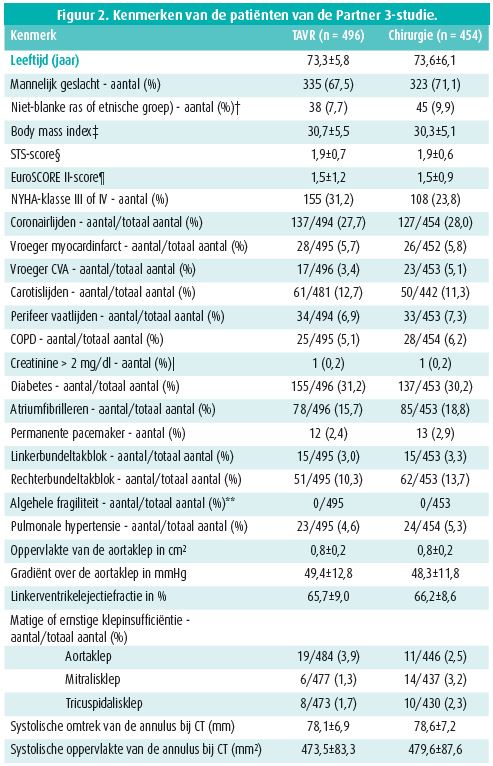
Deze gerandomiseerde studie werd uitgevoerd bij 1 000 patiënten van gemiddeld 73 jaar met een laag operatief risico (STS-PROM gemiddeld 1,9%) en een ernstige aortaklepstenose bij wie de klep diende te worden vervangen. De patiënten werden behandeld met een chirurgische bioprothese of een Sapien 3, die via de arteria femoralis werd ingeplant. Figuur 2 vat de kenmerken van de patiënten samen.
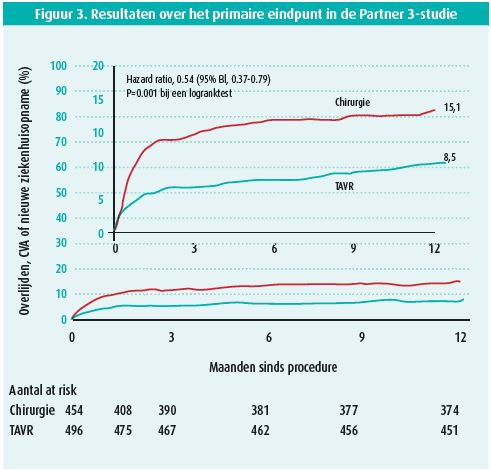
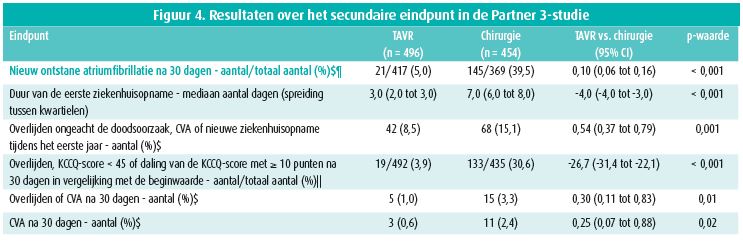
De incidentie van het primaire eindpunt, een samengesteld eindpunt van overlijden, cerebrovasculair accident en nieuwe ziekenhuisopname tijdens het eerste jaar, was significant lager na TAVI dan na chirurgie: 8,5 vs. 15,1 %, p < 0,001 voor non-inferioriteit en p = 0,001 voor superioriteit - figuur 3. De frequentie van cerebrovasculair accident, bloeding en optreden van atriumfibrilleren na 30 dagen was lager na TAVI en er was geen verschil in de frequentie van plaatsing van een pacemaker, ernstige vaatcomplicaties of een matig tot ernstig paravalvulair lek (figuur 4). Omgekeerd was de frequentie van linkerbundeltakblok en licht paravalvulair lek lager in de chirurgisch behandelde groep. De functionele toestand van de patiënten (NYHA-klasse en KCCQ-score) na 30 dagen was significant beter in de TAVI-groep. Na 1 jaar was de functionele toestand in de twee groepen vergelijkbaar. Na een TAVI herstellen de patiënten dus sneller.
EVOLUT Low Risk trial
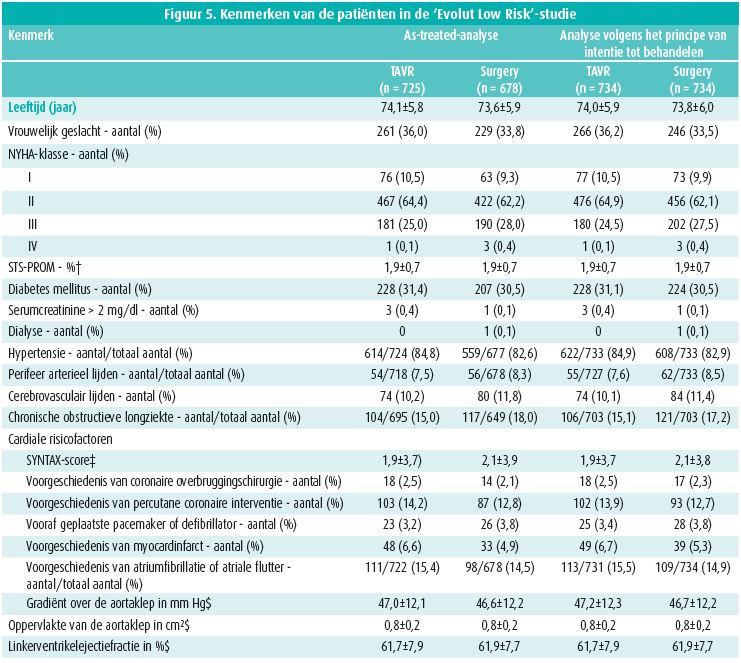
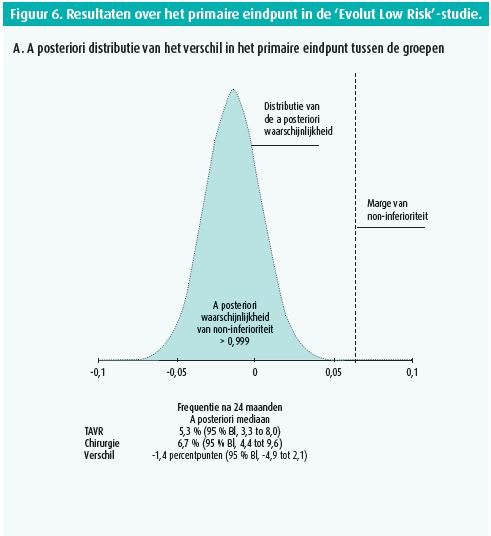
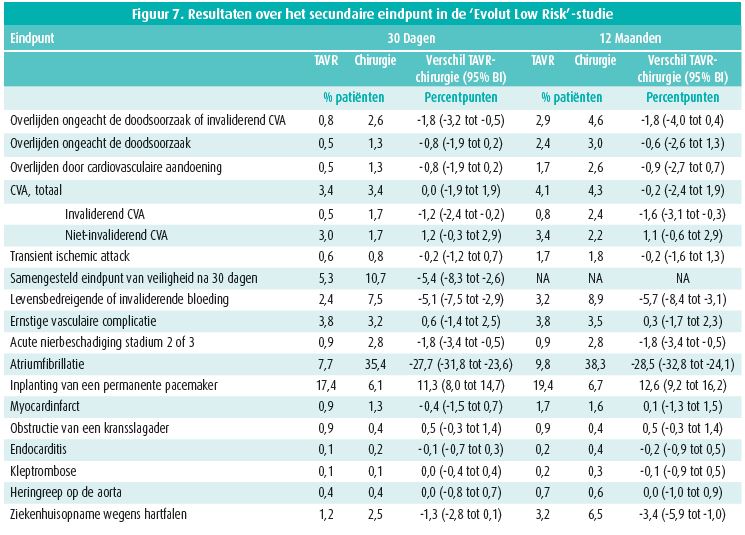
Deze gerandomiseerde studie werd uitgevoerd bij 1 468 patiënten van gemiddeld 74 jaar met een gemiddelde STS-PROM van 1,9 %, die werden behandeld met een chirurgische bioprothese of TAVI met inplanting van een Corevalve (3,6 %), een Evolut R (74,1 %) of Evolut Pro (22,3 %) via de arteria femoralis (99 %), de arteria subclavia (0,6 %) of direct via de aorta (0,4 %). Figuur 5 vat de kenmerken van de patiënten samen. De frequentie van het primaire eindpunt, een samengesteld eindpunt van overlijden en cerebrovasculair accident, was niet hoger in de TAVIgroep dan in de chirurgische groep: 5,3 vs. 6,7 %, waarschijnlijkheid van non-inferioriteit > 0,999-(figuur 6). Na 30 dagen was de frequentie van cerebrovasculair accident, bloeding, atriumfibrillatie of acute nierinsufficiëntie lager in de TAVI-groep. Die patiënten vertoonden echter vaker een matig tot ernstig paravalvulair lek en dienden vaker een pacemaker te krijgen dan na klassieke chirurgie (figuur 7).

Bespreking en perspectieven
Deze twee studies tonen aan dat een minimaal invasieve techniek bijzonder efficiënt is bij de behandeling van een degeneratieve aortaklepstenose, ook bij relatief jonge patiënten (gemiddelde leeftijd < 75 jaar) en patiënten zonder hoog operatief risico (STS-PROM gemiddeld < 2 %). De sterfte na 1 jaar was niet hoger, maar dat moet nog op lange termijn worden bevestigd. Indrukwekkend is ook dat de incidentie van cerebrovasculair accident significant lager was in de TAVI-groep, hoewel er geen gebruik werd gemaakt van een 'cerebral protection device' in de Partner 3-studie en slechts marginaal in de 'Evolut Low Risk'-studie (1,2 % van de gevallen). Dat was een belangrijk argument tegen het gebruik van TAVI in laagrisicosituaties, maar de resultaten zijn dus bijzonder geruststellend wat dat betreft.
Een ander bezwaar tegen TAVI bij patiënten met een laag risico was het optreden van ritmestoornissen. In de PARTNER 3-studie was het aantal patiënten bij wie een pacemaker diende te worden geplaatst, zeer laag en vergelijkbaar met dat in de chirurgische groep (6,5 vs. 4 % na 30 dagen en 7,3 vs. 5,4 % na 1 jaar, p = NS). In de 'Evolut Low Risk'-studie daarentegen was het aantal patiënten bij wie een pacemaker diende te worden geplaatst, bijna 3-maal hoger na TAVI (17,4 vs. 6,1 %, p < 0,05).
Een paravalvulair lek komt vaker voor na TAVI dan na chirurgie (enkel een licht paravalvulair lek in de Partner 3-studie, maar ook een matig tot ernstig paravalvulair lek in de 'Evolut Low Risk'-studie: 3,5 vs. 0,5 % na 30 dagen en 4,3 vs. 1,5 % na 1 jaar, p < 0,05).
In beide studies verliep het functionele herstel sneller en vertoonden de patiënten minder bloedingen, nierinsufficiëntie en atriumfibrilleren na TAVI.
Uit die twee studies blijkt dat TAVI weleens de beste behandeling zou kunnen zijn bij jonge patiënten met een laag operatief risico. Bij het nemen van een beslissing moet het hartteam dus rekening houden met alle aspecten, ook de voorkeur van de patiënt, als de voorgestelde behandelingen evenwaardig zijn.
In België gelden uiterst restrictieve voorwaarden voor terugbetaling van TAVI. Er zullen binnenkort nieuwe richtlijnen worden gepubliceerd, die ongetwijfeld rekening zullen houden met de resultaten van die twee studies en die dus TAVI zullen aanbevelen ongeacht het operatieve risico van de patiënt, maar wel rekening houdende met de voorkeur van de patient en anatomische criteria, die al dan niet in het voordeel van TAVI spreken. TAVI zou dan de eerstelijnstherapie worden bij een ernstige aortastenose.
Het aantal implantaten in België is veel lager dan het Europese gemiddelde (52 vs. 113 per miljoen inwoners). Op grond van de huidige richtlijnen, die zich enkel richten tot patiënten met een hoog of intermediair operatief risico, wordt het aantal patiënten dat in ons land in aanmerking komt voor TAVI, geraamd op 2 43119, 20. Het is dus niet houdbaar om het aantal TAVI's in ons land te beperken tot 500 per jaar.
Het financiële aspect is evenwel een echte rem op de vrijheid van keuze van de behandeling. De firma's verkopen die nieuwe percutane systemen immers tegen de prijs van goud.
Verder overleg tussen de producenten, de gezondheidsautoriteiten en de wetenschappelijke verenigingen is dus essentieel om de violen gelijk te stemmen en om alle patiënten toegang te bieden tot de moderne zorg.
Referenties
- Leon, M.B., Smith, C.R., Mack, M., Miller, D.C., Moses, J.W., Svensson, L.G., et al. Transcatheter aortic-valve implantation for aortic stenosis in patients who cannot undergo surgery. N Engl J Med, 2010, 363, 1597-1607.
- Makkar, R.R., Fontana, G.P., Jilaihawi, H., Kapadia, S., Pichard, A.D., Douglas, P.S. et al. Transcatheter aortic-valve replacement for inoperable severe aortic stenosis. N Engl J Med, 2012, 366, 1696-1704.
- Kapadia, S.R., Tuzcu, E.M., Makkar, R.R., Svensson, L.G., Agarwal, S., Kodali, S., et al. Longterm outcomes of inoperable patients with aortic stenosis randomly assigned to transcatheter aortic valve replacement or standard therapy. Circulation, 2014, 130, 1483-1492.
- Kapadia, S.R., Leon, M.B., Makkar, R.R., Tuzcu, E.M., Svensson, L.G., Kodali, S. et al. 5-year outcomes of transcatheter aortic valve replacement compared with standard treatment for patients with inoperable aortic stenosis (PARTNER 1): a randomised controlled trial. Lancet, 2015, 385, 2485-2491.
- Baumgartner, H., Falk, V., Bax, J.J., De Bonis, M., Hamm, C., Holm, P.J. et al. 2017 ESC/EACTS Guidelines for the management of valvular heart disease. Eur Heart J, 2017, 38, 2739-2791.
- Nishimura, R.A., Otto, C.M., Bonow, R.O., Carabello, B.A., Erwin, J.P. 3rd, Guyton, R. et al. 2014 AHA/ACC guideline for the management of patients with valvular heart disease: a report of the American College of Cardiology/ American Heart Association Task Force on Practice Guidelines. American College of Cardiology/American Heart Association Task Force on Practice Guidelines. J Am Coll Cardiol, 2014, 3 (22), e57-185.
- Smith, C.R., Leon, M.B., Mack, M.J., Miller, D.C., Moses, J.W., Svensson, L.G. et al. Transcatheter versus surgical aortic-valve replacement in highrisk patients. N Engl J Med, 2011, 364, 2187-2198.
- Adams, D.H., Popma, J.J., Reardon, M.J., Yakubov, S.J., Coselli, J.S., Deeb, G.M. et al. Transcatheter aortic-valve replacement with a self-expanding prosthesis. N Engl J Med, 2014, 370, 1790-1798.
- Kodali, S.K., Williams, M.R., Smith, C.R., Svensson, L.G., Webb, J.G., Makkar, R.R., et al. Two-year outcomes after transcatheter or surgical aortic-valve replacement. N Engl J Med, 2012, 366, 1686-1695.
- Mack, M.J., Leon, M.B., Smith, C.R., Miller, D.C., Moses, J.W., Tuzcu, E.M. et al. 5-year outcomes of transcatheter aortic valve replacement or surgical aortic valve replacement for high surgical risk patients with aortic stenosis (PARTNER 1): a randomised controlled trial. Lancet, 2015, 385, 2477-2484.
- Reardon, M.J., Adams, D.H., Kleiman, N.S., Yakubov, S.J., Coselli, J.S., Deeb, G.M., et al. 2-Year Outcomes in Patients Undergoing Surgical or Self-Expanding Transcatheter Aortic Valve Replacement. J Am Coll Cardiol, 2015, 66, 113-121.
- Deeb, G.M., Reardon, M.J., Chetcuti, S., Patel, H.J., Grossman, P.M., Yakubov, S.J. et al. 3-Year Outcomes in High-Risk Patients Who Underwent Surgical or Transcatheter Aortic Valve Replacement. J Am Coll Cardiol, 2016, 67, 2565-2574.
- Leon, M.B. and Smith, C.R. Transcatheter Aortic-Valve Replacement. N Engl J Med, 2016, 375, 700-701.
- Reardon, M.J., Van Mieghem, N.M., Popma, J.J., Kleiman, N.S., Sondergaard, L., Mumtaz, M. et al. Surgical or Transcatheter Aortic-Valve Replacement in Intermediate-Risk Patients. N Engl J Med, 2017, 376, 1321-1331.
- Thyregod, H.G., Steinbruchel, D.A., Ihlemann, N., Nissen, H., Kjeldsen, B.J., Petursson, P. et al. Transcatheter Versus Surgical Aortic Valve Replacement in Patients With Severe Aortic Valve Stenosis: 1-Year Results From the All-Comers NOTION Randomized Clinical Trial. J Am Coll Cardiol, 2015, 65, 2184-2194.
- Thyregod, H.G.H., Ihlemann, N., Jorgensen, T.H., Nissen, H., Kjeldsen, B.J., Petursson, P. et al. Five-Year Clinical and Echocardiographic Outcomes from the Nordic Aortic Valve Intervention (NOTION) Randomized Clinical Trial in Lower Surgical Risk Patients. Circulation, 2019, [E-pub ahead of paper].
- Mack, M.J., Leon, M.B., Thourani, V.H., Makkar, R., Kodali, S.K., Russo, M. et al.; the PARTNER 3 Investigators. Transcatheter Aortic-Valve Replacement with a Balloon-Expandable Valve in Low-Risk Patients. N Engl J Med, 2019, 380 (18), 1695-1705.
- Popma, J.J., Deeb, G.M., Yakubov, S.J., Mumtaz, M., Gada, H., O'Hair, D., Bajwa T, et al.; Evolut Low Risk Trial Investigators. Transcatheter Aortic-Valve Replacement with a Self-Expanding Valve in Low-Risk Patients. N Engl J Med, 2019, 380 (18), 1706-1715.
- Durko, A.P., Osnabrugge, R.L., Van Mieghem, N.M., Milojevic, M., Mylotte, D., Nkomo, V.T., Kappetein, P.A. Annual number of candidates for transcatheter aortic valve implantation per country: current estimates and future projections. Eur Heart J, 2018, 39, 2635-2642.
- Baron, S.J., Wang, K., House, J.A., Magnuson, E.A., Reynolds, M.R., Makkar, R. et al. Cost-Effectiveness of Transcatheter Versus Surgical Aortic Valve Replacement in Patients With Severe Aortic Stenosis at Intermediate Risk. Circulation, 2019, 139, 877-888.
Niets van de website mag gebruikt worden voor reproductie, aanpassing, verspreiding, verkoop, publicatie of commerciële doeleinden zonder voorafgaande schriftelijke toestemming van de uitgever. Het is ook verboden om deze informatie elektronisch op te slaan of te gebruiken voor onwettige doeleinden.