EAS-congresverslag
In deze interessante sessie van het jaarlijkse congres van de European Atherosclerosis Society worden de nieuwe behandelopties voor intensieve lipidentherapie samengevat.
Bempedoïnezuur
Ulrich Laufs (Leipzig, Duitsland)
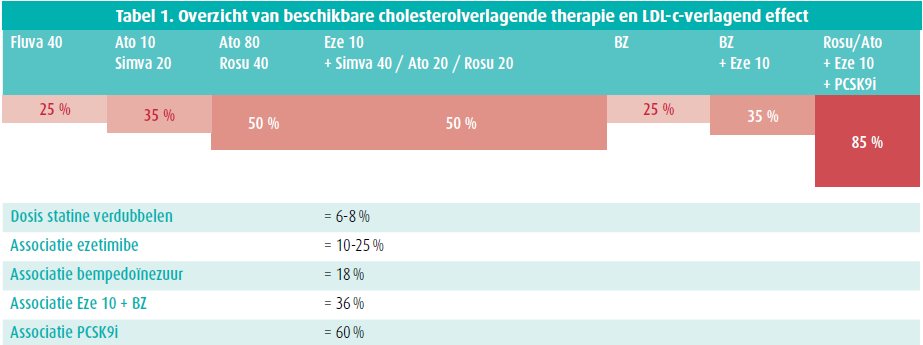
Hedendaagse cholesterolverlagende medicamenteuze therapie bestaat uit statines, ezetimibe en PCSK9-inhibitoren. Om het gebruik in de dagelijkse praktijk te kaderen toont hij een recente retrospectieve studie die de voorgeschreven cholesterolverlagende therapie bij 311 242 patiënten met een hoog cardiovasculair risico in Duitsland bestudeerde over een periode tussen 2013 en 2018.1 Hierin zag men een shift in het gebruik van simvastatine in 2013 naar meer gebruik van potente statines in 2018 door zowel huisartsen als specialisten. Opvallend is dat combinatietherapie met ezetimibe in 2018 nog slechts zelden gebruikt werd (4,7 % huisartsen en 16,3 % cardiologen). Op het vlak van efficiëntie kunnen we uit diezelfde data afleiden dat een combinatiepil met vaste dosis van statine en ezetimibe leidt tot een sterkere reductie van het LDL-c dan het gebruik van de twee producten als aparte preparaten (resp. gemiddelde LDL-c-reductie 28,4 % [40 mg/dL] vs. 19,4 % [27,5 mg/dL]), vermoedelijk door betere therapiecompliantie. Ondanks het gebruik van deze combinatiepil wordt de huidige LDL-c-doelstelling < 55mg/dL bij hoogrisicopatiënten slechts in 11 % behaald. Twee mogelijke verklaringen worden geopperd: de huidige cholesterolverlagende therapie is onvoldoende potent, oftewel wordt de beoogde potente dosis niet bereikt door statine-geassocieerde nevenwerkingen.
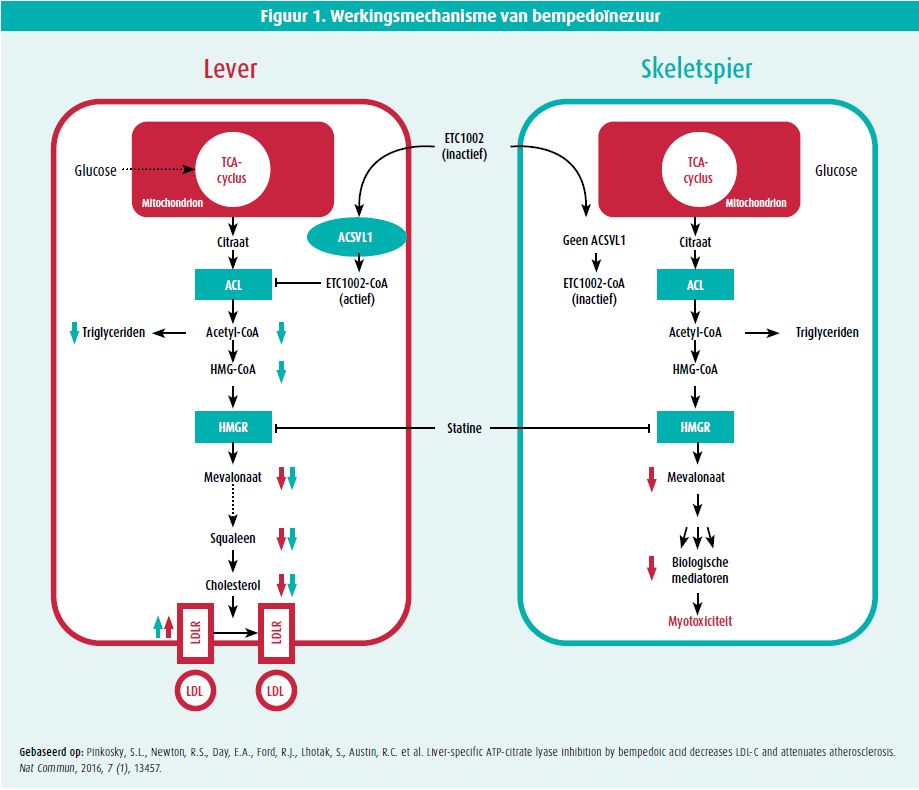
Om deze problemen aan te pakken werd bempedoïnezuur ontwikkeld. Bempedoïnezuur inhibeert ATP-citraatlyase (ACLY), een enzym dat zich in de route voor de biosynthese van cholesterol vóór HMG-CoA-reductase bevindt. Net als statines zal bempedoïnezuur het aantal LDL-receptoren verhogen, waardoor er meer LDL-c uit het bloed gezuiverd wordt. Een interessant voordeel ten opzichte van statines is dat bempedoïnezuur een prodrug is die geactiveerd moet worden door het ACSVL1-enzym, een enzym dat niet aanwezig is in skeletspierweefsel. Uit een belangrijke mendeliaanse randomisatiestudie kon men reeds enkele interessante voorspellingen over de efficiëntie en veiligheid van bempedoïnezuur formuleren. 2 Door het bestuderen van de genetische varianten die resp. de inhibitie van ACLY- en HMG-CoA-reductase simuleren, bleek het LDL-c-verlagende effect nagenoeg identiek. Daarnaast geven ACLYvarianten een vergelijkbaar effect als andere gekende genetische varianten op vlak van reductie in cardiovasculaire eindpunten, wat nogmaals de pathologische rol van LDL-c in atherosclerotische hart- en vaatziekten benadrukt. Ten slotte zijn er géén aanwijzingen dat ACLY-varianten geassocieerd zijn aan enige nefaste langetermijneffecten, wat kan dienen als surrogaat voor levenslange expositie aan bempedoïnezuur.
Momenteel zijn er verschillende fase 3-studies lopende met bempedoïnezuur. Uit de gepoolde data van deze studies ziet men een 17,8 % additionele LDL-c-daling bovenop maximaal getolereerde statines en een 24,5 % daling bij statine-intolerante patiënten met bempedoïnezuur monotherapie. 3 Aangezien de optimalisatie van de statinedosis in de dagelijkse praktijk vaak niet haalbaar is, kan de associatie van een combinatiepreparaat met bempedoïnezuur en ezetimibe een interessante behandeloptie zijn. Hiermee ziet men bovenop de maximaal getolereerde dosis statine een gemiddelde additionele LDL-c-daling van 36,2 % optreden.4,5
Op vlak van veiligheid kan een beperkte reversibele stijging van het creatinine en urinezuur optreden (vermoedelijk door zwakke inhibitie van OAT2-transporter in de renale tubulus) en een potentieel gunstig effect op het glucosemetabolisme (vermoedelijk door gunstige vetzuurmodulatie). 3 Een voorgeschiedenis van jicht kan een reden zijn om deze therapie niet voor te schrijven. Of de therapie gegeven kan worden aan patiënten die behandeld worden met urinezuurverlagende therapie is nog niet geweten.
De resultaten van de CLEAR Outcomes-studie (harde cardiovasculaire eindpunten) waarin 14 000 patiënten werden geïncludeerd worden verwacht in 2023.6
Duale of triple cholesterolverlagende combinatietherapie
Stephen Nicholls (Monash University, Australia)
Stephen Nicholls beklemtoont het causale verband tussen LDL-c en atherosclerotische hart- en vaataandoeningen. Het behalen van de strenge LDL-c-doelstellingen zal bij een groot aantal patiënten daarenboven leiden tot enige plaqueregressie. Zo'n 30 % van de groep die de doelstelling voor LDL-c behaalt, vertoont echter nog steeds ziekteprogressie. Deze patiënten hebben frequenter diabetes, hogere bloeddruk, lagere HDL-cen hogere ApoB-waarden (een maat voor het aantal circulerende LDL-partikels). Ondanks het bereiken van de LDL-c-doelstelling kan met andere woorden de atherogene lipideninhoud hoog blijven. Overige cholesterolverlagende therapie kan voor deze patiënten potentieel een gunstig additioneel effect opleveren.
Een aantal studies over combinatietherapie zijn beschikbaar. De PRECISE IVUS-studie toonde een grotere mate van plaqueregressie met ezetimibe bovenop atorvastatine ten opzichte van atorvastatine monotherapie (LDL-c-doelstelling 70 mg/dL).7 De IMPROVE-IT-studie toonde een bescheiden maar statistisch significante reductie in cardiovasculaire eindpunten (HR 0,936, CI 0,887-0,988, NNT 50) door de associatie van ezetimibe aan simvastatine bij patiënten die een acuut coronair syndroom doormaakten (de mediane opvolging is 6 jaar).8 Bij de PCSK9-inhibitoren zorgen zowel evolocumab als alirocumab voor een additionele LDL-c-verlaging van zo'n 60 %, bovenop de maximaal getolereerde statinetherapie. In de GLAGOV-studie zag men een grotere mate van plaqueregressie met evolocumab bovenop statine ten opzichte van statine monotherapie.9 Op vlak van cardiovasculaire eindpunten zag men 15 % reductie in zowel de FOURIER- als de ODYSSEY Outcomes-studie, resp. evolocumab bij patiënten met bewezen atherosclerotische ziekte en alirocumab na een acuut coronair syndroom.10,11 Een nieuwe manier om PCSK9 te inhiberen is inclisiran, een klein interfererend RNA (siRNA) dat LDL-c met zo'n 50 % doet dalen met slechts noodzaak tot intermittente toediening om de zes maanden. Grote klinische eindpuntstudies worden voorlopig afgewacht. Ten slotte is bempedoïnezuur ter beschikking gekomen, wat al uitgebreid besproken werd door Ulrich Laufs. Een recente (kleine) fase 2-studie bekeek de efficiëntie van de combinatietherapie bempedoïnezuur 180 mg, ezetimibe 10 mg en atorvastatine 20 mg per dag waarbij na zes weken een gemiddelde LDL-c-reductie van 60 % bereikt werd, waarvan 90 % de LDL-c-doelstelling < 70 mg/dL en 58 % een LDL-c < 55 mg/dL bereikte.12 Dergelijke 'triple therapie' zal voor veel patiënten een interessante strategie zijn, mede gezien de data van de recente Da Vinci-studie aantonen dat we er momenteel gewoon niet in slagen om de therapeutische doelstellingen voor LDL-c te bereiken.13
Statine-geassocieerde spierklachten (SAMS)
Erik Stroes (UMC Amsterdam)
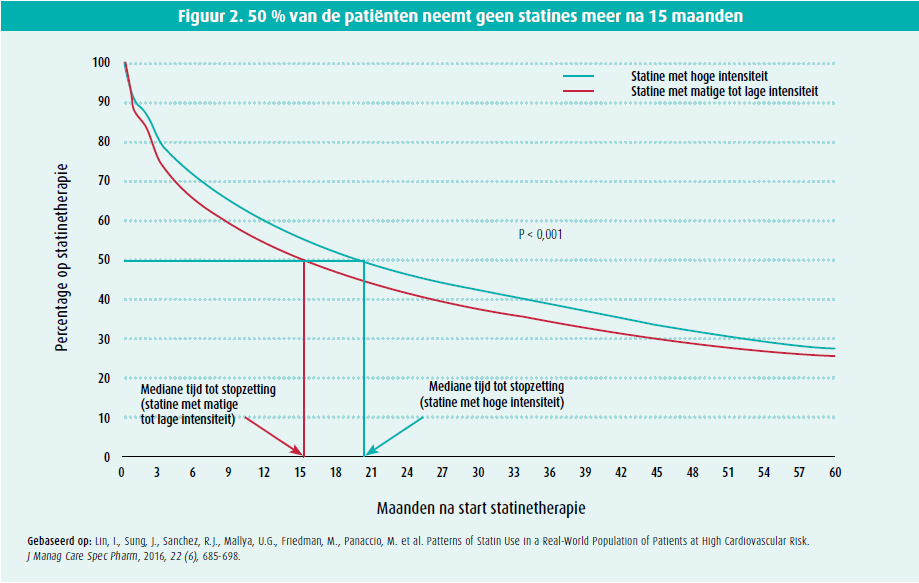
Erik Stroes sprak over statine-geassocieerde spierklachten (SAMS). Is dit het nocebo-effect of zijn dit echte klachten? Amerikaanse cijfers tonen aan dat ongeveer de helft van de patiënten zijn statine niet meer inneemt na zo'n 15 maanden.14 De voornaamste reden voor het onderbreken van de statine is het ervaren van bijwerkingen of angst voor het optreden van bijwerkingen.15 Opvallend is dat het vroegtijdig stoppen van een statine duidelijk gerelateerd is aan de hoeveelheid negatieve aandacht die in de media beschikbaar is.16 De vraag stelt zich dan ook of statine-gerelateerde nevenwerkingen niet louter bepaald worden door de negatieve verwachting die de patiënt eraan verbindt (nocebo-effect). De grote geblindeerde gerandomiseerde placebo-gecontroleerde statinestudies ondersteunen deze hypothese, aangezien er géén significant verschil aanwezig is op vlak van patiëntgerapporteerde myalgie tussen de statine- en placebogroepen.17 De Odyssey alternative-studie selecteerde patiënten op basis van eerdere statineintolerantie op minstens twee verschillende statines en werden blind gerandomiseerd naar alirocumab 75 mg per twee weken, ezetimibe 10 mg per dag of atorvastatine 20 mg per dag. In deze studie zag men géén verschil in spiergerelateerde nevenwerkingen tussen ezetimibe en atorvastatine (resp. 41 % en 46 %) én zag men alsnog spiergerelateerde nevenwerkingen met alirocumab in 32 % van de patiënten.18 Ook de SAMSON-studie, een geblindeerde n=1-studie waarbij patiënten gerandomiseerd werden naar sequentiële inname van géén pil, placebo of statine toonde aan dat 90 % van de statine-gerelateerde klachten verklaard kan worden door het nocebo-effect.19
Zijn álle SAMS dan nocebo-effect? Er zijn enkele geblindeerde, gerandomiseerde studies beschikbaar die het bestaan van SAMS lijken te verdedigen. De kleinschalige STOMP-trial rapporteerde meer myalgie na toediening van atorvastatine 80 mg vs. placebo gedurende 6 maanden aan 420 gezonde vrijwilligers (19 vs. 10 patiënten, p = 0,052).20 De GAUSS-3-studie includeerde 511 statine-intolerante patiënten (minstens 3 verschillende preparaten) en randomiseerde deze in een cross-over design naar atorvastatine 20 mg of placebo gedurende telkens 10 weken, waarbij men méér spierklachten zag optreden in de statinegroep in beide cross-over groepen (resp. 52 % vs. 36 %).21
Hoe moeten we als arts nu omgaan met SAMS? In de ideale wereld is de beste aanpak vermoedelijk het uitvoeren van een n=1-studie bij elke patiënt met statineintolerantie, om op deze manier cognitieve therapie te geven. De praktische haalbaarheid in de dagelijkse praktijk is uiteraard een groot vraagteken. De TaSINI-studie zal onderzoeken of een niet-geblindeerde n=1-studie uitgevoerd door de huisarts de statine-inname kan verhogen ten opzichte van standaardzorg.22 In deze studie zal men 90 patiënten in de primaire zorg randomiseren naar een niet-geblindeerde n=1-studie (interventiegroep), een geblindeerde n=1-studie (positieve controle) of standaardzorg (negatieve controle). De interventiegroep zal driemaal gedurende telkens 4 weken géén medicatie of atorvastatine 20 mg per dag krijgen. De geblindeerde n=1-studiegroep krijgt placebo of atorvastatine 20 mg per dag. Als de aanpak haalbaar blijkt, zal in de tweede tijd een grotere RCT gepland worden.
Discussie
Tijdens de discussie werden nog enkele interessante vragen gesteld, samengevat:
- Er zijn geen goede gevalideerde myalgiescores beschikbaar om 'echte' SAMS te differentiëren van SAMS als nocebo-klacht. Momenteel zijn er géén genetische varianten of scores beschikbaar om 'echte' SAMS te identificeren.
- PCSK9-inhibitoren kunnen een goed alternatief vormen bij statine-intolerantie, maar dit zou moeten worden voorbehouden aan patiënten die minstens 3 verschillende statines gekregen hebben, waarvan 1 ervan in de laagste dosering.
- Bempedoïnezuur heeft net als statines geen verlagend effect op lp(a).
- Net als bij andere risicofactoren zoals hypertensie of diabetes dient cholesterol frequent gecontroleerd te worden, waarbij snelle dosisescalatie de doelstelling moet zijn. De zogenaamde fire and forget-strategie waarbij een statine gestart wordt en niemand de opvolging verzorgt, moet worden vermeden.
- De levenslange expositie aan hoge LDL-c is causaal voor atherosclerose, vroegtijdige en agressieve behandeling van cholesterol moet het doel zijn.
- Combinatietherapie is noodzakelijk, waarbij gepersonaliseerde lipidenverlagende therapie in de nabije toekomst mogelijk zal zijn.
Referenties
- Katzmann, J.L., Sorio-Vilela, F., Dornstauder, E., Fraas, U., Smieszek, T., Zappacosta, S. et al. Non-statin lipid-lowering therapy over time in very-high-risk patients: effectiveness of fixeddose statin/ezetimibe compared to separate pill combination on LDL-C. Clin Res Cardiol, 2020.
- Ference, B.A., Ray, K.K., Catapano, A.L., Ference, T.B., Burgess, S., Neff, D.R. et al. Mendelian Randomization Study of ACLY and Cardiovascular Disease. N Engl J Med, 2019, 380 (11), 1033-1042.
- Bays, H.E., Banach, M., Catapano, A.L., Duell, P.B., Gotto, A.M., Laufs, U. et al. Bempedoic acid safety analysis: Pooled data from four phase 3 clinical trials. J Clin Lipidol, 2020, 14 (5), 649-59.e6.
- Ballantyne, C.M., Laufs, U., Ray, K.K., Leiter, L.A., Bays, H.E., Goldberg, A.C. et al. Bempedoic acid plus ezetimibe fixed-dose combination in patients with hypercholesterolemia and high CVD risk treated with maximally tolerated statin therapy. Eur J Prev Cardiol, 2020, 27 (6), 593-603.
- Ballantyne, C.M., Banach, M., Mancini, G.B.J., Lepor, N.E., Hanselman, J.C., Zhao, X. et al. Efficacy and safety of bempedoic acid added to ezetimibe in statin-intolerant patients with hypercholesterolemia: A randomized, placebocontrolled study. Atherosclerosis, 2018, 277, 195-203.
- Nicholls, S., Lincoff, A.M., Bays, H.E., Cho, L., Grobbee, D.E., Kastelein, J.J. et al. Rationale and design of the CLEAR-outcomes trial: Evaluating the effect of bempedoic acid on cardiovascular events in patients with statin intolerance. Am Heart J, 2021, 235, 104-112.
- Tsujita, K., Sugiyama, S., Sumida, H., Shimomura, H., Yamashita, T., Yamanaga, K. et al. Impact of Dual Lipid-Lowering Strategy With Ezetimibe and Atorvastatin on Coronary Plaque Regression in Patients With Percutaneous Coronary Intervention: The Multicenter Randomized Controlled PRECISE-IVUS Trial. J Am Coll Cardiol, 2015, 66 (5), 495-507.
- Cannon, C.P., Blazing, M.A., Giugliano, R.P., McCagg, A., White, J.A., Theroux, P. et al. Ezetimibe Added to Statin Therapy after Acute Coronary Syndromes. N Engl J Med, 2015, 372 (25), 2387-2397.
- Nicholls, S.J., Puri, R., Anderson, T., Ballantyne, C.M., Cho, L., Kastelein, J.J.P. et al. Effect of Evolocumab on Progression of Coronary Disease in Statin-Treated Patients. JAMA, 2016, 316 (22), 2373.
- Sabatine, M.S., Giugliano, R.P., Keech, A.C., Honarpour, N., Wiviott, S.D., Murphy, S.A. et al. Evolocumab and Clinical Outcomes in Patients with Cardiovascular Disease. N Engl J Med, 2017, 376 (18), 1713-1722.
- Schwartz, G.G., Steg, P.G., Szarek, M., Bhatt, D.L., Bittner, V.A., Diaz, R. et al. Alirocumab and Cardiovascular Outcomes after Acute Coronary Syndrome. N Engl J Med, 2018, 379 (22), 2097-2107.
- Rubino, J., Macdougall, D.E., Sterling, L.R., Hanselman, J.C., Nicholls, S.J. Combination of bempedoic acid, ezetimibe, and atorvastatin in patients with hypercholesterolemia: A randomized clinical trial. Atherosclerosis, 2021, 320, 122-128.
- Ray, K.K., Molemans, B., Schoonen, W.M., Giovas, P., Bray, S., Kiru, G. et al. EU-Wide Cross-Sectional Observational Study of Lipid- Modifying Therapy Use in Secondary and Primary Care: the DA VINCI study. Eur J Prev Cardiol, 2020.
- Lin, I., Sung, J., Sanchez, R.J., Mallya, U.G., Friedman, M., Panaccio, M. et al. Patterns of Statin Use in a Real-World Population of Patients at High Cardiovascular Risk. J Manag Care Spec Pharm, 2016, 22 (6), 685-698.
- Bradley, C.K., Wang, T.Y., Li, S., Robinson, J.G., Roger, V.L., Goldberg, A.C. et al. Patient-Reported Reasons for Declining or Discontinuing Statin Therapy: Insights From the PALM Registry. J Am Heart Assoc, 2019, 8 (7).
- Nielsen, S.F., Nordestgaard, B.G. Negative statin-related news stories decrease statin persistence and increase myocardial infarction and cardiovascular mortality: a nationwide prospective cohort study. Eur Heart J, 2016, 37 (11), 908-916.
- Newman, C.B., Tobert, J.A. Statin intolerance: reconciling clinical trials and clinical experience. JAMA, 2015, 313 (10), 1011-1012.
- Moriarty, P.M., Thompson, P.D., Cannon, C.P., Guyton, J.R., Bergeron, J., Zieve, F.J. et al. Efficacy and safety of alirocumab vs ezetimibe in statin-intolerant patients, with a statin rechallenge arm: The ODYSSEY ALTERNATIVE randomized trial. J Clin Lipidol, 2015, 9 (6), 758-769.
- Wood, F.A., Howard, J.P., Finegold, J.A., Nowbar, A.N., Thompson, D.M., Arnold, A.D. et al. N-of-1 Trial of a Statin, Placebo, or No Treatment to Assess Side Effects. N Engl J Med, 2020, 383 (22), 2182-2184.
- Parker, B.A., Capizzi, J.A., Grimaldi, A.S., Clarkson, P.M., Cole, S.M., Keadle, J. et al. Effect of Statins on Skeletal Muscle Function. Circulation, 2013, 127 (1), 96-103.
- Nissen, S.E., Stroes, E., Dent-Acosta, R.E., Rosenson, R.S., Lehman, S.J., Sattar, N. et al. Efficacy and Tolerability of Evolocumab vs Ezetimibe in Patients With Muscle-Related Statin Intolerance. JAMA, 2016, 315 (15), 1580.
- Tudor, K., Brooks, J., Howick, J., Fox, R., Aveyard, P. Tackling statin intolerance with n-of-1 trials (TaSINI) in primary care: protocol for a feasibility randomised trial to increase statin adherence. BMJ Open, 2020, 10 (2), e033070.
- Pinkosky, S.L., Newton, R.S., Day, E.A., Ford, R.J., Lhotak, S., Austin, R.C. et al. Liver-specific ATP-citrate lyase inhibition by bempedoic acid decreases LDL-C and attenuates atherosclerosis. Nat Commun, 2016, 7 (1), 13457.
Niets van de website mag gebruikt worden voor reproductie, aanpassing, verspreiding, verkoop, publicatie of commerciële doeleinden zonder voorafgaande schriftelijke toestemming van de uitgever. Het is ook verboden om deze informatie elektronisch op te slaan of te gebruiken voor onwettige doeleinden.