BSC-congresverslag - S11
Veneuze insufficiëntie
Luc Maraglia - Société Française de Phlébologie, Frankrijk
Veneuze insufficiëntie, zich klinisch manifesterend als chronische veneuze ziekte (CVZ), lokaliseert zich vooral ter hoogte van het onderste lidmaat en wordt gedefinieerd als elke morfologische of functionele veneuze abnormaliteit van langere duur die zich uit via klinische tekenen of symptomen. CVZ is gerelateerd aan insufficiëntie van het oppervlakkige, diepe of perforerende veneuze netwerk.1
Pathofysiologisch gezien leiden veranderingen in de veneuze wand en kleppen van het oppervlakkige veneuze systeem tot insufficiëntie van deze kleppen, veranderingen in vasomotorische tonus en reflux. Het gevolg hiervan is veneuze hypertensie, zich vooral manifesterend in rechtopstaande positie. Lediging in het diepe veneuze systeem wordt gecompromitteerd door obstructie of reflux, wat leidt tot veneuze hypertensie in het oppervlakkige systeem. De onderliggende etiologie is vaak een diepveneuze trombose (DVT). De symptomen en tekens hiervan zijn het zogenaamde post-trombotisch syndroom (PTS).
De CEAP-classificatie (clinical, etiological, anatomical, pathophysiological) laat toe CVZ in de onderste ledematen te beschrijven, waarbij vooral het klinische aspect relevant is voor de praktijk (tabel 1).
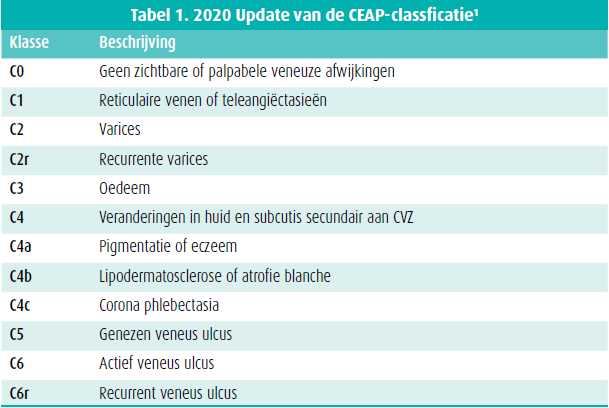
Symptomatologie van CVZ is gevarieerd, leeftijdsgebonden en komt meer voor bij vrouwen. De impact op de levenskwaliteit kan groot zijn. Meest typisch betreft het een zwaar/vermoeid gevoel in de benen. Jeuk en brandende pijn zijn andere symptomen, typisch toenemend bij lang rechtop staan. Klinische tekens en symptomen zijn niet per se gebonden aan elkaar.
Recent werden de richtlijnen over het management van onderste lidmaat CVZ door de European Society of Vascular Surgery (ESVS) aangepast.1 Het navragen van trombo-emboligene voorgeschiedenis en/of varicesingrepen en klinisch onderzoek in rechtopstaande houding zijn cruciaal. Een duplex ultrasound scanning (DUS) van de onderste ledematen wordt bij alle stadia aangeraden als eerste keuze beeldvorming. Het verschaft informatie over veneuze anatomie, doorgankelijkheid, wandpathologie, en de flow in het oppervlakkige netwerk. Verder geeft het informatie over morfologische en hemodynamische aspecten van de diepe venen. Een venous mapping opstellen (diameters, diepte, anatomische relatie met arteriën/zenuwen) is noodzakelijk bij het plannen en uitvoeren van veneuze interventies. Wanneer een supra-inguïnale veneuze pathologie vermoed wordt, gebaseerd op klinisch onderzoek en specifieke DUS-bevindingen, wordt bijkomend een abdominale pelvische DUS uitgevoerd.
Therapeutisch gezien verbeteren fysieke inspanningen, kinesitherapie, hoogstand van het been en het dragen van steunzolen de veneuze return. Levensstijlwijzingen zoals wandelen, obesitas voorkomen en vermijden van lang rechtop staan en hitteblootstelling sluiten hierbij aan. Compressietherapie (≥ 15 mmHg ter hoogte van de enkel) wordt aangewend om symptomen en oedeem te reduceren, waarbij de hoogst te verdragen druk ter hoogte van de enkel voor maximale effectiviteit zorgt. Er is echter geen evidentie voor het vertragen van progressie of recidief van veneus lijden. Compressietherapie blijft wel de hoeksteen van de conservatieve behandeling van CVZ.
Er is een klasse Ia-indicatie om compressietherapie toe te passen, bij patiënten met actieve veneuze ulceraties, waarbij de targetdruk ter hoogte van de enkel minstens 40 mmHg bedraagt.1 De belangrijkste contra-indicaties voor compressietherapie zijn ernstige atherosclerotische ziekte met een enkel-arm index < 0,6 of een bloeddruk ter hoogte van de enkel < 60 mmHg, en ernstige diabetische neuropathie met sensorische aantasting of micro-angiopathie met risico op huid necrose.
Veno-actieve drugs (VAD) werken door middel van vermindering van capillaire permeabiliteit, reductie van inflammatie en toename van veneuze tonus. Deze medicamenten moeten worden overwogen bij patiënten met symptomatische CVZ, maar staan ter discussie.1
Interventionele behandeling bestaat uit sclerotherapie, flebectomie en endoveneuze thermale ablatie. Een interventionele behandeling is geïndiceerd (Ia) bij oppervlakkige, veneuze insufficiëntie o.v.v. symptomatische variceuze venen (CEAP, C2), en als de veneuze insufficiëntie zich manifesteert als huidverandering (CEAP, C4-6). Het type interventionele behandeling is casusafhankelijk.
Wat betreft behandeling van insufficiëntie van de vena saphena magna is endoveneuze thermale ablatie (radiofrequent of laser), al dan niet in combinatie met flebectomie, de eerste keuze, waar dit vroeger open heelkunde was. Bij deze endoveneuze aanpak is lokale anesthesie voldoende en moet anticoagulatie niet worden onderbroken.
Acute en subacute diepveneuze trombose
Serge Motte - Erasmusziekenhuis
Anticoagulatie bij veneuze trombo-embolie (VTE) bestaat uit een acute fase en een langetermijnbehandeling (drie maanden) (tabel 2).
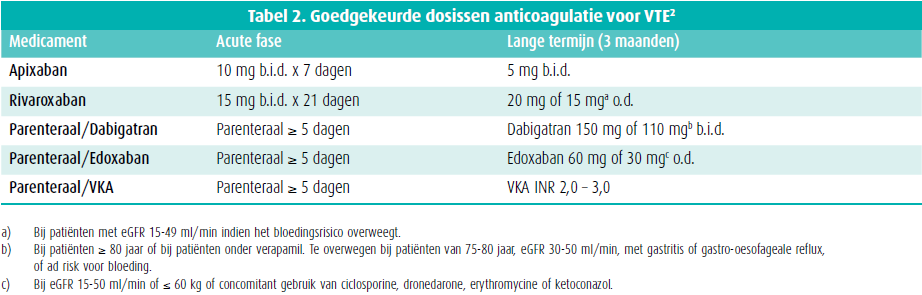
Betreffende de langetermijnbehandeling wordt in de tweede update van de CHEST-richtlijnen en expertpanelgroep het gebruik van DOAC's sterk aangeraden boven vitamine K-antagonisten (VKA).2 Hospitalisatie van een patiënt met een DVT wordt bepaald door het risico op lidmaatverlies (indicatie voor trombolyse), absolute contra-indicaties voor LMWH of DOAC (indicatie voor venacavafilter) en de indicatie voor hospitalisatie vanwege comorbiditeiten.3
Drie specifieke populaties in de behandeling van VTE zijn patiënten met ernstige nier-insufficiëntie, kanker of antifosfolipidensyndroom (APS). De RIETE-registry gaf aan dat 11 % van de patiënten met acute VTE ernstige nierinsufficiëntie had, met een hogere graad van majeure bloedingen (odds ratio 2,26 met 95 % BI 2,01 - 2,53) vergeleken met patiënten zonder ernstige nierinsufficiëntie.4 De nadruk ligt hier op het vermijden van de hoge dosis DOAC bij een eGFR 15-29 ml/min, die bij initiële behandeling in se aangewend kan worden, aangezien er weinig data is omtrent DOAC in de behandeling van VTE bij sterk gedaalde nierfunctie. Preferentieel wordt er initieel overgegaan tot enoxaparine 1 mg/kg daags, of tinzaparine 175 IU/kg, bij een geschatte creatinineklaring tussen 15 en 29 ml/min.
Patiënten met kanker vormden in het RIETE-registry 20 % van de patiënten met acute VTE en vertoonden een verhoogd risico op morbiditeit en mortaliteit.5 Een meta-analyse kon geen significant verschil aantonen tussen DOAC en LMWH in het voorkomen van recurrente VTE of majeure bloeding.6 De CHEST-richtlijnen weerhouden een sterke aanbeveling voor de orale anti-Xa inhibitoren ten opzichte van LMWH voor de initiële, en de onderhoudstherapie. Bij gastro-intestinale tumoren gaat de voorkeur uit naar apixaban of LMWH.2
Ongeveer 10 % van de patiënten met VTE blijkt het antifosfolipidensyndroom (APS) te hebben, met een hoger risico op recidief VTE.7,8 Het EMA pleit tegen gebruik van DOAC bij patiënten met het APS. Het risico op arteriële trombose bij patiënten met APS was hoger bij gebruik van een DOAC (rivaroxaban) ten opzichte van VKA.9,10 Bij triple-positieve APS moet men gebruik van een DOAC vermijden, terwijl bij niet-triple positieve APS reeds onder DOAC de DOAC verdergezet kan worden, of naar VKA overgeschakeld kan worden.11
Langetermijnanticoagulatie na VTE
Karl von Kemp - Universitair Ziekenhuis Brussel
Een inschatting van het risico op recidief wordt gemaakt door na te gaan of de VTE al dan niet uitgelokt was, en wat de risicofactoren waren. Deze laatste kunnen worden opgedeeld in transiënt en persisterend. De transiënte risicofactoren worden verder onderverdeeld in majeure en mineure risicofactoren (tabel 3).12 Tegenover het risico op recidief staat uiteraard het risico op bloedingen, dat aan de hand van het ACCP-model geëvalueerd kan worden, waarbij periodieke herevaluatie essentieel is (tabel 3).13
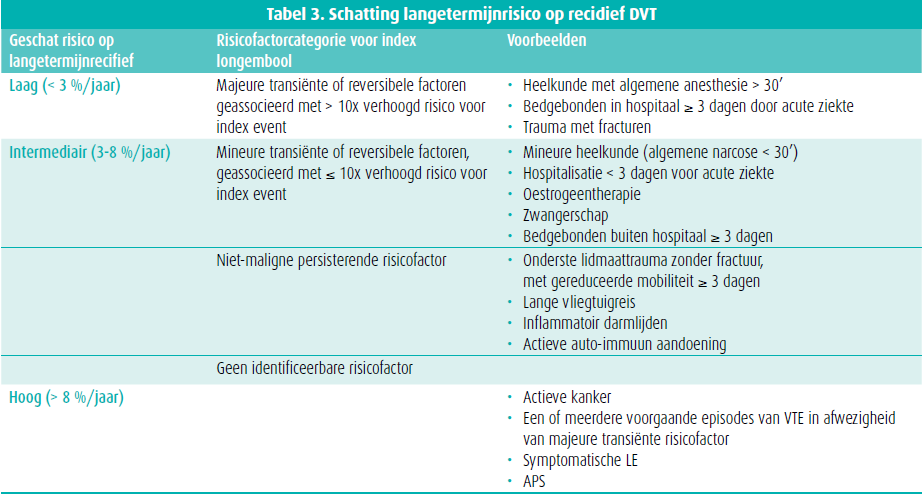
Bij een hoog risico op recidief VTE met een laag of intermediair bloedingsrisico is anticoagulatie ad vitam geïndiceerd, terwijl dit bij een hoog bloedingsrisico minstens overwogen moet worden. Bij een hoog bloedingsrisico is de strikte indicatie voor langetermijnanticoagulatie gelimiteerd tot recurrente, niet-uitgelokte VTE.12 Als er een absolute contra-indicatie is voor anticoagulatie moet een vena cava filter worden overwogen, of bij recidief longembolie ondanks correcte anticoagulatie. Bij een intermediair risico op recidief VTE zijn er meerdere mogelijkheden. Wanneer het om een eerste VTE met een persisterende niet-maligne risicofactor of recurrente VTE met een transiënte of persisterende niet-maligne risicofactor gaat, wordt anticoagulatie van onbepaalde duur gesuggereerd. Een eerste VTE met een transiënte, mineure risicofactor wordt best individueel beoordeeld.12 Bij een laag risico op recidief VTE, is er geen indicatie voor verlengde anticoagulatie.
Het gebruik van lage intensiteit anticoagulatie op het voorkomen van recurrente VTE en bloeding werd onderzocht in een trial met rivaroxaban (20 en 10 mg doses) vs. acetylsalicylzuur en een trial van apixaban (2 x 5 mg vs 2 x 2,5 mg doses) bij patiënten met twijfel (risico trombose/bloeding vergelijkbaar) voor verlengde anticoagulatie. Het verderzetten van anticoagulatie na drie maanden therapie, met rivaroxaban in een klassieke dosis van 20 mg, maar ook in een profylactische dosis 10 mg o.d. versus acetylsalicylzuur 100 mg verminderde significant recidief VTE, zonder toename van bloeding.14 Ook het verderzetten van apixaban 5 mg b.i.d. of in profylactische dosis 2,5 mg b.i.d. bleek het risico op VTE te reduceren, zonder een significante toename in bloedingen te veroorzaken.15
Referenties
- De Maeseneer, M.G., Kakkos, S.K., Aherne, T., Baekgaard, N., Black, S., Blomgren, L. et al. Editor's Choice - European Society for Vascular Surgery (ESVS) 2022 Clinical Practice Guidelines on the Management of Chronic Venous Disease of the Lower Limbs. Eur J Vasc Endovas Surg, 2022, 63 (2), 184-267.
- Stevens, S.M., Woller, S.C., Kreuziger, L.B., Bounameaux, H., Doerschug, K., Geersing, G-J. et al. Antithrombotic Therapy for VTE Disease: Second Update of the CHEST Guideline and Expert Panel Report. Chest, 2021, 160 (6), 545-608.
- Khan, F., Tritschler, T., Kahn S.R., Rodger, M.A. et al. Venous thromboembolism. The Lancet, 2021, 398 (10294), 64-77.
- Catella, J., Bertoletti, L., Mismetti, P., Ollier, E., Samperiz, A., Soler, S. et al. Severe renal impairment and risk of bleeding during anticoagulation for venous thromboembolism. J Thromb Haemost, 2020, 18 (7), 1728-1737.
- Monreal, M., Falgá, C., Valle, R., Barba, R., Bosco, J., Beato, J.L. et al. Venous thromboembolism in patients with renal insufficiency: findings from the RIETE Registry. Am J Med, 2006, 119 (12), 1073-1079.
- Mulder, F.I., Bosch, F.T.M., Young, A.M., Marshall, A., McBane, R.D., Zemla, T.J. et al. Direct oral anticoagulants for cancerassociated venous thromboembolism: a systematic review and meta-analysis. Blood, 2020, 136 (12), 1433-441.
- Tromeur, C., Sanchez, O., Presles, E., Pernod, G., Bertoletti, L., Jego, P. et al. Risk factors for recurrent venous thromboembolism after unprovoked pulmonary embolism: the PADISPE randomised trial. Eur Respir J, 2017, 51 (1), 1701202.
- Kearon, C., Parpia, S., Spencer, F.A., Baglin, T., Stevens, S.M., Bauer, K.A. et al. Antiphospholipid antibodies and recurrent thrombosis after a first unprovoked venous thromboembolism. Blood, 2018, 131 (19), 2151-2160.
- Pengo, V., Denas, G., Zoppellaro, G., José, S.P., Hoxha, A., Ruffatti, A. Rivaroxaban vs warfarin in high-risk patients with antiphospholipid syndrome. Blood, 2018, 132 (13), 1365-1371.
- Ordi-Ros, J., Sáez-Comet, L., Pérez-Conesa, M. Vidal, Riera-Mestre, A., Castro- Salomó, A., Cuquet-Pedragosa, J. et al. Rivaroxaban Versus Vitamin K Antagonist in Antiphospholipid Syndrome: A Randomized Noninferiority Trial. Ann Intern Med, 2019, 171 (10), 685-694.
- Arachchillage, D.R.J., Gomez, K., Alikhan, R., Anderson, J.A.M., Lester, W., Laffan, M. et al. Addendum to British Society for Haematology Guidelines on Investigation and Management of Antiphospholipid syndrome, 2012 (Br. J. Haematol. 2012; 157: 47-58): use of direct acting oral anticoagulants. Br J Haematol, 2020, 189 (2), 212-215.
- Konstantinides, S.V., Meyer, G., Becattini, C., Bueno, H., Geersing, G-J., Harjola, V-P. et al. 2019 ESC Guidelines on the diagnosis and management of acute pulmonary embolism. Eur Heart J, 2020, 41 (4), 543-603.
- Kearon, C., Akl, E.A., Comerota, A.J. et al. Antithrombotic therapy for VTE disease: antithrombotic therapy and prevention of thrombosis, 9th ed: American College of Chest Physicians evidence-based clinical practice guidelines. Chest, 2012, 141 (2), suppl:e419S-e494S.
- Weitz, J.I., Lensing, A.W.A., Prins, M.H., Bauersachs, R., Beyer-Westendorf, J., Bounameaux, et al. Rivaroxaban or Aspirin for Extended Treatment of Venous Thromboembolism. N Engl J Med, 2017, 376 (13), 1211-1222.
- Agnelli, G., Buller, H.R., Cohen, A., Curto, M., Gallus, A.S. et al. Apixaban for extended treatment of venous thromboembolism. N Engl J Med, 2013, 368 (8), 699-708.
Niets van de website mag gebruikt worden voor reproductie, aanpassing, verspreiding, verkoop, publicatie of commerciële doeleinden zonder voorafgaande schriftelijke toestemming van de uitgever. Het is ook verboden om deze informatie elektronisch op te slaan of te gebruiken voor onwettige doeleinden.