Over atriumfibrillatie via een accessoire bundel
Amiodaron, een klasse III-antiaritmicum (classificatie van Vaughan-Williams) werkt in op de verschillende ionenkanalen van het myocard en heeft daarbij vooral een sterk effect op de refractaire periode en de repolarisatie van de cellen. Het remt ook op niet-competitieve wijze de bèta-adrenerge receptoren.1-4
Von Kemp et al. hebben recent in dit tijdschrift een patiënt beschreven die werd behandeld met amiodaron wegens een acute atriumfibrillatie via een accessoire bundel met een snel kamerantwoord. Die gevalsbeschrijving heeft onze aandacht getrokken.5 We vinden het belangrijk om het gebruik van amiodaron bij supraventriculaire ritmestoornissen in het algemeen en atriumfibrillatie in het bijzonder te beschrijven. Anderzijds is het nuttig het effect van intraveneuze toediening van amiodaron in een acute situatie te vergelijken met dat van perorale toediening. Het bestaan van een accessoire bundel bij het ontstaan van een atriumfibrillatie vormt de basis voor de discussie. We beschrijven de verschillende antiaritmica die in die specifieke situatie worden gebruikt. Ook beschrijven we de differentiële diagnose van die onregelmatige tachycardieën met een breed QRS-complex.
Gebruik van amiodaron bij supraventriculaire tachycardie
Amiodaron wordt al lang aanbevolen voor de acute en chronische behandeling van meerdere supraventriculaire ritmestoornissen.6,7 De laatste internationale richtlijnen voor amiodaron zijn meestal klasse IIb-richtlijnen met een niveau C van bewijskracht.8 Een vrij zwakke richtlijn dus, wat echter vooral toe te schrijven is aan het feit dat er geen grote gecontroleerde studies zijn uitgevoerd, en de angst voor bijwerkingen op lange termijn bij een chronische behandeling, maar ook doordat veel vaker gebruik wordt gemaakt van andere zeer doeltreffende antiaritmica, zoals klasse IC-antiaritmica. In plaats van chronische toediening van amiodaron bij de preventie van recidief van supraventriculaire ritmestoornissen wordt nu meestal een ablatietechniek uitgevoerd, vaak als eerstelijnstherapie. Amiodaron blijft evenwel een mogelijke optie bij de behandeling van acute en chronische specifieke, moeilijk te controleren refractaire ritmestoornissen.8
Amiodaron en atriumfibrillatie
Atriumfibrillatie is de frequentste ritmestoornis, die ook vaak recidiveert. Perorale toediening van amiodaron bij de preventie op lange termijn van recidief van atriumfibrillatie wordt in de laatste richtlijnen beschouwd als een klasse I-richtlijn (klasse I/A).9 Dat lijkt wat verrassend, gezien de mogelijke bijwerkingen bij langdurige toediening van amiodaron. De richtlijnen houden rekening met het feit dat amiodaron een bijzonder doeltreffend antiaritmicum is en ook het kamerantwoord vertraagt. Ze stellen evenwel ook dat andere antiaritmica in de mate van het mogelijke te verkiezen zijn. Als de ventrikelfunctie niet normaal is, blijft amiodaron echter een voortreffelijke keuze.
Bij een refractaire atriumfibrillatie kan amiodaron ook als laatste redmiddel worden voorgeschreven om het kamerantwoord onder controle te brengen. Amiodaron geniet nog altijd de voorkeur in geval van een verminderde linkerventrikelfunctie. In geval van atriumfibrillatie met een snel kamerantwoord en hemodynamische verslechtering kan amiodaron ook in een acute situatie i.v. worden toegediend (klasse IIb/B).9
De bijwerkingen van chronische toediening van amiodaron zijn bekend, maar er treden zelden ernstige proaritmische problemen op, met uitzondering van bradycardie. Het hoofdprobleem is een verlenging van het QT-interval. Dat is inherent aan het werkingsmechanisme van amiodaron, dat inwerkt op de repolarisatie van de cellen. Een significante verlenging van het QT-interval houdt theoretisch een risico op torsade de pointes in.10,11 Een torsade de pointes treedt echter maar zelden op bij behandeling met amiodaron (in minder dan 1 % van de gevallen).11 Die paradoxaal lage incidentie in verhouding tot het vaak sterke effect van amiodaron op het QT-interval is volgens Antzelevitch toe te schrijven aan een geringere transmurale dispersie van de repolarisatie van het myocard in vergelijking met andere antiaritmica die ook het QT-interval verlengen.12 Torsade de pointes is ook gerapporteerd bij i.v. injectie van amiodaron, met een geraamde incidentie van 1,5 %.13
Enkele jaren geleden, toen de ablatietechnieken nog in hun kinderschoenen stonden, vooral bij atriumfibrillatie, hebben we geprobeerd om het belang van torsade de pointes door amiodaron in de gewone cardiologische praktijk te evalueren. In meerdere cardiologische centra hebben we zo in totaal 8 gevallen van torsade de pointes geregistreerd en gedocumenteerd. In twee gevallen is de torsade de pointes geëvolueerd naar een ventrikelfibrillatie, die gelukkig met succes kon worden behandeld via elektrische conversie (figuur 1).14 De belangrijkste afwijkingen die we daarbij hebben gevonden waren een verminderde myocardfunctie, een significante bradycardie en vaak een ernstige hypokaliëmie.
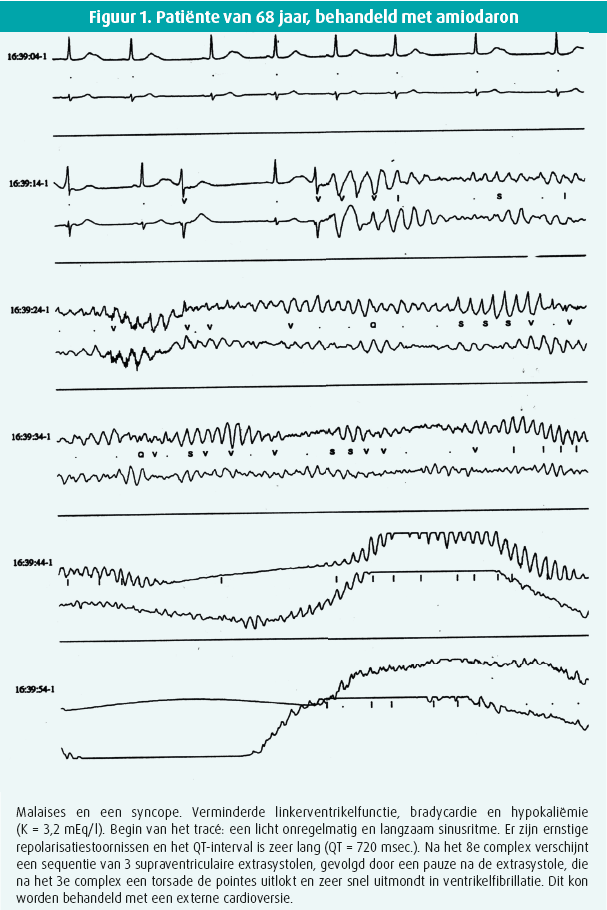
In een noodsituatie wordt vaak amiodaron i.v. toegediend voor acute conversie van een recent ontstane atriumfibrillatie. Dat is echter geen eerstelijnstherapie, aangezien het is bewezen dat het sinusritme minder snel herstelt met amiodaron dan met andere antiaritmica.15 Amiodaron verlaagt ook het kamerantwoord, wat ook positief is. Toediening van amiodaron voor conversie van atriumfibrillatie in een acute situatie is dus vooral geïndiceerd bij patiënten met een verminderde linkerventrikelfunctie en patiënten bij wie andere antiaritmica zoals flecaïnide en propafenon gecontra-indiceerd zijn (klasse I/A).9
Atriumfibrillatie en accessoire bundel
Atriumfibrillatie bij een patiënt met een accessoire bundel kan indrukwekkende elektrocardiografische tracés geven en uitmonden in gevaarlijke situaties, gezien de uiterst snelle geleiding van de atriale prikkels naar de ventrikels. De accessoire bundels bestaan immers uit myocardvezels zonder remmende eigenschappen, in tegenstelling tot de atrioventriculaire (AV) knoop (figuur 2).
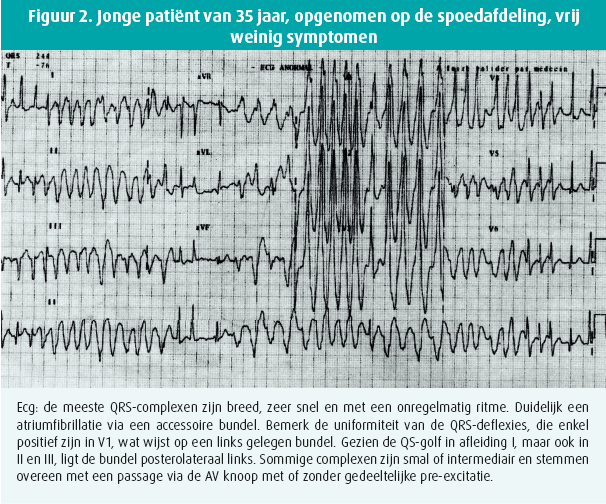
Een verrassende vaststelling is dat de richtlijnen van het ACC, de AHA en de ESC van 2006 nog een plaats zagen voor amiodaron bij de acute behandeling van een hemodynamisch stabiele atriumfibrillatie in geval van een snel geleidende accessoire bundel, ook al maanden ze aan tot voorzichtigheid (klasse IIb/B).16 De ESC-richtlijnen van 2019 en die van het ACC, de AHA en de ESC van 2020 daarentegen stellen dat amiodaron formeel gecontra-indiceerd is (klasse III-richtlijn),8,9 aangezien meerdere publicaties gewagen van een snellere geleiding via de accessoire bundel en eventueel evolutie naar ventrikelfibrillatie.17-19 En het is een klasse III-richtlijn gebleven, ondanks rapporten die toch stellen dat amiodaron een gunstig effect heeft in die situaties en veilig is.20
In tegenstelling tot de andere geneesmiddelen die de atrioventriculaire geleiding vertragen (niet-dihydropyridin calciumantagonisten, bètablokkers, digitalis ...), die ook gecontra-indiceerd zijn tijdens de acute fase van een atriumfibrillatie met een patente accessoire bundel, is het mogelijke risico van amiodaron in die situaties minder duidelijk. Gezien het vermoeden dat amiodaron veilig was en het gunstige effect van amiodaron op de refractaire periode van de accessoire bundel was amiodaron theoretisch ideaal om die ritmestoornissen te behandelen.21,22 De internationale richtlijnen spreken nu van een klasse III-richtlijn, wat een einde maakt aan alle onduidelijkheid.8,9 Die beslissing wordt weliswaar niet aangevochten, maar stoelt toch vooral op de beschrijving van enkele vrij zeldzame gevallen van snellere geleiding via de accessoire bundel en een mogelijke evolutie naar letale ventriculaire ritmestoornissen.
Hoe onderscheidt amiodaron per os zich van amiodaron intraveneus?
Het is a priori niet meteen duidelijk waarom intraveneuze injectie van amiodaron tijdens de acute fase meer risico's met zich meebrengt dan chronische toediening. Amiodaron per os heeft een krachtige, maar complexe werking door in te werken op de verschillende ionenkanalen van het myocard. De antiaritmische werking bij chronische toediening van amiodaron zou grotendeels toe te schrijven zijn aan zijn metaboliet, desethylamiodaron, wat niet het geval is bij intraveneuze toediening. Amiodaron per os werkt grotendeels in op de AV geleiding en heeft ook een sterk effect op de anterograde refractaire periode van de accessoire bundels.21,22 Dat laatste is trouwens de reden geweest waarom amiodaron zo vaak werd voorgeschreven in die indicaties. Met de ontwikkeling van ablatietechnieken is dat echter sterk veranderd.
I.v. injectie van amiodaron zou een matig, maar reëel effect hebben op de refractaire periode van de AV knoop, wat misschien vooral toe te schrijven is aan de indirecte bètablokkerende werking van amiodaron. Die laatste zou ten dele verantwoordelijk zijn voor de vertraging van de atriale potentialen via de AV knoop. Dat mechanisme zou in geval van een accessoire bundel, net zoals bij gebruik van andere antiaritmica die de AV knoop afremmen, het aantal potentialen verminderen dat naar de ventrikels wordt geleid, en zodoende ook de verborgen retrograde geleiding (concealed conduction) in de accessoire bundel. Het is bekend dat dat fenomeen een snellere anterograde passage van de atriumfibrillatie via de accessoire bundel bevordert. Maar volstaat dat mechanisme om de snellere geleiding bij i.v. toediening van amiodaron uit te leggen? Amiodaron i.v. verlengt immers ook de refractaire periode in de accessoire bundel,21,22 ook al neemt de refractaire periode meer toe bij orale dan bij i.v. toediening van amiodaron. Door dat gunstige effect op de refractaire periode heeft amiodaron, waarschijnlijk ten onrechte, de reputatie gekregen dat het zeer veilig is in die indicaties. Maar zoals eerder al vermeld zijn meerdere gevallen van toename van het kamerantwoord via de accessoire bundel beschreven na i.v. injectie.17-19 Dat is waarschijnlijk toe te schrijven aan het feit dat amiodaron bij i.v. injectie de bloeddruk verlaagt, maar vooral aan de hulpstoffen, zoals polysorbaat 80 en benzylalcohol, die in de oplossing voor amiodaron i.v. zitten. De hypotensie zou een reflexmatige adrenerge reactie opwekken. Dat zou inderdaad een mogelijke verklaring kunnen zijn voor de snellere geleiding via de accessoire bundel.17 Dat lijkt misschien tegenstrijdig, gezien de bètablokkerende werking die amiodaron zou uitoefenen op de AV knoop. Een sterke bloeddrukdaling kan een sterke adrenerge reactie opwekken, vooral na te snelle i.v. toediening, zeker als de hemodynamische situatie al precair is. In geval van een soms verontrustend ecg-tracé, een uiterst snel ritme met brede QRS-complexen, zullen artsen in een urgentie geneigd zijn sneller naar amiodaron te grijpen en amiodaron te snel toe te dienen.
Nog een belangrijk argument tegen i.v. toediening van amiodaron in die indicatie is dat amiodaron niet meteen werkt bij conversie van een atriumfibrillatie in de acute fase, los van een eventuele accessoire bundel. We hebben al onderstreept dat amiodaron geen eerstelijnstherapie is voor acute conversie van een atriumfibrillatie, en al zeker niet als er een accessoire bundel is.
Samengevat: i.v. toediening van amiodaron wegens een atriumfibrillatie met een patente accessoire bundel is gecontra-indiceerd, gezien het gevaar voor evolutie naar mogelijk letale ventriculaire ritmestoornissen, iets wat echter maar zelden gebeurt.
Acute behandeling van atriumfibrillatie met een snel kamerantwoord via een accessoire bundel
Als de situatie hemodynamisch ernstig is, moet meteen een cardioversie worden uitgevoerd. Buiten die uiterst dringende situatie kan atriumfibrillatie via een accessoire bundel worden behandeld met een klasse IC-antiaritmicum zoals flecaïnide (1-2 mg/kg in een infuus) of propafenon (2 mg/kg in een infuus).9, 25, 26 Die geneesmiddelen bereiken hun maximale effect pas na 15 tot 30 minuten. Ter herinnering: ze zijn gecontra-indiceerd in geval van een verminderde linkerventrikelfunctie en significant hartlijden. Desondanks moeten enkele voorzorgsmaatregelen worden genomen, gezien een mogelijke invloed op de nodale en infranodale AV geleiding.
Ajmaline, een klasse IA-antiaritmicum, langzaam i.v. in een dosering van 1 mg/kg (10 mg/min.), een geneesmiddel dat elektrofysiologen goed kennen maar in meerdere landen niet in de handel te verkrijgen is, kan een alternatief zijn. Ajmaline, dat in de praktijk ten onrechte weinig gebruikt wordt, heeft een snelle en vaak zeer effectieve werking. De voordelen van ajmaline zijn de snelle werking (enkele minuten, maar variabel naargelang de situatie) en de zeer korte eliminatiehalfwaardetijd (13 minuten), zodat er zeer makkelijk mee te werken is. Ajmaline heeft weinig negatieve hemodynamische effecten. Dat alles maakt een vrij soepel gebruik mogelijk.25, 26 Ter herinnering: ajmaline wordt vaak gebruikt bij de evaluatie van de elektrofysiologische eigenschappen van accessoire bundels, en vooral bij het ramen van de refractaire periode.27
Klassse IA- en klasse IC-antiaritmica werken over het algemeen vrij snel, vooral ajmaline. Ze verlengen de refractaire periode van de accessoire bundel, wat zich bijvoorbeeld uit in het verminderen of verdwijnen van de pre-excitatie op ecg-tracés in fibrillatie. Nog een ander voordeel van die antiaritmica is dat ze een atriumfibrillatie kunnen omzetten in een sinusritme, waardoor de patiënt meteen uit de gevarenzone raakt. Het percentage conversie is zeer hoog, aangezien de atriumfibrillatie in deze gevallen bijna altijd recent is ontstaan. Soms herstelt eerst het sinusritme voordat de pre-excitatie verdwijnt.
Ecg: differentiële diagnose
Ecg in atriumfibrillatie met passage via een accessoire bundel
Atriumfibrillatie met passage via een accessoire bundel wordt vaak beschreven als een (zeer) snel, onregelmatig ritme met brede QRS-complexen (figuur 2). Sommige specifieke kenmerken onderscheiden die situatie van andere ritmestoornissen die erop zouden kunnen gelijken. In dit geval is het ritme werkelijk onregelmatig en zeer snel, door een preferentiële of exclusieve passage via de accessoire bundel, die uit spiervezels zonder remmende eigenschappen bestaat. Het kleinste interval tussen 2 verbrede QRS-complexen is soms uiterst kort, soms korter dan 200 msec. Die RR-intervallen kunnen een idee geven van de refractaire periode van de accessoire bundel. De vorm van het QRS-complex kan verschillen en soms zijn er ook smalle complexen. De brede QRS-complexen wijzen dan op een preferentiële of volledige passage via de accessoire bundel. De smalle complexen stemmen overeen met exclusieve geleiding via de AV knoop en de intermediaire complexen zijn fusiecomplexen als gevolg van gelijktijdige geleiding via de AV knoop en de accessoire bundel.
Een accessoire bundel resulteert in een uniforme oriëntatie van de deflexies van de brede QRS-complexen, wat bijzonder duidelijk is in afleiding V1 (figuur 2). De brede QRS-complexen wijzen dus op een maximale pre-excitatie. Zo kan men nagaan of hun vorm strookt met de aanwezigheid van een accessoire bundel, en waar de bundel zich precies bevindt. Een negatieve concordantie (QS) in de precordiale afleidingen strookt bijvoorbeeld geenszins met een accessoire bundel.
Atriumfibrillatie met aberrante geleiding zonder passage via een accessoire bundel
De RR-intervallen zijn in dit geval per definitie ook onregelmatig, maar het kortste RR-interval is zelden korter dan 240-250 msec. Exclusieve passage via de AV knoop is immers een natuurlijke filter voor geleiding naar de ventrikels. Dat is toe te schrijven aan de specifieke kenmerken van de cellen van de AV knoop en aan het bestaan van onvolledige geleiding in de AV knoop, wat een te snelle opeenvolging van potentialen verhindert (verborgen geleiding/concealed conduction). De QRS-complexen bij een aberrante geleiding vertonen over het algemeen de kenmerkende vorm van een klassiek bundeltakblok. Op lange tracés vindt men niet zelden alternerend een aberrante geleiding van het type rechterbundeltakblok en van het type linkerbundeltakblok. Intermediaire vormen wijzen op een partiële aberrante geleiding. Tracés van een atriumfibrillatie met aberrante geleiding zijn dus goed te onderscheiden van tracés van een atriumfibrillatie via een accessoire bundel (figuur 3).
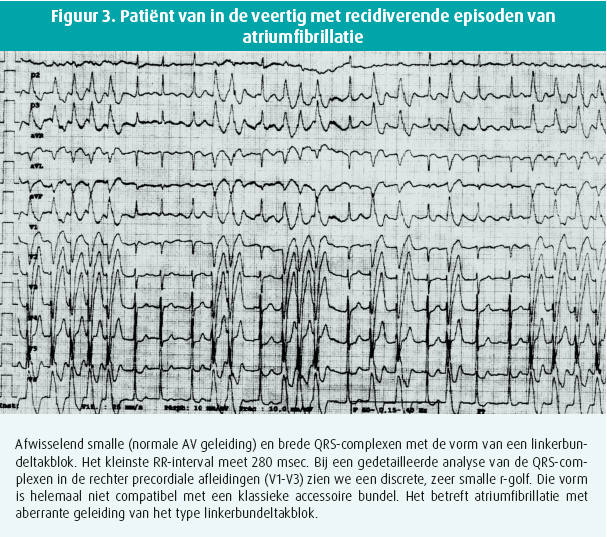
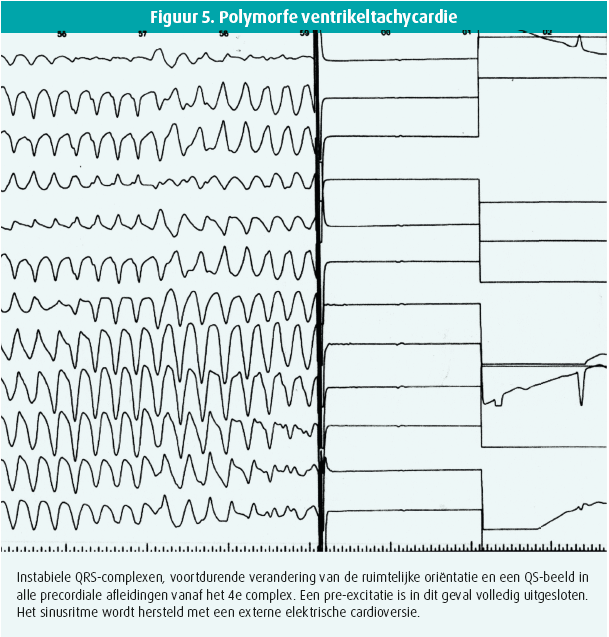
Polymorfe ventrikeltachycardie
Bij patiënten met een significant hartlijden en vooral ischemisch hartlijden toont het ecg soms snelle ventriculaire ritmestoornissen met een soms zeer korte koppeling, die kunnen doen denken aan atriumfibrillatie via een accessoire bundel, als de episoden lang duren.
In die situaties is de kliniek vaak vrij duidelijk. Deze ventriculaire ritmestoornissen duren zelden lang, tenzij ze levensbedreigend zijn. De vorm van de QRS-complexen is per definitie zeer wisselend en er is geen uniforme oriëntatie zoals kan worden gezien bij een accessoire bundel (figuur 4 en 5).
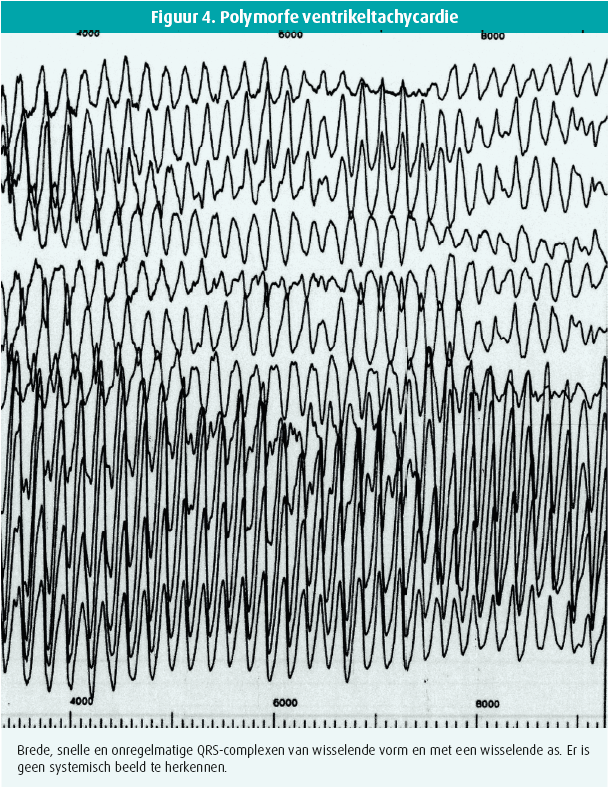
Torsade de pointes
Een torsade de pointes is ook een zeer snel ritme met brede QRS-complexen. De vorm van de QRS-complexen is zeer wisselend en de complexen draaien om de basislijnen met een zeer kenmerkend beeld van verandering van richting van de ventrikelactiviteit (omkering van punten). Ook dat is helemaal niet compatibel met pre-excitatie (figuur 1).
Conclusie
Sinds de ontwikkeling van ablatietechnieken wordt amiodaron veel minder vaak voorgeschreven bij de behandeling van supraventriculaire ritmestoornissen. Toch zijn er nog altijd enkele specifieke indicaties voor amiodaron, vooral bij de preventie van recidief van atriumfibrillatie. Atriumfibrillatie met een snelle geleiding via een accessoire bundel komt weinig voor, maar intraveneuze toediening van amiodaron is dan formeel gecontra-indiceerd. Amiodaron wordt vaak in een urgentie toegediend omdat het bekendstaat als een veilig geneesmiddel. In uitzonderlijke gevallen kan amiodaron echter letale ventriculaire ritmestoornissen veroorzaken. In die gevallen zijn klasse IC- of klasse IA-antiaritmica te verkiezen, tenzij in geval van hemodynamische instabiliteit. Dan is een snelle elektrische cardioversie wenselijk.
Referenties
- Vaughan Williams, E.M.A. Classification of Antiarrhythmic Actions Reassessed after a Decade of New Drugs, J Clin Pharmacol, 1984, 24 (4), 129-147.
- Task Force of the Working Group on Arrhythmias of the European Society of Cardiology. The Sicilian Gambit, Circulation, 1991, 84, 1831-1851.
- Hamilton, D., Nandkeolyar, S., Lan, H., Desai, P., Evans, J., Hauschild, C. et al. Amiodarone, a Comprehensive Guide for Clinicians. Am J Cardiovascular Drugs, 2020, 20, 549-558.
- Zipes, D., Prystowsky, E., Heger, J. Amiodarone: Electrophysiologic Actions, Pharmacokinetics and Clinical effects. J Am Coll Cardiol, 1984, 3, 1059-1071.
- von Kemp, M., Vermeersch, G., Schwagten, B. Wanneer amiodaron niet het juiste antwoord is … Tijdschr Cardiol, 2022, 34 (6), 25-28.
- ACC/AHA/ESC guidelines for the management of patients with supraventricular arrhythmias. J Am Coll Cardiol, 2003, 42, 1493-1531.
- Rosenbaum, M.B., Chiale, P.A., Ryba, D., Elizari, M. Control of Tachyarrhythmias associated with Wolff-Parkinson-White Syndrome by Amiodarone Hydrochloride. Am J Cardiol, 1974, 34, 215-223.
- Brugada, P., Katritsis, D.G., Arbelo, E., Arribas, F., Bax, J.J., Blomström-Lundqvist, C. et al. 2019 ESC Guidelines for the management of patients with supraventricular tachycardias. Eur Heart J, 2019, 00, 1-65.
- 2020 ESC Guidelines for the diagnosis and Management of Atrial Fibrillation. Eur Heart J, 2020, 42, 373-498.
- Kirchhof, P., Franz, M., Bardai, A., Wilde, A. Giant T-U Waves precede Torsades de Pointes in Long QT Syndrome. J Am Coll Cardiol, 2009, 54, 143-149.
- Hohnloser, S., Klingenheben, T., Singh, B. Amiodarone-associated Proarrhythmic Effects. Ann Intern Med, 1994, 121, 529-535.
- Antzelevitch, C. Role of transmural dispersion of repolarisation in the genesis of drug-induced torsades de pointes. Heart Rhythm, 2005, 2 (suppl), S9-15.
- Shenthar, J., Rachaiah, J., Pillai, V., Chakali, S., Balasubramanian, V., Nanjappa, M. Incidence of drug-induced torsades de pointes with intravenous amiodarone. Indian Heart J, 2017, 69, 707-713.
- Scavee, C., Blommaert, D., Mairesse, G., Nanan, A., de Meester, A., De Roy, L. Torsades de Pointes after Amiodarone administration. Acta Cardiologica, 2001, 56, 332.
- Chevalier, P., Durand-Dubief, A., Burri, H., Cucherat, M., Kirkorian, G., Touboul, P. Amiodarone versus placebo and class IC drugs for cardioversion of recent onset atrial fibrillation: a meta-analysis. J Am Coll Cardiol, 2003, 41, 255-262.
- ACC/AHA/ESC 2006 guidelines for the management of patients with atrial fibrillation. Europace, 2006, 6, 651-745.
- Boriani, G., Biffi, M., Frabetti, L. et al. Ventricular Fibrillation after intravenous amiodarone in Wolff-Parkinson-White syndrome with atrial fibrillation. Am Heart J, 1996, 131, 1214-1216.
- Schützenberger, W., Leish, F., Gmeiner, R. Enhanced accessory pathway conduction following intravenous amiodarone in atrial fibrillation. A case report. Int J Cardiol, 1987, 16, 93-95.
- Tijunels, M.A., Herbert, M.E. Myth: Intravenous amiodarone is safe in patients with atrial fibrillation and Wolff-Parkinson- White syndrome in the emergency department. CEJM, 2005, 7, 262-265.
- Ren, J., Yang, Y., Zhu, J., Wu, S., Wang, J., Zhang. H., Shao, X. The use of intravenous amiodarone in patients with atrial fibrillation and Wolff-Parkinson-White syndrome. Pacing Clin Electrophysiol, 2021, 44, 35-43.
- Wellens, H.J.J., Brugada, P., Abdollah, H., Dassen, W. A comparison of the electrophysiologic effects of intravenous and oral amiodarone in the same patient. Circulation, 1984, 69, 120-124.
- Feld, G.K., Nademanee, K., Stevenson, W., Weiss, J., Klitzner, T., Singh, B.N. Clinical and electrophysiologic effects of amiodarone in patients with atrial fibrillation complicating the Wolff-Parkinson-White syndrome. Am Heart J, 1988, 115, 102-107.
- Nunain, S., Garrat, C., Linker, N., Gill, J., Ward, D., Camm, A.J. A comparison of intravenous Propafenone and flecainide in the treatment of tachycardias associated with the Wolff- Parkinson-White Syndrome. Pace, 1991, 14, 2028-2034.
- Boahene, K., Klein, G., Yee, R., Sharma, A., Fujimura, O. Termination of acute atrial Fibrillation in the Wolff-Parkinson-White Syndrome by Procainamide and Propafenone: Importance of Atrial Fibrillatory Cycle length. J Am Coll Cardiol, 1991, 16, 1408-1414.
- Aronson, J.K. Ajmaline and its derivates. Meyler's Side Effects of Drugs, 2016, 7th Ed.
- Zipes, D. Therapy for cardiac arrhythmias. Braunwald's Heart Disease: A textbook of Cardiovascular Medicine, 2019.
- Wellens, H.J.J., Bar, F., Gorgels, A., Vanagt, E. Use of ajmaline in patients with the Wolff- Parkinson-White syndrome to disclose short refractory period of the accessory pathway. Am J Cardiol, 1980, 45, 130-133.
Niets van de website mag gebruikt worden voor reproductie, aanpassing, verspreiding, verkoop, publicatie of commerciële doeleinden zonder voorafgaande schriftelijke toestemming van de uitgever. Het is ook verboden om deze informatie elektronisch op te slaan of te gebruiken voor onwettige doeleinden.