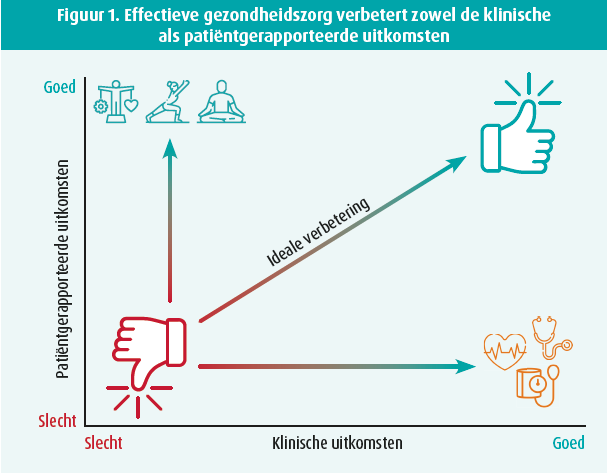
Patiëntgerapporteerde uitkomsten (PRO's) zijn een gestandaardiseerde manier om het perspectief van patiënten over hun gezondheid in kaart te brengen. PRO's worden gedefinieerd als 'elke rapportage over de gezondheidstoestand van een patiënt die rechtstreeks van de patiënt komt, zonder interpretatie door een clinicus of iemand anders'.1 Samen met klinische uitkomsten geven PRO's het volledige beeld van zorgresultaten weer. Idealiter is de gezondheidszorg gericht op het verbeteren van zowel klinische uitkomsten als PRO's2 (figuur 1).
Terwijl PRO's aanvankelijk werden gebruikt voor beschrijvend klinisch onderzoek en populatiegebaseerde enquêtes, vonden ze geleidelijk hun weg naar de klinische praktijk.3, 4 PRO's zijn van bijzonder belang voor het monitoren en het management van chronische aandoeningen die de levenskwaliteit beïnvloeden. Ze kunnen worden gebruikt voor individuele beoordeling ter ondersteuning van medische besluitvoering en om aspecten van de zorgkwaliteit te evalueren.5-8 Bovendien worden PRO's steeds vaker gebruikt om behandelingen en interventies in klinische onderzoeken te beoordelen, waardoor beslissingen over regelgeving en terugbetaling voor geneesmiddelen en medische hulpmiddelen worden onderbouwd.9-13 Het gebruik van PRO's is echter niet zonder methodologische uitdagingen; er zijn hiaten tussen de beschikbare evidentie en de implementatie in de klinische praktijk.14, 15
Om het gebruik en de verdere ontwikkeling van PRO's te ondersteunen heeft de Europese Vereniging voor Cardiologie (ESC) een consensusdocument opgesteld.16 Hierin wordt gedefinieerd wat PRO's zijn en hoe ze kunnen worden gemeten, en beschreven hoe PRO's verder kunnen worden geïntegreerd in cardiovasculair onderzoek, de klinische praktijk, regelgeving en beslissingen omtrent terugbetalingen. In dit artikel zullen we de voornaamste aspecten van dit consensusdocument bespreken.
Wat zijn PRO's?
Hoewel de definitie van PRO's door de U.S. Food and Drug Administration (FDA), zoals hierboven geciteerd, algemeen aanvaard is, is er minder consensus over de componenten van PRO's. Volgens deze definitie hebben PRO's betrekking op de status van de gezondheidstoestand van een patiënt zoals direct gerapporteerd door de patiënt.1 Deze door de patient gerapporteerde gezondheidsstatus kan symptomen, functionele status en gezondheidsgerelateerde levenskwaliteit (HRQoL) omvatten.17 Toch zijn er nog andere uitkomsten relevant, zoals een globale indruk van de levenskwaliteit, gezondheidsgedrag, en ervaringen met zorg (figuur 2).18 Deze uitbreidingen leiden tot de volgende definitie van PRO's: 'elke rapportage over de gezondheidstoestand, het gezondheidsgedrag of de ervaring met de gezondheidszorg van een patiënt die rechtstreeks van de patient komt, zonder interpretatie van een clinicus of iemand anders'.19, 20 Deze uitgebreide definitie was de eerste die expliciet patiëntervaringen opnam als PRO's. Belangrijk is dat patiëntervaringen hier verwijzen naar ervaringen met de zorgprocessen, en geen betrekking hebben op de hotelfunctie van zorginstellingen.

Hoe worden PRO's gemeten?
PRO's worden meestal gemeten met behulp van vragenlijsten, ook wel patientgerapporteerde meetinstrumenten (PROM's) genoemd. Ervaringen met de zorg kunnen worden gemeten met behulp van patiëntgerapporteerde ervaringsmetingen (PREM's).
Er zijn drie soorten PROM's: generieke, ziektespecifieke en domeinspecifieke instrumenten.5 Er wordt geadviseerd om deze soorten PROM's in combinatie te gebruiken omdat ze complementaire informatie geven.21 Generieke PROM's bestaan uit vragen die algemeen van aard zijn en daarom kunnen worden gebruikt in elke populatie van respondenten. Dergelijke generieke PROM's worden meestal gekozen om verschillende patiëntenpopulaties, patiënten met verschillende mate van comorbiditeiten en patiëntengroepen met gezonde controles te vergelijken. Generieke PROM's zijn meestal multidimensionaal en omvatten een breed scala aan functionele domeinen, zoals mobiliteit, emoties of zelfzorg. Voorbeelden van veelgebruikte generieke PROM's zijn de EuroQol-5 dimensies,22 de SF-3623 of PROMIS.24
Ziektespecifieke PROM's worden gebruikt wanneer uitkomsten met betrekking tot een specifieke aandoening van belang zijn. Dergelijke instrumenten zijn vaak gevoeliger dan algemene PROM's wanneer ze worden gebruikt in een bepaalde patiëntenpopulatie, omdat ze gerichter en gedetailleerder kunnen zijn. De meeste ziektespecifieke PROM's zijn multidimensionaal, zoals de Minnesota Living with Heart Failure (MLHF) Questionnaire25 of de Myocardial Infarction Dimensional Assessment Scale (MIDAS).26
Domeinspecifieke PROM's hebben betrekking op een specifiek symptoom of probleem. Omdat ze een enkel fenomeen meten, zijn ze vaak, maar niet altijd, unidimensioneel en beperkt in omvang, maar ze kunnen verschillende niveaus van diepgang hebben. Een voorbeeld van een domeinspecifieke PROM met weinig diepgang is de unidimensionale visuele analoge schaal voor pijnintensiteit.27 De McGill Pain Questionnaire daarentegen is een multidimensionale domeinspecifieke PROM met meer diepgang, die ontworpen is om de sensorische, affectieve en evaluatieve aspecten van pijn en de intensiteit ervan te meten.27 Sommige domeinspecifieke PROM's zijn ook ziektespecifiek (bijvoorbeeld gezondheidsgedrag bij aangeboren hartaandoeningen).28
In het ESC-consensusdocument wordt een inventaris gemaakt van alle cardiologiespecifieke PROM's.16 De meeste van deze PROM's zijn multidimensionaal, terwijl andere vragenlijsten slechts één construct meten, zoals bijvoorbeeld gezondheidsgedrag.
Hoe kies je de meest geschikte PROM?
Of het nu voor klinische of onderzoeksdoeleinden is, het is belangrijk om PROM's te selecteren die op een efficiënte manier valide en betrouwbare informatie geven. Daarom is een gedegen evaluatie van de eigenschappen van de PROM's essentieel om PROM's van hoge kwaliteit te vinden die passen bij de beoogde doelen.
Gekende evaluatiesystemen voor PROM's zijn de Evaluating the Measurement of Patient-Reported Outcomes-tool (EMPRO),29 en de COnsensus-based Standards for the selection of health Measurement INstruments (COSMIN).30 In deze evaluatiesystemen worden aspecten zoals betrouwbaarheid en validiteit geëvalueerd. De COSMIN is het meest uitgebreide en het meest gebruikte systeem. Terwijl COSMIN diepgaande informatie geeft over de meeteigenschappen, geeft EMPRO een breder perspectief op de PROM door ook de wijze en de belasting van de afname van de vragenlijst te beoordelen. Een ander aspect om in gedachten te houden zijn de voorwaarden van het gebruik van de geselecteerde PROM's. De meeste PROM's kunnen gratis worden gebruikt. Er zijn echter PROM's met zeer strenge regels voor het gebruik ervan en hoge licentiekosten. Het is belangrijk om na te gaan of er goede alternatieven zijn die gratis zijn.
Als er geen relevante PROM voor een specifieke aandoening of probleem bestaat, zijn er drie mogelijke manieren om verder te gaan:31 1) er kan een PROM voor een nauw verwante aandoening worden gebruikt, 2) er kan een generiek instrument worden gebruikt, of 3) er kan een nieuwe PROM worden ontwikkeld.31 De eerste twee opties zijn suboptimaal, maar de laatste optie is tijdrovend en vereist expertise in instrumentontwikkeling en psychometrie.
PRO's in de klinische zorg
Binnen de cardiologie is er groeiende interesse in het gebruik van PROM's, maar de implementatie in de echte klinische praktijk blijft nog beperkt. Het gebruik van PRO's in de klinische praktijk geeft echter de mogelijkheid om symptomen, het functioneren en individuele gezondheidsdoelen van patiënten te kwantificeren. De PROM's kunnen belangrijke informatie geven die het gesprek tussen clinici en patiënten kan sturen, en die kan helpen bij de gedeelde besluitvoering (figuur 3). Verder kunnen PRO's aan gezondheidszorgwerkers een beter beeld geven van het perspectief van elke specifieke patiënt. PRO's beoordelen inderdaad op een systematische manier wat belangrijk is voor patiënten. Belangrijk hierbij is echter dat patiënten het relatieve belang van elke PRO moeten kunnen aangeven. Op die manier geven ze een gewicht aan individuele items op basis van wat voor hen belangrijk is. Het integreren van het relatieve belang van items in PROM's staat nog in de kinderschoenen, maar zou verder moeten worden ontwikkeld om de beoordeling van PRO's meer in lijn te brengen met de voorkeuren van individuele patiënten.

Het gebruik van PRO's geeft ook betere inzichten in de gezondheidsstatus van patiënten.32 Wanneer PRO's cross-sectioneel worden beoordeeld, kunnen ze worden vergeleken met benchmarks voor de populatie. Het is echter ook interessant en valide om PRO's op een longitudinale manier te beoordelen, omdat dit de beoordeling van de evolutie over de tijd mogelijk maakt.
Zorgverleners moeten leren hoe ze de resultaten van PROM's moeten interpreteren en hoe de resultaten kunnen worden geïntegreerd in de zorgprocessen. Informatie van PROM's, die routinematig wordt verzameld via smartphones, patiëntportalen, ziekenhuiskiosken of tablets, moet worden geïntegreerd in het medische dossier op een locatie die gemakkelijk toegankelijk is voor de clinici. Verder is het belangrijk dat clinici de bevindingen met patiënten bespreken.33 Uiteraard vereist dit alles tijd, financiële middelen, personeel en een digitale infrastructuur.
Het ESC-consensusdocument geeft de volgende aanbevelingen voor de verdere ontwikkeling van PRO's in klinische/ gedeelde besluitvorming:
- Artsen moeten zich vertrouwd maken met of worden opgeleid over wat PRO's zijn, hoe ze kunnen worden gebruikt en hoe de gegevens moeten worden geïnterpreteerd.
- Het meten van PRO's moet worden geïntegreerd in de standaard klinische praktijk 1) om individuele patiënten te vergelijken met de populatie en 2) om evoluties van patiënten te beoordelen, zodat de effectiviteit van behandeling en patiëntmanagement kan worden geëvalueerd.
- PROM's moeten zodanig worden aangepast dat patiënten het relatieve belang van elke PRO kunnen aangeven om PRO's voorkeurgevoelig te maken.
- Zorgverleners moeten feedback geven aan patiënten over hun PRO-scores. Het gebruik van PROM's kan het begrip van patiënten vergroten en hun gezondheidsgedrag verbeteren.
- Bij het communiceren van PRO-scores met patiënten wordt het gebruik van visuele analogieën aanbevolen, omdat de meeste mensen beperkte ervaring hebben met het interpreteren van grafieken.
- Managers en bestuurders moeten tijd, personeel, financiële middelen en een digitale infrastructuur ter beschikking stellen voor clinici om hen in staat te stellen evidence-based (gevalideerde) PRO-beoordelingen te implementeren.
- PRO's moeten een plaats krijgen in de ontwikkeling en evaluatie van programma's voor de volksgezondheid.
PRO's in kwaliteitsmonitoring en -verbetering
Er is een groeiend bewustzijn dat PRO's een plaats hebben in de evaluatie van kwaliteit van zorg. Dat komt voor een groot deel vanuit het concept 'value-based healthcare', wat neerkomt op het verbeteren van patiëntrelevante uitkomsten, in verhouding tot de kosten per patiënt om deze verbeteringen te bereiken.34 Bij PRO-gebaseerde performantiemaatstaven wordt de informatie die verzameld is door middel van PROM's of PREM's geaggregeerd, bij voorkeur als ratio.19, 20 Een voorbeeld is het percentage patiënten met depressieve gevoelens, gemeten met de Patient Health Questionnaire-9 (PHQ9), die na zes maanden geen depressieve symptomen meer vertonen. Hoe hoger dit percentage, hoe beter de geleverde zorg, omdat de doelen van de behandeling en zorg zijn bereikt.
Het monitoren van de kwaliteit van zorg kan op regionaal, nationaal of internationaal niveau plaatsvinden. Hiervoor worden kwaliteitsregisters ontwikkeld. Kwaliteitsregisters dienen als benchmark om zorginstellingen/organisaties met elkaar te vergelijken of om de effecten van kwaliteitsverbeteringsprojecten te evalueren. In de meeste landen is nog geen consensus bereikt over welke PRO's te gebruiken voor elke hartaandoening in de nationale klinische registers.
Het ESC-consensusdocument geeft de volgende aanbevelingen voor de verdere ontwikkeling van PRO's in kwaliteitsmonitoring en -verbetering:
- De beoordeling van de kwaliteit van zorg zou PRO-gebaseerde performantiemaatstaven moeten omvatten, die risicogecorrigeerd moeten zijn.
- Professionele richtlijnen, zoals die van de ESC, zouden een beschrijving moeten bevatten van welke PROM's en PREM's zouden kunnen worden gebruikt om de prestaties van, en/of de naleving van, de aanbevelingen te beoordelen.
- Voor klinische registers moet een internationale consensus worden bereikt over welke algemene en ziektespecifieke PROM's en PREM's opgenomen moeten worden voor elke hartaandoening.
PRO's in klinische studies
Het belang van PRO's in klinische studies werd reeds sinds het begin van de jaren 1990 erkend. Zo werd bijvoorbeeld vastgesteld dat complicaties tijdens gerandomiseerde, gecontroleerde studies naar antihypertensiva door artsen slechts 7 % van de symptomen werd gerapporteerd die door patiënten door middel van vragenlijsten werden gerapporteerd.35 Sindsdien hebben steeds meer klinische studies PRO's gebruikt als primaire, secundaire of verkennende/tertiaire eindpunten. In ClinicalTrials.gov steeg het aandeel trials dat PRO's opnam van 14 % in 2004-200736 naar 27 % in 2007-2013.37
In de Australian and New Zealand Clinical Trial Registry had in de periode 2005-2017 45 % van de trials PRO's als eindpunten.38 Dat illustreert dat de waarde van PRO's in klinische trials breed erkend wordt, omdat de typische eindpunten in klinische trials niet altijd een accurate weerspiegeling geven van alle risico's, voordelen, kwaliteit van leven en kosten voor patiënten.39
In klinische onderzoeken moeten PRO-eindpunten vooraf worden bepaald, ethisch worden beoordeeld en worden goedgekeurd in het onderzoeksprotocol. Hiervoor kunnen bestaande 'kernuitkomstensets' worden gebruikt. Het is aangewezen om een expert in psychometrie en klinische interpretaties van PRO's in de onderzoekscommissie te hebben, en om patiënten te betrekken bij het selecteren van geschikte PRO-instrumenten en het ontwerpen van de manier waarop deze instrumenten zullen worden bepaald. Recente voorbeelden zijn de specifieke richtlijnen voor het gebruik van de Seattle Angina Questionnaire en de Kansas City Cardiomyopathy Questionnaire in klinische trials.14, 15
Het ESC-consensusdocument geeft de volgende aanbevelingen voor de verdere ontwikkeling van PRO's in klinische studies:
- PRO-eindpunten moeten a priori worden bepaald en opgenomen in de ethische beoordeling en de onderzoeksregistratie.
- Beoordelingscommissies en adviesraden moeten PRO-expertise hebben.
- Patiënten moeten worden betrokken bij het selecteren van geschikte PRO-instrumenten.
- Richtlijnen voor het gebruik, de analyse en de interpretatie van PRO's in klinische studies moeten worden ontwikkeld.
PRO's voor regelgevende doeleinden
PRO's worden gebruikt voor wettelijke goedkeuring van geneesmiddelen of medische hulpmiddelen. Internationale regelgevende instanties erkennen dat valide, goed gedefinieerde en nauwkeurig verzamelde metingen van PRO's een aanvulling kunnen zijn op bestaande metingen van veiligheid en werkzaamheid van de behandeling, als bewijs voor het maken van regelgevende beslissingen.40
Met betrekking tot geneesmiddelen zijn fundamentele stappen die zijn voorgesteld om de ontwikkeling van geneesmiddelen patiëntgerichter te maken onder andere het betrekken van patiëntvertegenwoordigers tijdens de ontwikkelingscyclus van een geneesmiddel en het identificeren van haalbare patiëntgerichte uitkomsten. De FDA heeft in 2009 richtlijnen over PRO's gepubliceerd, waarin het nut van PRO's wordt beschreven, de beoordeling van PROM's en bijbehorende klinische onderzoeksgegevens worden besproken, en methoden aangehaald om het perspectief van patiënten bij de beoordeling van medische producten te verbeteren.1 In 2019 specificeerde de FDA dat een gunstig effect op symptomen of fysieke functie de basis kan zijn voor het goedkeuren van een geneesmiddel voor de behandeling van hartfalen, zelfs als het geen gunstig effect heeft op overleving of ziekenhuisopnames.41 Daarom worden sponsors van nieuwe trials aangemoedigd om vroegtijdig met de FDA te overleggen om overeenstemming te bereiken over de voorgestelde eindpunten.41 In 2015 stelde het Europees Geneesmiddelenagentschap (EMA) in een richtlijn over het onderzoek naar geneesmiddelen voor acuut hartfalen het volgende: 'Verbetering van de kwaliteit van het leven en/of de zelfbeoordeelde algemene klinische status van patiënten, gebaseerd op gevalideerde ordinale responsmetingen ten opzichte van de uitgangssituatie, kunnen als secundair eindpunt worden gebruikt'.42 In een nieuwe richtlijn van 2017 stelde het EMA dat PRO's moeten worden opgenomen als secundaire eindpunten in studies bij chronisch hartfalen als ze de besluitvorming kunnen ondersteunen. In bijzondere omstandigheden kunnen metingen van symptoomlast ook als primair eindpunt worden gebruikt.43
Het ESC-consensusdocument geeft de volgende aanbevelingen voor de verdere ontwikkeling van PRO's voor regelgevende doeleinden:
- Er moeten minimumeisen worden ontwikkeld voor PROM's die geschikt zijn voor regelgevende doeleinden
- Minimaal klinisch belangrijke verschillen moeten worden bepaald voor alle PROM's die voor regelgevende doeleinden gebruikt (zullen) worden.
PRO's voor terugbetalings- en gezondheidseconomische doeleinden
Er is een toenemend gebruik van PROM's en PREM's bij terugbetalingsbeslissingen in systemen die betalen per prestatie, omdat de kwaliteit van de zorg dan ook wordt beoordeeld door de lens van patiënten.44 Een voorbeeld is het Quality and Outcomes Framework in Groot-Brittannië, waar praktijken in de eerstelijnszorg financieel worden beloond voor het bereiken van kwaliteitsnormen die de ervaringen van patiënten includeren.45 Betaling voor performantie moet rekening houden met de ervaringen van patiënten. Bij vergoedingen op basis van PRO's moet echter rekening worden gehouden met adequate risicoaanpassingen. Als dat niet het geval is, kunnen zorgverleners en praktijken worden gestraft voor de zorg voor ziekere, complexere of sociaal achtergestelde patiënten, die slechtere PRO-scores zullen hebben.
PRO's worden steeds meer erkend als een belangrijk aandachtspunt bij evaluaties van gezondheidstechnologie. Dergelijke evaluatie van gezondheidstechnologie is een dominant raamwerk geworden voor het nemen van beslissingen met betrekking tot de dekking en terugbetaling van nieuwe medische technologieën. Dossiers die bij relevante agentschappen worden ingediend bevatten vaak PRO-gegevens, en informatie over de levenskwaliteit wordt vaak opgenomen in kosteneffectiviteitsanalyses.
Het ESC-consensusdocument geeft de volgende aanbevelingen voor de verdere ontwikkeling van PRO's voor terugbetaling en gezondheidseconomische doeleinden:
- Het gebruik van een breed scala aan PRO's (d.w.z. functionele status, symptomen, dagelijkse levensverrichtingen, empowerment) bij het informeren van beslissingen over vergoeding moet verder worden geëvalueerd.
- Er moet een consensus worden bereikt tussen patiënten, clinici en beleidsmakers over het kiezen van de meest geschikte PROM's.
- Vergoedingen gebaseerd op PRO's moeten rekening houden met risicoaanpassingen en casemix.
- Health Technology Assessment (HTA) zou zowel generieke als ziektespecifieke metingen moeten overwegen om vergelijkingen tussen aandoeningen mogelijk te maken en om de specifieke kenmerken van bepaalde ziektes vast te leggen.
- Er zou een internationale consensus moeten worden bereikt over de geschikte methoden voor het verzamelen van gegevens om geïntegreerde evaluatie van PRO's in de besluitvorming over gezondheid in verschillende landen te bevorderen.
Conclusie
Het gebruik van PRO's geeft inzicht in het perspectief van patiënten. Het ESC-consensusdocument16 heeft tot doel het gebruik van PRO's in de cardiologie te stimuleren door richtlijnen te bieden aan artsen, onderzoekers en beleidsmakers. Adviezen werden gegeven voor toekomstige ontwikkelingen en het optimale gebruik van PRO's bij gedeelde klinische besluitvorming, kwaliteitsmonitoring en -verbetering, klinische studies, beslissingen over regelgeving en terugbetaling. Dit document biedt een raamwerk dat het potentieel van PRO's en het toenemende gebruik ervan zal stimuleren.
Referenties
- US Department of Health and Human Service Food and Drug Administration. Guidance for industry. Patient-reported outcome measures: Use in medical product development to support labeling claims. Silver Spring, MD: Food and Drug Administration, 2009.
- Liu, J.B., Pusic, A.L., Temple, L.K., Ko, C.Y.K. Patient-reported outcomes in surgery: Listening to patients improves quality of life. Bull Am Coll Surg, 2017, 102 (3), 18-23.
- Noonan, V.K., Lyddiatt, A., Ware, P., Jaglal, S.B., Riopelle, R.J., Bingham, C.O., Figueiredo, S. et al. Montreal Accord on Patient-Reported Outcomes (PROs) use series Paper 3: patient-reported outcomes can facilitate shared decision-making and guide self-management. J Clin Epidemiol, 2017, 89, 125-135.
- Bingham, C.O., Noonan, V.K., Auger, C., Feldman, D.E., Ahmed, S., Bartlett, S.J. Montreal Accord on Patient-Reported Outcomes (PROs) use series Paper 4: patient-reported outcomes can inform clinical decision making in chronic care. J Clin Epidemiol, 2017, 89, 136-141.
- Lauck, S.B., Lewis, K.B., Borregaard, B., de Sousa, I. "What Is the Right Decision for Me?" Integrating Patient Perspectives Through Shared Decision-Making for Valvular Heart Disease Therapy. Can J Cardiol, 2021, 37 (7), 1054-1063.
- Basch, E., Barbera, L., Kerrigan, C.L., Velikova, G. Implementation of Patient-Reported Outcomes in Routine Medical Care. Am Soc Clin Oncol Educ Book, 2018, 38, 122-134.
- Spertus, J.A. Understanding How Patients Fare: Insights Into the Health Status Patterns of Patients With Coronary Disease and the Future of Evidence-Based Shared Medical Decision-Making. Circ Cardiovasc Qual Outcomes, 2018, 11 (3), e004555.
- Arbelo, E., Aktaa, S., Bollmann, A., D'Avila, A., Drossart, I., Dwight, J. et al. Quality indicators for the care and outcomes of adults with atrial fibrillation. Europace, 2021, 23 (4), 494-495.
- Squitieri, L., Bozic, K.J., Pusic, A.L. The Role of Patient-Reported Outcome Measures in Value-Based Payment Reform. Value Health, 2017, 20 (6), 834-836.
- Psotka, M.A., von Maltzahn, R., Anatchkova, M., Agodoa, I., Chau, D., Malik, F.I. et al. Patient-Reported Outcomes in Chronic Heart Failure: Applicability for Regulatory Approval. JACC Heart Fail, 2016, 4 (10), 791-804.
- Steinberg, B.A., Dorian, P., Anstrom, K.J., Hess, R., Mark, D.B., Noseworthy, P.A. et al. Patient-Reported Outcomes in Atrial Fibrillation Research: Results of a Clinicaltrials.gov Analysis. JACC Clin Electrophysiol, 2019, 5 (5), 599-605.
- Patrick, D.L., Burke, L.B., Powers, J.H., Scott, J.A., Rock, E.P., Dawisha, S. et al. Patient-reported outcomes to support medical product labeling claims: FDA perspective. Value Health, 2007, 10 Suppl 2, S125-137.
- Fraser, A.G., Nelissen, R., Kjaersgaard-Andersen, P., Szymanski, P., Melvin, T., Piscoi, P. Investigators CM. Improved clinical investigation and evaluation of high-risk medical devices: the rationale and objectives of COREMD (Coordinating Research and Evidence for Medical Devices). Eur Heart J Qual Care Clin Outcomes, 2022, 8 (3), 249-258.
- Spertus, J.A., Jones, P.G., Sandhu, A.T., Arnold, S.V. Interpreting the Kansas City Cardiomyopathy Questionnaire in Clinical Trials and Clinical Care: JACC State-of-the-Art Review. J Am Coll Cardiol, 2020, 76 (20), 2379-2390.
- Thomas, M., Jones, P.G., Arnold, S.V., Spertus, J.A. Interpretation of the Seattle Angina Questionnaire as an Outcome Measure in Clinical Trials and Clinical Care: A Review. JAMA Cardiol, 2021, 6 (5), 593-599.
- Moons, P., Norekval, T.M., Arbelo, E., Borregaard, B., Casadei, B., Cosyns, B. et al. Placing patient-reported outcomes at the centre of cardiovascular clinical practice: implications for quality of care and management. Eur Heart J, 2023, 44 (36), 3405-3422.
- Rumsfeld, J.S., Alexander, K.P., Goff, D.C.Jr., Graham, M.M., Ho, P.M., Masoudi, F.A. et al. Cardiovascular health: the importance of measuring patient-reported health status: a scientific statement from the American Heart Association. Circulation, 2013, 127 (22), 2233-2249.
- Acquadro, C., Berzon. R., Dubois, D., Leidy, N.K., Marquis, P., Revicki, D., Rothman, M. Incorporating the patient's perspective into drug development and communication: an ad hoc task force report of the Patient-Reported Outcomes (PRO) Harmonization Group meeting at the Food and Drug Administration, February 16, 2001. Value Health, 2003, 6 (5), 522-531.
- National Quality Forum. Patient reported outcomes (PRO) in performance measurement. Washington DC: National Quality Forum, 2013.
- Cella, D., Hahn, E.A., Jensen, S.E., Butt, Z., Nowinski, C.J., Rothrock, N., Lohr, K.N. Patient-Reported Outcomes in Performance Measurement. Durham (NC): Research Triangle Institute, 2015.
- Devlin, N.J., Appleby, J. Getting the most out of PROMS: Putting health outcomes at the heart of NHS decision-making. London, UK: The King's Fund, 2010.
- EuroQol Group. EuroQola new facility for the measurement of health-related quality of life. Health Policy, 1990, 16 (3), 199-208.
- Ware, J.E., Snow, K.K., Kosinski, M., Gandek, B. SF36 Health survey: Manual & interpretation guide. Boston: The Health Institute, New England Medical Center, 1993.
- Cella, D., Yount, S., Rothrock, N., Gershon, R., Cook, K., Reeve, B. et al. The Patient-Reported Outcomes Measurement Information System (PROMIS): Progress of an NIH Roadmap Cooperative Group During its First Two Years. Med Care, 2007, 45 (5).
- Rector, T.S., Kubo, S.H., Cohn, J.N. Patients' self-assessment of their congestive heart failure. Part 2: Content, reliability and validity of a new measure, the Minnesota Living with Heart Failure questionnaire. Heart Fail, 1987, 3, 198-209.
- Thompson, D.R., Jenkinson, C., Roebuck, A., Lewin, R.J., Boyle, R.M., Chandola, T. Development and validation of a short measure of health status for individuals with acute myocardial infarction: the myocardial infarction dimensional assessment scale (MIDAS). Qual Life Res, 2002, 11 (6), 535-543.
- Hawker, G.A., Mian, S., Kendzerska, T., French, M. Measures of adult pain: Visual Analog Scale for Pain (VAS Pain), Numeric Rating Scale for Pain (NRS Pain), McGill Pain Questionnaire (MPQ), ShortForm McGill Pain Questionnaire (SFMPQ), Chronic Pain Grade Scale (CPGS), Short Form36 Bodily Pain Scale (SF36 BPS), and Measure of Intermittent and Constant Osteoarthritis Pain (ICOAP). Arthritis Care Res, 2011, 63 (S11), S240-S52.
- Goossens, E., Luyckx, K., Mommen, N., Gewillig, M., Budts, W., Zupancic, N. et al. Health risk behaviors in adolescents and emerging adults with congenital heart disease: psychometric properties of the Health Behavior Scale-Congenital Heart Disease. Eur J Cardiovasc Nurs, 2013, 12 (6), 544-557.
- Valderas, J.M., Ferrer, M., Mendívil, J., Garin, O., Rajmil, L., Herdman, M., Alonso, J. Development of EMPRO: a tool for the standardized assessment of patient-reported outcome measures. Value Health, 2008, 11 (4), 700-708.
- Mokkink, L.B., de Vet, H.C.W., Prinsen, C.A.C., Patrick, D.L., Alonso, J., Bouter, L.M. et al. COSMIN Risk of Bias checklist for systematic reviews of Patient-Reported Outcome Measures. Qual Life Res, 2018, 27 (5), 1171-1119.
- Comins, J.D., Brodersen, J., Siersma, V., Jensen, J., Hansen, C.F., Krogsgaard, M.R. Choosing the most appropriate PROM for clinical studies in sports medicine. Scand J Med Sci Sports, 2021, 31 (6), 1209-1215.
- Sandhu, A.T., Zheng, J., Kalwani, N.M., Gupta, A., Calma, J., Skye, M. et al. Impact of Patient-Reported Outcome Measurement in Heart Failure Clinic on Clinician Health Status Assessment and Patient Experience: A Substudy of the PROHF Trial. Circ Heart Fail, 2023, 16 (2), e010280.
- Wohlfahrt, P., Zickmund, S.L., Slager, S., Allen, L.A., Nicolau, J.N., Kfoury, A.G. et al. Provider Perspectives on the Feasibility and Utility of Routine Patient-Reported Outcomes Assessment in Heart Failure: A Qualitative Analysis. J Am Heart Assoc, 2020, 9 (2), e013047.
- Porter, M.E. A strategy for health care reform-toward a value-based system. N Engl J Med, 2009, 361 (2), 109-112.
- Anderson, R.B., Testa, M.A. Symptom distress checklists as a component of quality of life measurement: Comparing prompted reports by patient and physician with concurrent adverse event reports via the physician. Drug Inf J, 1994, 28, 89-114.
- Scoggins, J.F., Patrick, D.L. The use of patient-reported outcomes instruments in registered clinical trials: evidence from ClinicalTrials. gov. Contemp Clin Trials, 2009, 30 (4), 289-292.
- Vodicka, E., Kim, K., Devine, E.B., Gnanasakthy, A., Scoggins, J.F., Patrick, D.L. Inclusion of patient-reported outcome measures in registered clinical trials: Evidence from ClinicalTrials.gov (20072013). Contemp Clin Trials, 2015, 43, 1-9.
- Mercieca-Bebber, R., King, M.T., Calvert, M.J., Stockler, M.R., Friedlander, M. The importance of patient-reported outcomes in clinical trials and strategies for future optimization. Patient Relat Outcome Meas, 2018, 9, 353-367.
- Warsame, R., D'Souza, A. Patient Reported Outcomes Have Arrived: A Practical Overview for Clinicians in Using Patient Reported Outcomes in Oncology. Mayo Clin Proc, 2019, 94 (11), 2291-2301.
- Kuehn, C.M. A Proposed Framework for Patient-Focused Policy at the U.S. Food and Drug Administration. Biomedicines, 2019, 7 (3), 64.
- US Department of Health and Human Service Food and Drug Administration. Treatment for Heart Failure: Endpoints for Drug Development: Guidance for Industry. Silver Spring, MD: Food and Drug Administration, 2019.
- European Medicines Agency. Guideline on clinical investigation of medicinal products for the treatment of acute heart failure (CPMP/EWP/2986/03 Rev. 1). London, UK, European Medicines Agency, 2015.
- European Medicines Agency. Guideline on clinical investigation of medicinal products for the treatment of chronic heart failure (CPMP/EWP/235/95, Rev.2). London, UK, European Medicines Agency, 2017.
- Wasson, J.H., Sox, H.C., Miller, H.D. Aligning Payments, Services, and Quality in Primary Care. JAMA, 2021.
- Roland, M. Linking physicians' pay to the quality of care--a major experiment in the United kingdom. N Engl J Med, 2004, 351 (14), 1448-1454.
Niets van de website mag gebruikt worden voor reproductie, aanpassing, verspreiding, verkoop, publicatie of commerciële doeleinden zonder voorafgaande schriftelijke toestemming van de uitgever. Het is ook verboden om deze informatie elektronisch op te slaan of te gebruiken voor onwettige doeleinden.