D'après l'exposé des Pr W. Desmet et O. Gach, intitulé 'From the new guidelines to clinical practice: interactive case presentations of high risk MI patients with diabetes or CKD', présenté le 9 février 2018 à l'occasion du 37e congrès de la Belgian Society of Cardiology
En 2017, l'ESC a publié ses nouvelles recommandations pour l'utilisation de la bithérapie antiplaquettaire (DAPT).1 La possibilité de poursuivre la DAPT 1 an après un syndrome coronarien aigu (ACS), sous la forme d'une dose réduite de ticagrélor (2 x 60 mg/jour) en association avec l'acide acétylsalicylique, a ainsi été intégrée en classe IIb dans ces recommandations. Cette option ne s'applique toutefois qu'aux patients à haut risque, c'est-à-dire les patients âgés de plus de 65 ans, les patients atteints d'un diabète sucré, les patients pluritronculaires (> 50 % de sténose dans minimum 2 vaisseaux), les patients avec antécédents d'infarctus du myocarde et les patients souffrant de néphropathie chronique. Lors de la session de la BSC, les professeurs W. Desmet et O. Gach ont détaillé les preuves relatives à 2 de ces groupes à haut risque au moyen d'une étude de cas.
Le patient atteint d'insuffisance rénale chronique (Pr W. Desmet)
Le Pr Desmet a présenté un premier cas, concernant un patient de 72 ans avec insuffisance rénale modérée et NSTEMI. Les recommandations reprennent différents critères susceptibles d'être appliqués pour distinguer les patients avec syndrome coronarien aigu (ACS) associés à un risque cardiovasculaire très élevé des patients à risque faible, intermédiaire ou élevé. Cette stratification du risque détermine entre autres la nécessité et le timing d'éventuelles procédures invasives. L'insuffisance rénale est en soi considérée comme un facteur de risque intermédiaire. Pour le reste, plusieurs scores sont à disposition pour orienter la pratique clinique. Ainsi, le score SYNTAX donne une idée du risque ischémique du patient, tandis que les scores PRECISE-DAPT et DAPT sont utilisés pour évaluer le risque hémorragique du patient individuel et éventuellement adapter la durée de la DAPT.1 Comme l'a illustré le Pr Desmet, ces scores peuvent néanmoins varier à court terme, en conséquence de petites fluctuations quotidiennes de paramètres déterminants, si bien qu'une évaluation clinique reste essentielle.
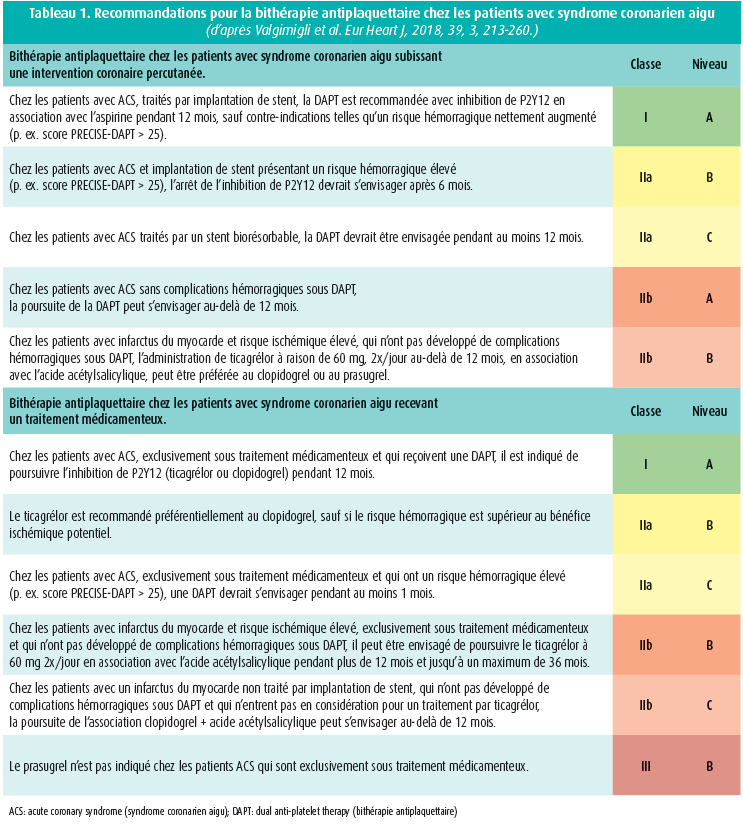
Se fondant sur les résultats de l'étude PEGASUS, les recommandations de 2017 sur la DAPT préconisent une DAPT réduite, sur la base de 2 x 60 mg de ticagrélor par jour, en association avec l'acide acétylsalicylique, chez les patients à haut risque après un infarctus du myocarde, à condition qu'ils n'aient pas connu de complications hémorragiques durant les 12 premiers mois (tableau 1).1, 2 Dans cette étude, les patients à haut risque étaient inclus jusqu'à 2 ans maximum après un infarctus aigu du myocarde, et traités par l'acide acétylsalicylique en monothérapie ou par l'association d'acide acétylsalicylique et d'une dose réduite de ticagrélor (2 x 60 mg/jour), et ce jusqu'à 3 ans après l'infarctus. Une réduction du risque relatif de 20 % a été atteinte pour le critère d'évaluation principal composé de la mortalité cardiovasculaire, de l'infarctus du myocarde et de l'AVC. Cette réduction s'est accompagnée d'une augmentation significative des hémorragies majeures selon les critères TIMI, toutefois sans différence significative au niveau des hémorragies intracrâniennes ou fatales. Le bénéfice maximum était par ailleurs obtenu en cas de poursuite de la DAPT à faible dose 1 an après l'infarctus du myocarde. La réduction observée pour le critère d'évaluation principal est même plus importante pour les patients souffrant de néphropathie chronique que pour le groupe à fonction rénale normale, mais, comme on peut s'y attendre, elle s'accompagne d'une augmentation des saignements, certes proportionnelle dans les deux groupes et à nouveau sans différence significative entre le ticagrélor et l'acide acétylsalicylique.3 Le Pr Desmet a dès lors souligné l'importance de bien soupeser le risque hémorragique et le risque ischémique pendant l'hospitalisation de référence et de signaler, dès ce moment, les candidats à une DAPT à dose réduite. Cette éventualité est, bien sûr, soumise à la condition d'une bonne tolérance de la DAPT 'à forte dose' pendant la première année.
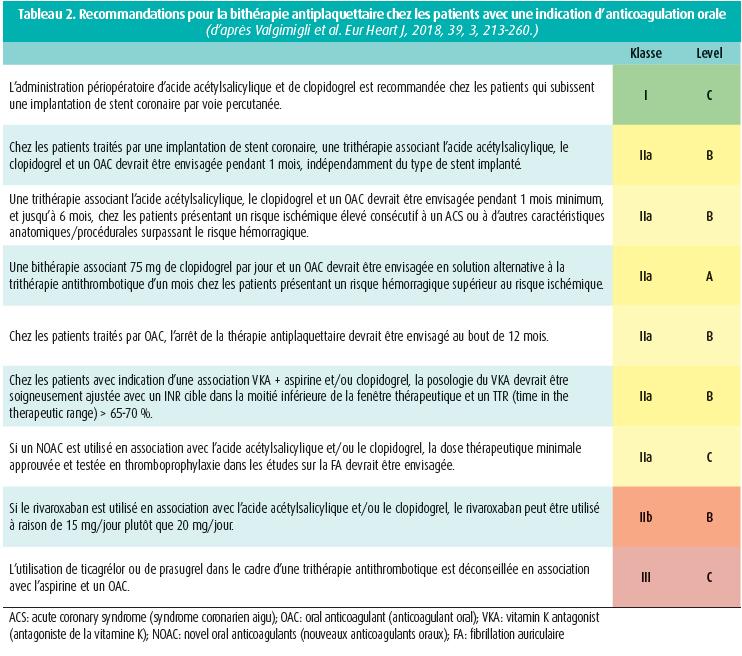
Le deuxième cas présenté concernait un STEMI aigu chez un patient avec insuffisance rénale chronique et indication d'anticoagulation orale (score CHA2DS2VASc 3/9). Conformément aux recommandations, l'auditoire s'accordait à l'unanimité sur l'instauration d'une thérapie antiplaquettaire en traitement aigu avant d'adresser le patient pour une coronarographie diagnostique en urgence. Pour ce faire, 33 % des personnes présentes utilisent le clopidogrel dans de telles circonstances, les 67 % restants préférant le ticagrélor. Les options en matière de traitement à long terme étaient cependant plus diverses, variant entre les associations avec le clopidogrel (33 %) ou le ticagrélor (43 %), et ce tant en bithérapie qu'en trithérapie avec l'acide acétylsalicylique et des anticoagulants oraux. En cas d'utilisation de ticagrélor, 66 % poursuivraient en outre également le traitement jusqu'à 1 an. Pour les patients présentant une indication d'anticoagulation orale et de PCI, les recommandations ne mentionnent pourtant à ce jour que les associations de clopidogrel et d'antagonistes de la vitamine K (VKA) ou de faibles doses de NACO1 (tableau 2). Compte tenu des données limitées disponibles actuellement pour ce qui concerne l'utilisation du ticagrélor, plus puissant, ou du prasugrel en association avec les VKA, ces associations conservent jusqu'à présent une indication de classe IIIc. Le problème de l'imprévisibilité du clopidogrel en matière d'inhibition plaquettaire (cf. non-répondeurs) a cependant été soulevé par le Pr W. Desmet comme facteur limitant du clopidogrel et pourrait d'ailleurs s'utiliser comme argument en faveur du ticagrélor ou du prasugrel. Les études à venir devront faire la lumière sur le sujet.
Dans le cas où une anticoagulation est nécessaire, les recommandations actuelles n'établissent pas clairement la durée de l'éventuelle tri- ou bithérapie, qui dépend en réalité de l'estimation du risque hémorragique, d'une part, et du risque ischémique du patient individuel, d'autre part. En pratique, cette considération demeure souvent complexe et différents critères déterminent tant le risque ischémique que le risque hémorragique. Une évaluation clinique correcte reste donc primordiale et peut aussi entraîner, chez un patient individuel, une décision thérapeutique qui s'écarte des recommandations usuelles.
Le patient atteint d'un diabète sucré (Pr O. Gach)
Le Pr O. Gach a présenté le cas d'un patient diabétique avec STEMI aigu dans la paroi antérieure. Les recommandations actuelles indiquent en classe Ia l'instauration la plus rapide possible d'un inhibiteur de P2Y12 chez le patient STEMI.1 Malgré les preuves plutôt limitées en la matière, toute l'assemblée suivait cette recommandation. Dans l'étude ATLANTIC, nous avons vu que l'administration d'une dose de charge de ticagrélor avant l'hospitalisation de patients STEMI n'entraînait pas d'amélioration significative de la reperfusion.4 L'absorption gastro-intestinale, ralentie pendant un ACS et qui freine donc l'apparition de l'effet antiagrégant du ticagrélor, pourrait être une explication. Qui plus est, le délai DTB (door-to-balloon) était particulièrement court dans cette étude: il n'y avait qu'une différence de 31 minutes entre le groupe traité avant l'arrivée à l'hôpital et le groupe traité au laboratoire de cathétérisme. En revanche, on a noté un bénéfice significatif au niveau de la prévention des thromboses de stents précoces, ce qui peut malgré tout plaider en faveur d'une dose de charge précoce. Dans le même ordre d'idée, l'étude ACCOAST n'a pas montré de bénéfice d'une dose de charge de prasugrel avant l'hospitalisation, bien qu'il s'agisse là d'une population NSTEMI.5 Le Pr Gach a ensuite étayé les recommandations actuelles, publiées en 2017, au moyen de données issues de sa propre pratique. Il a ainsi montré que l'instauration préhospitalière d'inhibiteurs puissants de P2Y12 à des patients STEMI traités par PCI donnait un bénéfice en termes de mortalité, sans augmentation significative des complications hémorragiques, et ce dans une période recensant à peine 10 % de procédures radiales (personal communication, in press).
Pour le traitement à long terme, allant jusqu'à 12 mois, le ticagrélor et le prasugrel ont tous deux montré un avantage significatif sur le clopidogrel.6, 7 La prudence reste toutefois de mise lorsque l'on compare le ticagrélor et le prasugrel. Ainsi, l'étude PLATO a inclus un plus grand nombre de patients STEMI que l'étude TRITON-TIMI 38, et les patients du bras clopidogrel de l'étude PLATO ont généralement reçu une dose de charge plus élevée. Le prasugrel s'est accompagné d'un nombre significativement réduit d'infarctus du myocarde et d'un nombre réduit de thromboses de stents, tandis que le ticagrélor a en outre pu se targuer d'une mortalité totale moindre. La poursuite de la DAPT pendant plus de 12 mois ne s'est cependant pas révélée efficace sur le long terme, induisant par ailleurs un risque hémorragique accru.
Toutefois, le nombre de patients ACS inclus dans les études était trop réduit. Sans oublier que les stents à élution médicamenteuse de 2e génération n'étaient pas encore souvent utilisés. Pour couronner le tout, il est difficile de faire une comparaison directe entre les études sur la DAPT compte tenu des différentes définitions qu'elles utilisent pour décrire les hémorragies. Néanmoins, en 2014 et 2015, les études DAPT et PEGASUS TIMI 54 sont parvenues à démontrer pour la première fois, dans un contexte randomisé et contrôlé contre placebo, une diminution des événements ischémiques avec une DAPT de plus de 12 mois, et ce sans augmentation significative des hémorragies majeures.2, 8
Le diabète est un facteur de risque indépendant d'événements ischémiques, qui peut s'expliquer par une activité accrue des plaquettes, un turnover accéléré des plaquettes et la nécessité de doses supérieures d'antiplaquettaires chez les diabétiques. Il se peut dès lors que les patients diabétiques tirent plus de bénéfice d'une thérapie antiplaquettaire plus intensive. Cette hypothèse est étayée par les études GPIIb-IIIa, chez des patients NSTEMI, et par l'étude TRITON-TIMI 38, qui n'ont relevé aucune augmentation des complications hémorragiques.
Le Pr Gach a encore attiré l'attention du public sur le fait que le pronostic des patients atteints d'insuffisance cardiaque et de diabète est moins favorable que celui des insuffisants cardiaques non diabétiques et que, à l'inverse, la mortalité est 10 x plus élevée parmi les diabétiques avec insuffisance cardiaque que chez les diabétiques sans insuffisance cardiaque. Les résultats des études EMPAREG et CANVAS sont également prometteurs à cet égard. Depuis peu, nous disposons - en parallèle aux antiplaquettaires - d'une classe de médicaments antidiabétiques grâce à laquelle les cardiologues et les endocrinologues peuvent cumulativement atteindre une réduction du risque relatif de mortalité cardiovasculaire de l'ordre de 14 %.9, 10 Les études à venir devront confirmer le véritable potentiel des inhibiteurs de SGLT2 en prévention cardiovasculaire tant primaire que secondaire chez les patients diabétiques.
Conclusion
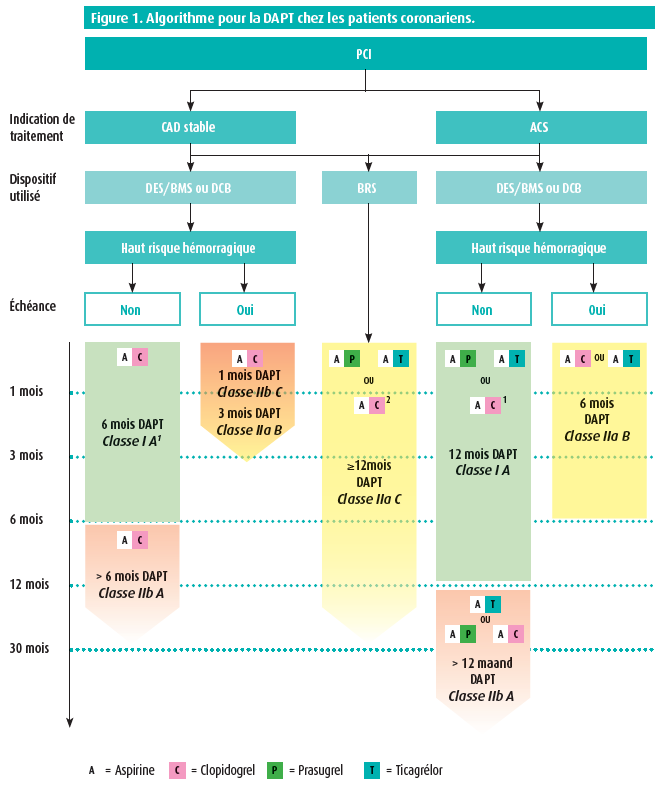
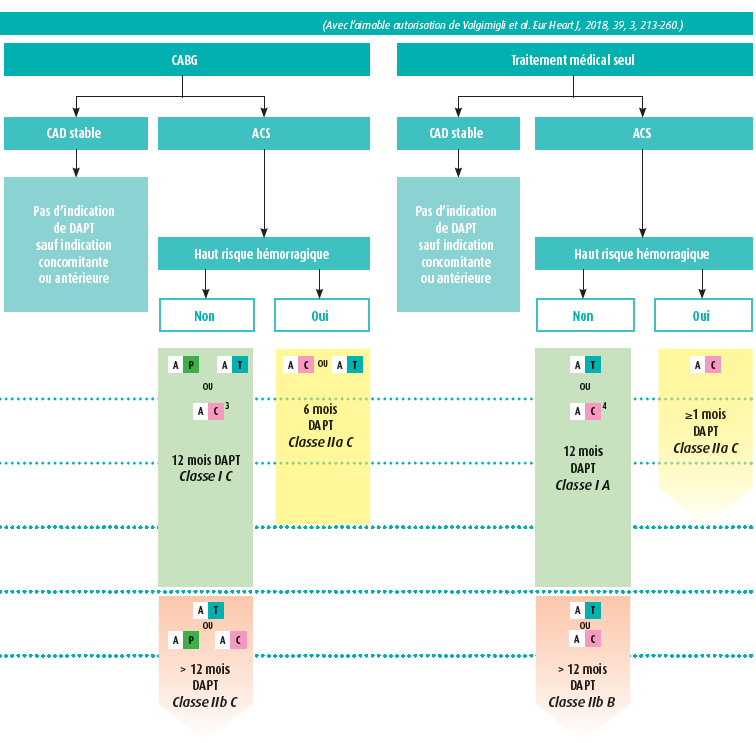
Dans la lignée des résultats d'études récentes, les recommandations actuelles pour la DAPT soutiennent pour la première fois la DAPT prolongée au-delà de 12 mois. Dans un premier temps, cette recommandation concerne un groupe sélectionné de patients ACS à haut risque, à condition qu'aucune complication hémorragique ne soit survenue durant la première année. Une signalisation précoce des patients pouvant entrer en considération semble importante et une estimation individuelle du risque hémorragique et du risque ischémique demeure primordiale en ce sens.
Références
- Valgimigli, M., Bueno, H., Byrne, R. A., Collet, J. P., Costa, F., Jeppsson, A., et al. 2017 ESC focused update on dual antiplatelet therapy in coronary artery disease developed in collaboration with EACTS: The Task Force for dual antiplatelet therapy in coronary artery disease of the European Society of Cardiology (ESC) and of the European Association for Cardio-Thoracic Surgery (EACTS). Eur Heart J, 2018, 39 (3), 213-260.
- Bonaca, M. P., Bhatt, D. L., Cohen, M., Steg, P. G., Storey, R. F., Jensen, E. C., et al. Longterm use of ticagrelor in patients with prior myocardial infarction. N Engl J Med, 2015, 372, 19, 1791-1800.
- Magnani, G., Storey, R. F., Steg, G., Bhatt, D. L., Cohen, M., Kuder, J., et al. Efficacy and safety of ticagrelor for long-term secondary prevention of atherothrombotic events in relation to renal function: insights from the PEGASUS-TIMI 54 trial. Eur Heart J, 2016, 37, 4, 400-408.
- Montalescot, G., van 't Hof, A. W., Lapostolle, F., Silvain, J., Lassen, J. F., Bolognese, L., et al. Prehospital ticagrelor in ST-segment elevation myocardial infarction. N Engl J Med, 2014, 371 (11), 1016-1027.
- Montalescot, G., Bolognese, L., Dudek, D., Goldstein, P., Hamm, C., Tanguay, J. F., et al. Pretreatment with prasugrel in non-ST-segment elevation acute coronary syndromes. N Engl J Med, 2013, 369 (11), 999-1010.
- Wallentin, L., Becker, R. C., Budaj, A., Cannon, C. P., Emanuelsson, H., Held, C., et al. Ticagrelor versus clopidogrel in patients with acute coronary syndromes. N Engl J Med, 2009, 361 (11), 1045-1057.
- Wiviott, S. D., Braunwald, E., McCabe, C. H., Montalescot, G., Ruzyllo, W., Gottlieb, S., et al. Prasugrel versus clopidogrel in patients with acute coronary syndromes. N Engl J Med, 2007, 357 (20), 2001-2015.
- Mauri, L., Kereiakes, D. J., Yeh, R. W., Driscoll-Shempp, P., Cutlip, D. E., Steg, P. G., et al. Twelve or 30 months of dual antiplatelet therapy after drug-eluting stents. N Engl J Med, 2014, 371 (23), 2155-2166.
- Scirica, B. M., Bhatt, D. L., Braunwald, E., Steg, P. G., Davidson, J., Hirshberg, B., et al. Saxagliptin and cardiovascular outcomes in patients with type 2 diabetes mellitus. N Engl J Med, 2013, 369 (14), 1317-1326
- Neal, B., Perkovic, V., Mahaffey, K. W., de Zeeuw, D., Fulcher, G., Erondu, N., et al. Canagliflozin and Cardiovascular and Renal Events in Type 2 Diabetes. N Engl J Med, 2017, 377 (7), 644-657.
Niets van de website mag gebruikt worden voor reproductie, aanpassing, verspreiding, verkoop, publicatie of commerciële doeleinden zonder voorafgaande schriftelijke toestemming van de uitgever. Het is ook verboden om deze informatie elektronisch op te slaan of te gebruiken voor onwettige doeleinden.