Compte rendu de session - Congrès de l'EHRA
Dans le contexte de la pandémie de COVID-19, le dernier congrès de l'EHRA s'est pour la première fois tenu entièrement en ligne, consacrant une grande part de son attention aux nouvelles tendances dans la device therapy. Le samedi 24 avril, une session de 'pour ou contre' a été dédiée à deux sujets spécifiques : d'une part, la stimulation du système de conduction (SSC) et, d'autre part, le rôle du défibrillateur automatique implantable sous-cutané (DAI-SC).
Stimulation du système de conduction (SSC) vs stimulation ventriculaire droite (SVD)
Gaurav Upadhyay (USA) vs Michael Glikson (ISR)
Depuis le développement du premier stimulateur cardiaque, en 1958, la sonde de stimulation est traditionnellement positionnée au niveau de l'apex du ventricule droit. Il est assez rapidement devenu évident que la stimulation apicale ventriculaire droite peut provoquer une dyssynchronie induite par la stimulation et ainsi déboucher sur une insuffisance cardiaque induite par la stimulation (ICIS). L'ICIS est définie comme une diminution de la fraction d'éjection ventriculaire gauche (FEVG) > 10 % après l'implantation du stimulateur, lors de stimulation ventriculaire droite > 20 % et après exclusion d'autres causes de dysfonction ventriculaire gauche (ischémie aiguë, valvulopathie, arythmie auriculaire, …). L'incidence n'est pas clairement établie, mais, selon la définition, elle est décrite entre 10 % et 60 % dans les études. Une étude de suivi sur la base d'un registre danois portant sur 27 700 patients note une incidence de 11 % pendant une période de suivi de 2 ans après l'implantation d'un stimulateur cardiaque1. Dans une étude de registre américaine, on a rapporté jusqu'à 38 % plus souvent d'insuffisance cardiaque d'apparition récente dans les 6 premiers mois suivant l'implantation du dispositif dans le groupe traité pour des troubles de la conduction AV, et ayant donc un plus grand besoin de stimulation ventriculaire droite, par rapport au groupe de patients avec maladie du noeud sinusal. La cause cadre dans la séquence d'activation du myocarde lors de simulation ventriculaire droite (apicale, septale ou au niveau de la voie d'éjection), laquelle ne recourt pas au système normal de conduction his-purkinje. Les médiateurs pour le développement d'une insuffisance cardiaque induite par la stimulation sont une perfusion myocardique réduite, une augmentation du travail myocardique, une augmentation de la désorganisation myofibrillaire (au niveau cellulaire) et une augmentation de l'inflammation et de l'apoptose. Une analyse rétrospective révèle les facteurs de risque suivants : stimulation VD > 20 %, durée du QRS stimulé > 140 ms, sexe masculin et antécédent d'infarctus aigu du myocarde ou d'autre cardiomyopathie.
La stimulation du système de conduction (SSC) vise le positionnement spécifique de la sonde de stimulation au niveau du système de conduction natif, ce qui permet par la suite d'obtenir une contraction physiologique des ventricules grâce à la séquence d'activation du myocarde via le réseau his-purkinje. Dans la stimulation du faisceau de his (SFH), la sonde ventriculaire est placée au niveau du faisceau de his, ce qui entraîne une contraction cardiaque plus physiologique après la stimulation (sélective ou non sélective) et un complexe QRS stimulé plus étroit. Dans une étude de 20192, l'upgrading vers la SFH chez des patients qui avaient développé une insuffisance cardiaque sous une stimulation classique du ventricule droit a conduit à un raccourcissement de la durée du QRS, à une amélioration de la fraction d'éjection et à une amélioration de la capacité fonctionnelle (NYHA) (figure 1). Dans une étude de cohorte prospective, la SFH a entraîné une réduction de risque de 31 % pour un critère d'évaluation combiné (décès, hospitalisation pour insuffisance cardiaque ou nécessité d'upgrade vers une TRC) par rapport à la stimulation ventriculaire droite classique3.
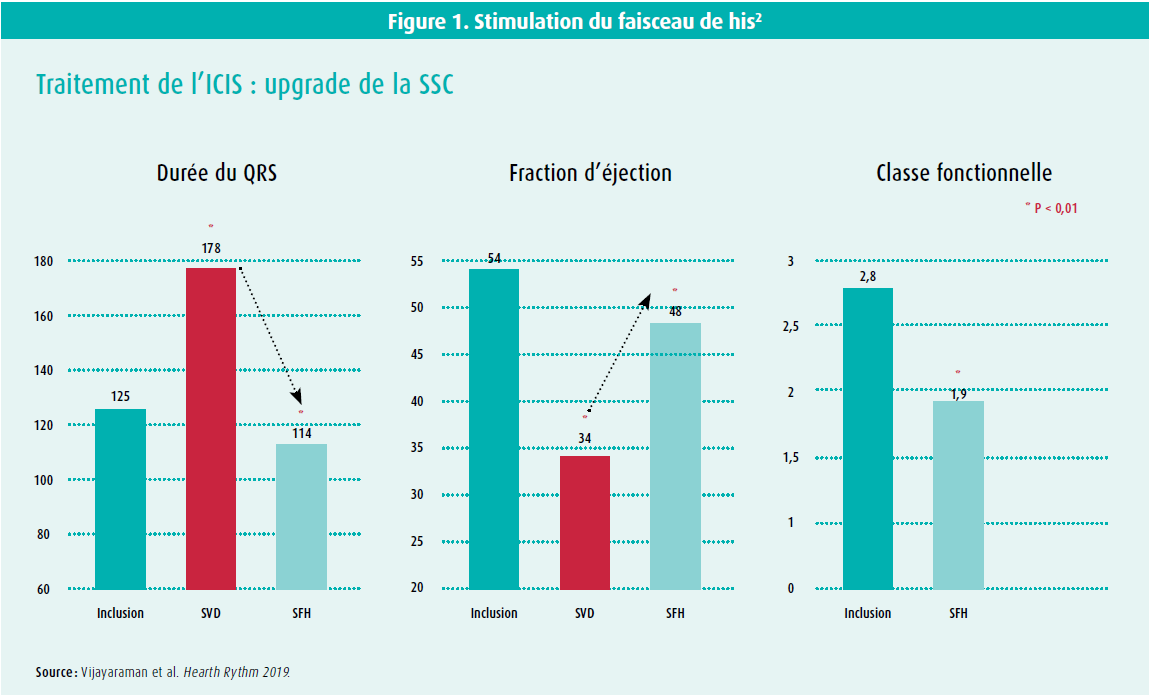
Plus récemment, l'accent a davantage été mis sur le système de conduction distal. Lors d'une stimulation de la branche gauche (SBG), on obtient - en positionnant la sonde au niveau du côté gauche du septum, dans la région de la branche gauche - une contraction physiologique comparable sans dyssynchronie ventriculaire. Cette technique était initialement décrite comme stratégie de sauvetage en cas d'échec du positionnement de la sonde VG pendant l'implantation d'un dispositif de TRC, mais elle a rapidement évolué vers un champ plus large chez des patients avec indication de stimulation liée à une bradycardie. La SBG a donc les mêmes avantages que la SFH, notamment une séquence de contraction physiologique, mais sans les inconvénients décrits avec la SBG (valeurs limites élevées, valeurs basses de détection de l'onde R et, de ce fait, moins de révisions liées à la sonde). La poursuite des innovations et l'extension de la disponibilité d'outils de délivrance par l'industrie peuvent également aboutir à un taux plus élevé de réussite des procédures, à un nombre moins élevé de complications et à une meilleure issue pour les patients ayant une indication de stimulation.
Bien que la stimulation du système de conduction soit une technique prometteuse, nous devons tenir compte de ses limites actuelles. Nous manquons actuellement de vastes études contrôlées et randomisées comparant la stimulation du système de conduction à la stimulation ventriculaire droite. Nous notons par ailleurs un plus grand besoin de révision de la sonde avec la SFH (> 10 %). Nous devons également tenir compte du fait que nous disposons, avec la thérapie de resynchronisation cardiaque (TRC), d'une technique étayée par des données robustes et validée dans de multiples essais randomisés contrôlés (ERC). À ce jour, la stimulation de la branche gauche ne bénéficie pas de données spécifiques issues d'études randomisées (mais des ERC sont en cours). Par ailleurs, diverses inquiétudes restent encore sans réponse, comme l'absence de suivi à long terme, le potentiel effet néfaste de l'activation retardée du ventricule droit, les risques associés à la procédure de positionnement septal profond et les risques en cas de nécessité d'extraire la sonde de la BG (par exemple dans le contexte d'une endocardite sur sonde). Nous devons également tenir compte du fait que l'électrode s'utilise hors indication lorsqu'elle est positionnée sur la branche gauche. Pour l'heure, l'indication de SFH reste limitée à une indication de classe 2A en cas d'échec de l'implantation d'un système de TRC et à une indication de classe 2B après une stimulation classique du ventricule droit pour une indication antibradycardique en cas de fonction ventriculaire gauche préservée, et également à une indication de classe 2B après l'implantation d'un système de TRC chez des patients dont la fraction d'éjection est diminuée.
Défibrillateur automatique implantable sous-cutané (DAI-SC) vs transveineux (DAI-TV)
Liesbeth Timmers - Belgique vs Haran Burri - Suisse
Le premier défibrillateur automatique implantable sous-cutané (DAI-SC) a été implanté en 2008, il y a donc déjà 13 ans. La principale différence avec le système transveineux conventionnel (DAI-TV) est que l'électrode du DAI-SC se situe sous la peau. Nous savons que le système transveineux a quelques défauts. Il y a, d'une part, les complications spécifiques pendant l'implantation et juste après, notamment la tamponnade, le pneumothorax et la dislocation de la sonde. D'autre part, nous observons aussi des complications à long terme (défaillance de la sonde, endocardite). Une récente méta-analyse établit le risque de présenter les effets indésirables suivants comme suit : pneumothorax 1,1 % ; hématome 1,2 % ; dislocation de la sonde 3,1 % ; infection 1,5 %.6 Il ressort de données relativement anciennes (2007) que, sur un délai de 5 ans, il peut survenir jusqu'à 15 % de défaillance de l'électrode, et même jusqu'à 20 % à plus long terme (10 ans)5. Outre la nécessité de révisions, avec la morbidité et la mortalité périopératoires y associées, ce phénomène est aussi responsable d'une importante charge psychologique.
Le DAI-SC, dont l'électrode se situe sous la peau, et non dans le vaisseau sanguin, nous permet de réduire ces risques périprocéduraux (tamponnade, perforation, pneumothorax) et, bien qu'une infection reste possible, elle sera limitée, le cas échéant, à une infection locale accompagnée d'un moindre risque d'infection systémique et/ou d'endocardite sur sonde. Nous disposons aujourd'hui de nombreuses études ayant évalué l'efficacité et la sécurité du DAI-SC par rapport à celles du DAI-TV. L'an dernier, l'étude PRAETORIAN6 a montré une comparaison randomisée entre les deux systèmes et le DAI-SC s'est révélé non inférieur au DAI-TV pour un critère d'évaluation principal composé de complications liées au dispositif et de chocs inappropriés. Le nombre de chocs inappropriés était plus élevé dans le groupe DAI-SC (9,7 % dans le groupe DAI-SC vs 7,3 % dans le groupe DAI-TV), mais sans différence significative, et peut encore être amélioré par la disponibilité du filtre Smartpass (activé chez seulement 20 % des patients dans l'étude PRAETORIAN).
La figure 2 reprend les recommandations actuelles pour le DAI-SC, les recommandations européennes appliquant une classe IIa pour les patients avec indication de DAI (sans nécessité de stimulation antibradycardique, TRC ou stimulation antitachycardique). Les recommandations américaines décrivent un champ d'indication comparable et ajoutent une indication de classe I pour les patients présentant un accès veineux difficile et/ ou un risque accru d'infection.
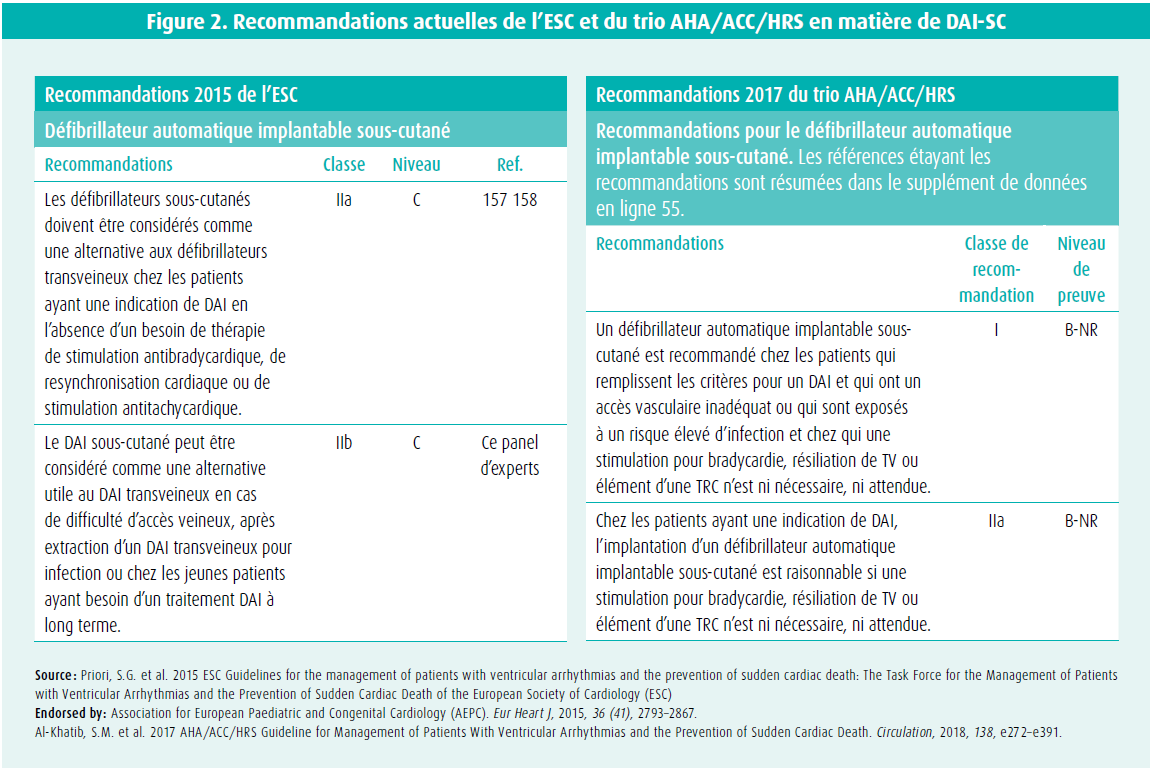
Bien que les données ci-dessus étayent la sécurité et l'efficacité du DAI-SC, nous devons tenir compte de plusieurs éléments détaillés dans la dernière partie.
Tous les patients ne sont pas éligibles à l'implantation d'un DAI-SC. Nous voyons que, lors de la sélection par ECG réalisée avant l'implantation, jusqu'à 17,7 % des patients n'avaient qu'un seul vecteur jugé adapté. Nous observons par ailleurs que l'analyse des données de l'étude MADIT-II révèle que jusqu'à 5 % des patients ayant une indication de DAI sans nécessité de stimulation antibradycardique développent malgré tout une indication de TRC ou de stimulation dans les 20 mois qui suivent. Il s'avère en outre que jusqu'à 90 % des arythmies ventriculaires connues entrent en considération pour un traitement par simulation antitachycardique7. Nous devons également tenir compte du fait que, bien que le DAI-SC puisse théoriquement offrir un avantage esthétique (car il n'est pas positionné devant les pectoraux), jusqu'à 50 % des patients signalent que le DAISC engendre plus de douleur qu'ils le pensaient et jusqu'à 40 % des femmes ressentent une gêne lorsqu'elles portent un soutien-gorge.
Nous devons également prendre en compte le fait que l'incidence de défaillance de la sonde est nettement plus faible avec les électrodes récentes (2 % sur un suivi de 10 ans), par rapport aux données historiques que l'on utilise souvent pour les comparaisons. Par ailleurs, il s'avère que l'électrode du DAI-SC peut, tout comme l'électrode transveineuse, être sensible aux problèmes techniques comme en témoigne la mise en garde de la FDA relative à l'électrode sous-cutanée Emblem (décembre 2020). Une récente série de patients ayant subi un remplacement de batterie du DAI-SC révèle que 10 à 20 % des patients échouent au test du seuil de défibrillation, possiblement en raison d'une fibrose autour de la sonde9. Pour terminer, citons encore les possibilités limitées de programmation, la durée de vie de la batterie, le coût du système DAI-SC et l'anesthésie nécessaire pendant la procédure.
Conclusion
Les actuelles avancées technologiques et le développement de nouvelles perspectives, de nouvelles techniques et de nouveaux outils sont à l'origine d'évolutions rapides dans le domaine de la device therapy. L'objectif ultime est d'atteindre une efficacité optimale et une sécurité maximale pour le patient. En ce sens, la stimulation du système de conduction (SSC) offre une stimulation plus physiologique, réduit le risque de cardiomyopathie induite par la stimulation et peut, après validation dans des études randomisées, se positionner pour le patient ayant une indication de stimulation antibradycardique et/ou de resynchronisation cardiaque. Le DAI sous-cutané (DAI-SC) peut offrir une solution aux inconvénients connus des électrodes transveineuses, en tenant compte des limites du système actuel (pas de stimulation possible pour bradycardie, pour resynchronisation ou pour SAT). Le développement plus poussé du DAI-SC, suivi d'une comparaison validée avec les derniers systèmes DAI-TV en date, déterminera s'il pourra conserver et/ou étendre sa position.
Références
- Tayal, B. et al. Incidence of heart failure after pacemaker implantation: a nationwide Danish Registry-based follow-up study. Eur Heart J, 2019, 44, 3641-3648.
- Vijayaraman, P. et al. Prospective evaluation of feasibility and electrophysiologic and echocardiographic characteristics of left bundle branch area pacing. Heart Rhythm, 2019, 12, 1774-1782.
- Vijayaraman, P. et al. His-Purkinje Conduction System Pacing Following Transcatheter Aortic Valve Replacement: Feasibility and Safety. J Am Coll Cardiol EP, 2020, 6, 649-657.
- Kleemann, T. et al. Annual rate of transvenous defibrillation lead defects in implantable cardioverter-defibrillators over a period of >10 years. Circulation, 2007, 19, 2474-2480.
- Ezzat, V.A. et al. A systematic review of ICD complications in randomised controlled trials versus registries: is our 'real-world' data an underestimation? Open Heart, 2015, 2.
- Knops, R.E. et al. Subcutaneous or Transvenous Defibrillator Therapy. N Engl J Med, 2020, 383, 526-536.
- Wathen, M.S. et al. Prospective randomized multicenter trial of empirical antitachycardia pacing versus shocks for spontaneous rapid ventricular tachycardia in patients with implantable cardioverter-defibrillators: Pacing Fast Ventricular Tachycardia Reduces Shock Therapies (PainFREE Rx II) trial results. Circulation, 2004, 17, 2591-2596.
Niets van de website mag gebruikt worden voor reproductie, aanpassing, verspreiding, verkoop, publicatie of commerciële doeleinden zonder voorafgaande schriftelijke toestemming van de uitgever. Het is ook verboden om deze informatie elektronisch op te slaan of te gebruiken voor onwettige doeleinden.